Министерство образования Российской Федерации
Уссурийский Государственный Педагогический Институт
Биолого-химический факультет
Курсовая работа
Пятая побочная подгруппа Переодической системы элементов Д.И. Менделеева
Выполнила:
студентка 2 курса 521 группы
Савенко О.В._________
Научный руководитель:
Ст. преподаватель
Карпенко Н.Н._________
Уссурийск, 2001 г.
Содержание :
Глава I. Ванадий…………………………………………
I.1. История открытия элемента…………………………………………………
I.2. Характеристика элемента……………………………………………..….
I.3. Распространенность в природе………………………………………….
I.4. Химические свойства ванадия…………………………………………….
I.5. Оксиды ванадия…………………………………………………………….
I.6. Ванадиевые кислоты, основания и соли…………………………………
I.7. Органические соединения ванадия………………………………………
I.8. Потенциальная опасность для здоровья…………………………………
I.9. Физиологическое значение………………………………………….
I.10. Области применения ванадия……………………………………………..
Глава II. Характеристика элементов ниобия и
тантала…………………………………………………………………..
II.1. История открытия элементов…………………………………
Глава III. Ниобий…………………………………………………..
III.1. Ниобий в свободном состоянии………………………………………
III.2. Химические свойства ниобия………………………………………….
III.3. Оксиды ниобия, кислоты и их соли…………………………………..
III.4. Соединения ниобия…………………………………………………….
Глава IV. Тантал…………………………………………………………
IV.1. Тантал в свободном состоянии………………………………………….
IV.2. Химические свойства тантала…………………………………………….
IV.3. Химия танталовых соединений…………………………………………….
IV.4. Применение тантала и ниобия………………………………………………
Глава V. Нильсборий…………………………………………………
Литература…………………………………………………………
Глава I. Ванадий
I
.1 История открытия элемента
Ванадий назван в честь богини
красоты древних скандинавов — легендарной Фреи
Ванадис.
Это имя элементу дал в 1831 г. Гавриил Сефстрем,
профессор Горно
го института в Стокгольме,
Он выделил элемент из шлака, получающег
ося при плавке руды в доменных пе
чах. Работу Г. Сефстрем
осуществил вместе со своим
ученико
м Иоганном Якобом Берцелиусом.
Объективность
требует сказать
, что до Г. Сефстрема
этот элемент уже был выделен, и даже
не один
, а два раза. В 1801
г. мексиканский ми
нералог А
ндрес Мигу
эль
дель
Рио
обнаружил в бурой свин
цовой
руде не встречавшийс
я прежде элеме
нт и наз
вал его
«эритронием».
Однако он усомнился в своих выв
одах и решил, что име
ет дело с недавн
о открытым хром
ом, поэтому н
е об
народовал своей находки. Чуть раньше
Г. Сефстрема
к открытию этого элемента подошел Фридри
х Вёлер,
тот самый, с именем которого связывают пе
рвый в истории си
нте
з органического вещества в лаборатории. Ф. Вёлер исследовал привезенные и
з Мексики руды (с которыми им
ел дело и Дель
Рио) и обнаружил в ни
х нечто
необычное, но тут он некстати заболел, а когда возобновил ра
боту и определил,
ч
то имеет дело с новым элементом, то было уже поздн
о —
Г. Сефстрем
к этому времени опубли
ков
ал и
звестие о с
воем открытии
. Таким образом, честь открытия ванадия оставалас
ь з
а Г. Сефстремом.
Реклама

Ф. Велер
же, «проз
евавший» ванадий, так написал др
угу о своей неудач
е: «
Я был настоящим ослом,
проглядев новый элемент в бурой свинцовой руде, и прав был Берцелиус,
когда он
не без иронии
смеялся над тем, как неудачно и
слабо, без упорства, стучался я в дом богини Ванадис»
.
Однако на самом деле Сефстрем
выделил и
з шлака не чи
стый металл, а твердые и
жаростойкие его соединения — карбиды ванадия. Он получил порошок черного цвета, а в чистом ви
де ванадий — ковкий металл св
етло серого цвета. Но это выяснилось лиш
ь после 1667 г. (т. е.
более тридцати лет спустя после открытия Г. Сефстрема),
когда ванадий и его соединения как следует изучили Ген
ри Энфильд
Роско
и Эдуард Горне. В 1869 г. Г. Роско удалось впервые получить ванади
й 96-процентной чистоты. Металл оказался хрупким и тве
рдым, но только,
что несколькими строчками
выше говорилось,
что ванадий — ковкий, а не хрупкий. Противоречия здесь нет. По мере
удалени
я оставшихся 4% примесей ванадий становится
все более пластич
ным и ковким. Впервые чистый ванадий получен в 1927 г.
I
.2. Характеристика элемента
Ванадий считают как бы связующим между элементами первой и побочной подгрупп V группы. Его химия напоминает химию подгруппы азота тем, что в степени окисления +5 ванадию соответствует кислота НVО3
, гораздо более устойчивая, чем кислоты сурьмы и висмута — членов главной подгруппы. В то же время этот элемент образует простое вещество, которое, подобно другим членам побочной подгруппы, является типичным устойчивым тугоплавким металлом.
Реклама

По количеству степеней окисления ванадий напоминает азот. Ни у кого из его аналогов (ни у ниобия, ни у тантала) нет такого количества степеней окисления, как у ванадия. Точно известны четыре его состояния: +2, +3, +4 и +5. У азота есть еще два других: +1 и -3. Относительно недавно появилось сообщение о том, что при содержании кислорода 14,5—15,5 % происходит образование σ-фазы, близкой по составу к V2
O. Наличие степени окисления +4 и +1 подтверждается органическими производными ванадия. Что же касается соединений с водородом, когда формально степень окисления соответствует -3, то ванадий обладает способностью растворять водород и при этом образовывать с ним гидрид.
По стабильности валентные состояния ванадия неравноценны. В обычных условиях самым устойчивым состоянием будет +4. В это состояние он может быть переведен из +3 даже молекулярным кислородом, а из +5 восстановлен мягкими восстановителями. На этом основана, кстати сказать, ванадатометрия -определение при помощи соединений ванадия присутствия, например, ионов Fe2+
, Os4+
, Mo+5
.
I
.3. Распространенность в природе
На его долю приходится пять из каждых ста тысяч атомов земной коры. Однако число богатых месторождений невелико. Первое из них было обнаружено в 1902г. в Испании - ванадий сопутствовал свинцу. Исключительной по своему содержанию является руда, добываемая на высоте 4700 м в Перу: она состоит из сульфида ванадия – V2
S5
. При обжиге получается одновременно два нужных экономике продукта: оксид серы (IV), необходимый для получения серной кислоты, и ванадий - для оборонной промышленности. Ведь ванадий - стратегическое сырье, без него не обходится производство специальных сортов стали.
Всего известно более 65 минералов, включающих ванадий. Интересной особенностью распространения этого элемента является его содержание в ископаемых растительного происхождения: углях, нефти, горючих сланцах и др. Вода морей содержит 0,3 г ванадия на 1000 т, и некоторые обитатели морей (морские ежи, голотурии) включают его в состав своего организма.
Долгое время не получали чистый ванадий, а когда это произошло, то оказалось, что свойства даже 96% ванадия резко отличаются от свойств 100 %. Это металл серебристо-серого цвета, ковкий и пластичный. При температуре, близкой к абсолютному нулю (4,3 К), обладает сверхпроводимостью. Однако даже небольшие примеси кислорода, азота или водорода делают металл твердым и хрупким, как бы переводя его из типичного металла в нетипичный. В таком изменении свойств есть своя логика: по мере того как он все более насыщается кислородом и переходит от VO к V2
O5
, его металлический характер меняется на неметаллический.
Процесс получения чистого ванадия довольно сложный. Сначала стремятся получить его оксид (V2
O5
или V2
O3
) или галогенид (VС13
или VI3
), а затем применяют либо металлотермию:
V2
O5
+ 5Ca = 5CaO+2V;
2VCl3
+ 3Mg== 3MgCl2
+2V,
либо восстановление углем в вакууме:
V2
О3
+ 3C = 3CO+2V,
либо термическую диссоциацию в вакууме на горячей проволоке:
2VI3
= 2V+3I2
Последним способом получают металл высокой чистоты.
I
.3.1. Источники
Основным источником поступления ванадия в подземные воды являются железные и полиметаллические руды, содержащие небольшую примесь ванадия, а также экологические факторы: сточные воды предприятий черной и цветной металлургии, добыча и переработка нефти, сжигание углеводородного топлива (например, выбросы автомобилей). Ванадий имеет свойство связываться с другими элементами и частицами и поэтому в основном задерживается в почве, где и остается длительное время. В растениях обнаруживаются только незначительные следы ванадия, что свидетельствует о его слабом накоплении в растительных тканях.
I
.3.2. Влияние на качество воды
В воде ванадий образует устойчивые анионные комплексы (V4
O12
)4-
и (V10
O26
)6-
. В миграции ванадия существенна роль его растворенных комплексных соединений с органическими веществами, особенно с гумусовыми кислотами. Концентрация ванадия в природных водах ничтожна - сотые и тыс. доли мг/л. В таких количествах ванадий не оказывает сколько-нибудь значительного влияния на качество воды. Очевидно, этот факт и является причиной того, что ни ВОЗ, ни USEPA, ни ЕС содержание ванадия в воде не нормируют. По российским нормам предельно допустимая концентрация ванадия для питьевой воды составляет 0,1 мг
/л
. Практически такие концентрации могут встречаться только при проникновении в подземные воды ванадийсодержащих сточных вод.Технология удаления из воды: обратный осмос, ионный обмен, дистилляция.
I
.4. Химические свойства ванадия
На воздухе ванадий не изменяется, устойчив он к воде, к растворам минеральных солей и щелочей. Кислоты на него действуют только такие, которые одновременно являются окислителями. На холоде на него не действуют разбавленные азотная и серная кислоты. По-видимому, на поверхности металла образуется тончайшая пленка оксида, препятствующая дальнейшему окислению металла («пассивированное состояние»). Для того чтобы заставить пассивированный ванадий интенсивно реагировать, его нужно нагреть. При 600—700°С происходит интенсивное окисление компактного металла, а в мелкораздробленном состоянии он вступает в реакции при более низкой температуре:
2V +5O2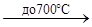 2V2
O5
2V2
O5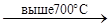 2VO2
+O2
;
2VO2
+O2
;
2V +5F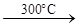 2VF5
; 2VF5
;
 2V +2Cl2
в
токе
хлора
t
VCl4 2V +2Cl2
в
токе
хлора
t
VCl4
Прямым взаимодействием элементов при нагревании могут быть получены сульфиды, карбиды, нитриды, арсениды, силициды. Для техники важны желто-бронзовый нитрид VN (tпл
= 2050°С), устойчивый к воде и кислотам, а также обладающий высокой твердостью карбид VC (tпл
= 2800 °С).
Ванадий очень чувствителен к примесям газов (O2
, N2
, H2
), которые резко меняют его свойства, даже если присутствуют в самых незначительных количествам. Поэтому и сейчас можно в разных справочниках встретить различную температуру плавления ванадия. Загрязненный ванадий, в зависимости от чистоты и способа получения металла, может плавиться в интервале от 1700 до 1900°С. При чистоте 99,8 - 99,9 % его плотность равна 6,11 г
/см
3
при 20°С, температура плавления составляет 1919°С, а температура кипения 3400 °С.
Металл исключительно стоек как в органических, так и в большинстве неорганических агрессивных средах. По стойкости к действию НС1, НВr и холодной серной кислоты он значительно превосходит титан и нержавеющую сталь. С галогенами, за исключением самого агрессивного из них — фтора, соединений не образует. С фтором же дает кристаллы VF5
, бесцветные, возгоняющиеся без превращения в жидкость при 111°С. Атмосфера из углекислого газа на металлический ванадий действует значительно слабее, чем на его аналоги - ниобий и тантал. Он обладает высокой стойкостью к расплавленным металлам, поэтому может применяться в конструкциях атомных реакторов, где расплавленные металлы используются как теплоносители. Ванадий не ржавеет ни в пресной, ни в морской воде, ни в растворах щелочей. Действуют на него лишь расплавленные щелочи:
4V + 12NaOH + 5O2
= 4Na3
VО4
+ 6H2
О
Из кислот на него действуют концентрированная серная и азотная кислоты, плавиковая и их смеси:
V + 4H2
SО4
= V(SО4
)2
+ 2H2
О + 2SО2
Особенностью ванадия считается высокая растворимость в нем водорода. В результате такого взаимодействия образуются твердые растворы и гидриды. Наиболее вероятная форма существования гидридов — металлообразные соединения с электронной проводимостью. Они способны довольно легко переходить в состояние сверхпроводимости. Гидриды ванадия могут с некоторыми твердыми или жидкими металлами образовывать растворы, в которых повышается растворимость водорода.
Самостоятельный интерес представляют карбиды ванадия, так как по своим качествам дают для современной техники материал с весьма ценными свойствами. Они исключительно тверды, тугоплавки и обладают хорошей электрической проводимостью. Ванадий способен для образования своих карбидов даже вытеснить другие металлы из их карбидов:
3V + Fе3
С = V3
С + 3Fе
Известен целый ряд соединений ванадия с углеродом:
V3
С; V2
C; VC; VзС2
; V4
С3
С большинством членов главной подгруппы ванадий дает соединения как бинарные (т. е. состоящие только из двух элементов.), так и более сложного состава. Нитриды образуются при взаимодействии порошка металла или его оксидов с газообразным аммиаком:
6V + 2NН3
= 2V3
N + 3Н2
V2
О2
+ 2NH3
= 2VN + 2H2
О + H2
Для, полупроводниковой техники интерес представляют фосфиды V3
Р, V2
P, VP, VP2
и арсениды V3
As, VAs.
Комплексообразующие свойства ванадия проявляются в образовании соединений сложного состава типа фосфорно-ванадиевой кислоты H7
PV12
O36
или Н7
[Р(V2
O6
)6
].
I
.5. Оксиды ванадия
В системе ванадий - кислород взаимодействие начинается при нагревании до температуры примерно 300°С. Получено большое количество оксидов ванадия, характер которых постепенно меняется при переходе от низших оксидов к высшим. Относительно недавно обнаружен низший оксид V2
О. Он нестоек и по своему характеру близок к металлическому состоянию. Его светло-серые кристаллы отливают металлическим блеском, хорошо проводят электрический ток.
Оксид VO более стоек, нерастворим в воде, но растворяется в разбавленных кислотах с образованием двухзарядного катиона V2+
.
VO + H2
SО4
= VSО4
+ H2
О
Водные растворы ванадия в такой степени окисления окрашены в фиолетовый, или в бледно-голубой цвет. Растворы солей иона V2+
неустойчивы и настолько сильные как восстановители, что при стоянии выделяют водород прямо из воды, а ион ванадия переходит в более устойчивые высшие степени окисления. При добавлении к растворам любого даже слабого основания образуется бурый аморфный осадок V(OH)2
. В чистом виде, однако, выделить его нельзя, так как на воздухе он быстро превращается в серо-зеленый гидроксид V(ОН)3
.
Из особенностей оксида можно отметить существование при определенных концентрациях ванадия димера V2
О2
, а также совершенно особое влияние температуры на его состояние. Оксиды обычно делаются нестойкими при высоких температурах и разлагаются. Здесь же наблюдается совершенно удивительное свойство: оксид VO устойчив лишь при высокой температуре. Даже при медленном и постепенном охлаждении он разлагается и переходит в высшие оксиды.
Оксид ванадия, соответствующий степени окисления +3, имеет амфотерный характер с преобладанием основных свойств. Как кислотные качества можно рассматривать образование им с оксидами MgO, MnO, СаО двойных соединений, а с Fe2
О3
, Сr2
О3
, Аs2
О3
непрерывный ряд твердых растворов. С оксидами же щелочных металлов Li2
О и Na2
О получаются соли LiVO3
, NаVОз, которые можно считать ванадиевыми солями.
Внешне V2
O3
- блестящие черные кристаллы (tпл
= 1970°С), по структуре подобны корунду, в воде, растворах щелочей и кислотах не растворяются, кроме плавиковой и азотной (быстрее всего в кипящей):
V2
O3
+ 6НМОз = 2V(NО3
)3
+ ЗН2
O
Водные растворы таких солей окрашены в зеленый цвет. Из них добавлением аммиака можно осадить рыхлый серо-зеленый осадок, который считается гидроксидом ванадия в степени окисления +3. Отметим, что такое состояние менее устойчиво и менее характерно для ванадия, чем +4 и +5. Поэтому соединения ванадия со степенью окисления +3 стремятся перейти в более стабильное состояние и проявляют, следовательно, свойства восстановителей.
Сине-голубые кристаллы VO2
на воздухе теряют свою форму, так как вещество гигроскопично. Это наиболее устойчивый оксид ванадия, поэтому его можно получить либо окислением низших оксидов:
2V2
О3
+ О2
= 4VО2
,
либо восстановлением высшего:
V2
O5
+ Н2
С2
О4
= 2VО2
+ 2СО2
+ Н2
О
Оксид VO2
амфотерен и одинаково легко растворяется как в основаниях:
4VО2
+ 2NaOH + 6H2
О = Na2
[V4
O5
] • 7Н2
O,
так и в кислотах:
VО2
+ 2HC1 = VОСl2
+ Н2
O;
VO2
+ H2
SO4
= VOSO4
+ H2
O
Водный его раствор не изменяет цвета ни синей, ни красной лакмусовой бумажек, т. е. его амфотерность распределена поровну между кислотными качествами и основными. Водные растворы солей содержат ванадий не в виде простого катиона, а в виде иона ванадила, имеющего две формы существования: VO2+
- и V2
O2
4+
- и придающего синий цвет растворам.
В щелочах образуются соли поливанадиевых кислот H4
V4
O9
или H2
V2
O5
, называются соли ванадитами или поливанадатами. При величине рН = 4 из растворов солей можно осадить серовато-бурый аморфный гидроксид VO(OH)2
. Если щелочность увеличить, при рН от 8 до 10 гидроксид (в соответствии со своими амфотерными качествами) будет растворяться, превращаясь в соли. При сплавлении этого оксида ванадия с оксидами щелочноземельных металлов получаются ванадаты:
VO2
+ CaO = CaVO3
Могут образовываться три ряда ванадатов СаVО3
, Са2
VO4
, Ca3
VO5
со сложной структурой.
Наиболее важным и интересным, с точки зрения химика, считается высший оксид ванадия V2
O5
, который может иметь вид красных или красно-желтых кристаллов либо оранжевого порошка. Получается он по реакции ванадия с кислородом. При 600—700°С взаимодействие идет очень быстро, так как образующийся оксид V2
О5
расплавляется (tпл
= 675°С) и скатывается с поверхности металлического ванадия. Лабораторный способ его получения — из метаванадата аммония;
2NH4
VО3
= V2
О5
+2NH3
+H2
О
Высший оксид ванадия имеет ярко выраженный кислотный характер и при растворении в воде образует ванадиевую кислоту:
V2
О5
+ Н2
О = 2НVО3
Форма существования ванадия в растворе кислоты - в виде катиона VO2+
, цвет раствора желтовато-оранжевый. При растворении оксида ванадия (V) в основаниях получаются соли изомерных ванадиевых кислот, напоминающих фосфаты:
V2
O5
+2NaOH = 2NaVO3
+H2
O
V2
O5
+6NaOH = 2Na3
VO4
+3H2
O
По форме они соответствуют мета
- [НVO3
], орто
- [Н3
VO4
]и H2
V2
O7
пированадиевым кислотам. В этом отношении ванадий обнаруживает сходство уже не с азотом, а с фосфором.
Особенность ванадия (в степени окисления +5) при растворении в сильных кислотах — образовывать комплексные соединения, содержащие до девяти -двенадцати атомов ванадия на молекулу. Другим замечательным свойством оксида можно считать способность в расплавленном состоянии проводить электрический ток, скорее всего вследствие диссоциации на ионы:
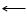  V2
O5
VO2+
+ VO3- V2
O5
VO2+
+ VO3-
А ведь пропускание электрического тока считается безусловной «привилегией» металлов. По этому свойству распознается принадлежность вещества к металлам или неметаллам.
Характер гидратных форм оксидов ванадия меняется закономерно с изменением степени его окисления. В состоянии наибольшего окисления он образует кислоты, подобные кислотам фосфора и мышьяка, элементов, которые являются соседями ванадия, но относятся к противоположной подгруппе. Слово «противоположная» означает, что элементы различных подгрупп одной группы — химические антиподы: для одних должны быть более характерны свойства металлов, а для других — неметаллов. Но при сравнении членов обеих подгрупп можно заметить, что «противоположности» сближаются. У элементов побочной подгруппы все более усиливаются свойства неметаллов, характерные для главной подгруппы, и наоборот.
Ванадий в этом отношении служит примером. В высшей окислительной степени у него преобладают свойства неметалла. При состоянии окисления +4 его гидроксид в одинаковой мере проявляет. Свойства обеих противоположностей, т. е. он амфотерен.
Сопоставив приведенные данные об оксидах ванадия с аналогичными сведениями о подобных соединениях других членов V группы, можно прийти к следующему выводу: по количеству оксидов и по числу состояний окисления ванадий далеко превосходит не только членов побочной подгруппы (это естественно), но и некоторые элементы главной подгруппы. Если судить по кислородным соединениям (именно их особенности несколько десятилетий назад считались основным признаком сходства и различия), то ванадий должен считаться более близким «родственником» азота, чем висмут, сурьма и даже мышьяк. Ведь эти элементы не образуют всех типов оксидов, присущих азоту, а существующие у них по своим свойствам подобны оксидам фосфора.
I.6. Ванадиевые кислоты, основания и соли
Ванадиевая кислота, подобно фосфорной и мышьяковой имеет три формы: НVО3
(мета-),
H3
VO4
(орто-),
H4
V2
O7
(
nupo
-).
Сами кислоты в чистом виде не получаются, но соли их можно осадить из раствора. Например, регулированием кислотности среды можно выделить серебряную соль во всех трех формах (табл. 1).
Таблица 1
| Среда |
РН |
Соль |
| Кислая |
4,3 – 4,7 |
AgVO3
|
| Слабокислая |
5,5 – 5,8 |
Ag4
V2
О7
|
| Почти нейтральная |
6 - 6,5 |
Ag3
VО4
|
Сам собой напрашивается вывод о сходстве солей ванадиевых и фосфорных кислот. Аналогичные соли были выделены и для других ионов металлов (например, соли натрия).
Наиболее устойчивой в водных растворах является метаванадиевая кислота, которая все время именуется как просто ванадиевая. Это соединение обладает признаками амфотерности, которые более значительны, чем у фосфорных кислот. Для нее возможны направления электролитической диссоциации как с отщеплением Н+
, так и ОН-
.
     VO3
-
+ H+
HVO3
= VO2
OH VO2
+
+ ОН- VO3
-
+ H+
HVO3
= VO2
OH VO2
+
+ ОН-
Существование VO2
-
можно доказать тем, что соляная кислота реагирует с раствором ванадиевой кислоты и окисляется до свободного хлора:
  2VO2
+
+ 2HCl 2V02 +
+ Cl2
+ 2OH- 2VO2
+
+ 2HCl 2V02 +
+ Cl2
+ 2OH-
Следовательно, в этом случае проявляются некоторые признаки основания.
По цвету раствора и по солям, выделяющимся из него, можно судить, в форме ионов каких кислот присутствует ванадий в растворе.
При растворении в воде оксида ванадия (V) появляется желтая окраска, которая может меняться и даже исчезать совсем в зависимости от среды. Такая особенность объясняется возможностью ионаVO3
-
существовать в различных формах. Желтый цвет обусловлен присутствием этого иона в тримерной форме [V3
О9
]3-
. При сильно щелочной среде раствор бесцветен: там находятся ионы пиро- и ортованадиевых кислот:
2[V3
09
]3-
+ 60H-
= 3[V2
O7
]4-
+ 3H2
O;
[V2
О7
]4-
+ 2ОН-
= 2[VO4
]3-
+ Н2
О
По мере уменьшения щелочности окраска опять становится желтой и даже оранжевой. Это связано с изменением формы существования иона VO3-
от [V3
О9
]3-
в щелочной среде и [VO4
]3-
в нейтральной до [V6
O17
]4-
в кислой:
3[VО4
]3-
+6H+
= 3[V2
O9
]3-
+ 3H2
О;
2[V3
О9
]3-
+ 2H+
= [V6
Ol7
]4-
+ H2
О
При подщелачивании процесс идет в обратную сторону:
[V6
O17
] 4-
+ 2OН-
= 2[V3
О9
]3-
+ H2
O
Оранжевый цвет приписывается присутствию иона декаванадата:
5 [V6
O17
]4-
+
2Н+
= 3[V10
O28
]6-
+ Н2
О,
который может быть выделен из раствора в виде оранжевой соли кальция Ca3
V10
O28
.
16H2
О. Здесь приведены простейшие формулы. Реально же в небольших количествах присутствуют и другие соединения, заключающие в составе своей молекулы до 12 атомов ванадия.
Из солей ванадиевой кислоты растворимы соли одновалентных металлов (К, Na и т.д.), а ванадаты аммония, двух- и трехвалентных металлов труднорастворимы. Из них особенно важен ванадат аммония. Из него при действии на его раствор сульфида аммония образуется вишнево-красный раствор тиосоли:
NH4
VО3
+ 4(NH4
)2
S + 3H2
О = (NH4
)3
VS4
+ 6NH4
ОH
Пероксид водорода Н-О-О-Н производит в нем замену части атомов кислорода на пероксидную группу -O-O- и превращает его в перванадат:
2NH4
VО3
+ 3H2
О2
= (NH4
)2
H2
V2
О10
+ 2H2
О
Сами по себе и в щелочной среде такие соединения устойчивы, а при подкислении образуются свободные надкислоты общей формулы H4
V2
Ox
(причем x > 7). Они постепенно разлагаются с выделением кислорода. Свойство давать пероксидные соединения характерно и для остальных членов подгруппы ванадия.
Из других солей пятивалентного ванадия достаточно полно охарактеризованы сульфид V2
S5
и единственное соединение с галогенами - пентафторид ванадия VF5
. Первое из этих двух соединений проще всего может быть получено в виде черного порошка нагреванием V2
О3
с серой при 350°С;
2V2
O3
+ 13S = 2V2
S5
+ 3SO2
При нагревании на воздухе он сгорает до V2
S5
, а при 400°С и в отсутствие воздуха способен распадаться на V2
S3
и серу. В воде V2
S5
практически нерастворим, но легко растворяется в щелочах.
Пентафторид может быть легко получен при взаимодействии элементов (300°С), он представляет собой бесцветное кристаллическое вещество. Возгоняется при 111°С, водой VF5
полностью гидролизуется. Ему соответствует комплексная кислота H[VF6
]. Сама она не выделена, но получены соли некоторых металлов - (калия, серебра, бария). К нагреванию они не особенно устойчивы:
 K[VF6
] 330°C
KF+VF5 K[VF6
] 330°C
KF+VF5
В соединениях с серой и фтором ванадий выступает в роли типичного металла.
Таким образом, в кислородсодержащих кислотах и их солях он ведет себя как неметалл, но в других своих соединениях — как металл. Следовательно, пятивалентный ванадий проявляет свойства неметалла, и этому его качеству соответствуют кислоты, но он способен проявлять признаки металличности в некоторых соединениях.
Четырехвалентному ванадию соответствуют предполагаемые кислотыH2
V4
О9
; Н2
VO3
; H4
VO4
и H6
VO5
. Соединения элемента такой степени окисления становятся в растворе производными ванадила.
Ванадиюсо степенями окисления +3, +2 соответствуют основания V(OH)3
и V(OH)2
. Оба они образуются при действии щелочи на растворы, содержащие соответственно ионы V3+
и V2+
. В этих состояниях окисления ионы ванадия ведут себя как типичные ионы металлов. Отличает их разве только неустойчивость. Ванадий стремится перейти в свое самое стабильное состояние +4. Поэтому оба основания на воздухе легко окисляются до степени окисления ванадия +4, т. е. являются восстановителями:
2V(OH)2
+ O2
= 2VO(OH)2
;
4V(ОН)3
+ O2
= 4VО(ОН)2
+ 2Н2
O
Из-за своей неустойчивости в чистом виде гидроксиды не получены. Они могут существовать некоторое время при действии щелочей на растворы солей ванадия: V(ОН)3
в виде рыхлого зеленого осадка, а V(ОН)2
— буро-коричневого.
Однако соли трехкислотного основания V(ОН)3
вполне устойчивы. Безводный трифторид VF3
зеленовато-желтого цвета плавится лишь при температуре выше 800°С. Трихлорид — красно-фиолетовые кристаллы — устойчив в отсутствие влаги. Менее устойчивы бромид и иодид.
Состояние окисления +2 ванадия наименее устойчиво, поэтому ванадий, содержащийся в солях, стремится, отдав электрон или два, перейти в более глубокую степень окисления. Все-таки осторожным восстановлением из смеси паров тетрахлорида и водорода может быть получен дихлорид:
VCl4
+ H2
= VCl2
+ 2HCl.
в виде бледно-зеленых кристаллов. При растворении в воде сначала появляется фиолетовая окраска, которая быстро меняется на зеленую. Происходит переход ванадия из двузарядного иона в трехзарядный:
V2+
-e =
V3+
На этом процесс не заканчивается, ванадий стремится перейти в наиболее стабильное состояние +4. Происходит снова изменение цвета раствора. Подобным же образом ведут себя бромид и иодид.
I
.7. Органические соединения ванадия
Ванадий в деятельности некоторых видов организмов играет важную и далеко еще не установленную роль. Известно, что не только соединения ванадия ядовиты, но также и пыль, появляющаяся при обработке металла. Однако некоторые растения (дуб, сахарная свекла, табак, бук и др.) содержат значительные количества ванадия. Одним из активных собирателей ванадия является бледная поганка, хорошо знакомая каждому грибнику. В крови некоторых морских существ (голотурии, асцидии, морские ежи) содержание ванадия достигает 10 %, а концентрация может в миллиарды раз превышать концентрацию этого элемента в морской воде,
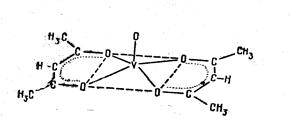 Он обнаружен в куриных яйцах и мясе кур, коровьем молоке и печени животных, есть и в мозгу человека. Следовательно, в небольших дозах он чем-то необходим организмам. Эксперименты по добавлению соединений ванадия в рацион быков и свиней показали, что при этом улучшается аппетит, и животные быстрее прибавляют в росте и массе. Предполагают, что микрокаталитические дозы ванадия ускоряют процессы окисления в биологических системах. Он обнаружен в куриных яйцах и мясе кур, коровьем молоке и печени животных, есть и в мозгу человека. Следовательно, в небольших дозах он чем-то необходим организмам. Эксперименты по добавлению соединений ванадия в рацион быков и свиней показали, что при этом улучшается аппетит, и животные быстрее прибавляют в росте и массе. Предполагают, что микрокаталитические дозы ванадия ускоряют процессы окисления в биологических системах.
рис 1. Органический комплекс ванадия, обладающий каталитической активностью в органических реакциях.
Комплексные ванадиевые соединения с органическими реагентами (рис. 1) находят применение в аналитической химии. Однако вопрос о состоянии ионов ванадия в этих соединениях и сегодня нельзя считать выясненным до конца. Особенно это относится к состоянию ванадия (V). Во многих случаях даже не определено, в какой форме — катионной или анионной — находится ванадий в органических соединениях. При образовании большинства органических соединений с ванадием он может быть в составе либо катионов VO3+
, VO2+
, VO(OH)2+
, либо в виде анионов V4
O11
2-
и V6
O17
4-
.
Многие комплексы ванадия с органическими реагентами интенсивно окрашены и способны к изменению цвета в зависимости от условий процесса и характера среды. Все же следует сказать, что химия органических соединений ванадия еще ждет своих исследователей.
I
.8. Потенциальная опасность для здоровья
Наибольшему воздействию при вдыхании содержащей ванадий пыли подвержены легкие, бронхи, глаза. Рабочие, вдыхавшие такую пыль даже непродолжительное время жалуются на раздражение и хрипы в легких, кашель, боли в груди, насморк и першение в горле. Иногда наблюдается удушье, зеленоватый налет на языке и побледнение кожных покровов. Правда, эти признаки исчезают уже вскоре после прекращения вдыхания загрязненного воздуха. Аналогичные результаты были получены и на животных. По данным Агентства по учету токсических веществ и болезней США. Других типов воздействия ванадия на организм человека не наблюдается. Данные об отрицательном влиянии ванадии при его поступлении с пищей или при кожном контакте отсутствуют. Тем не менее, опыты, проводившиеся на животных показали, что воздействие сверхвысоких доз ванадия приводит к смертельному исходу. У беременных животных, подвергавшихся воздействию несколько меньших доз наблюдались дефекты у новорожденных. У животных, долгое время вдыхавших или получавших с пищей значительные количества ванадия появлялись незначительные проблемы с печенью и почками. Следует отметить, что те дозы ванадия, которые использовались в опытах многократно превышают концентрации, имеющие место в природе.
Департамент здравоохранения США, Агентство по исследованию рака и Агентство по охране окружающей среды США не относят ванадий к числу канцерогенов. При исследовании животных, длительное время получавших повышенные дозы ванадия с водой, рост числа опухолевых заболеваний не выявлен.
I
.9. Физиологическое значение
Суммируя различные источники, можно сказать, что ванадий - это микроэлемент, участвующий в регулировании углеводного обмена, сердечно-сосудистой деятельности (в частности, уменьшает выработку холестерина). Ванадий участвует также в процессах формирования костей и зубов, роста и метаболизма жиров, а также стимулирует рост и репродукцию клеток, действуя при этом как противораковое средство. Ванадий вместе с цирконием, сопутствуя серебру, благотворно действует на функции паренхиматозных органов (печень, селезенка, легкие), щитовидной и поджелудочной желез, гипофиза, половых органов, мышечной системы.
Хотя дефицит ванадия у человека - редкое явление, однако у подопытных животных нехватка ванадия приводит к ухудшению роста зубов, костей, хрящей и мускулов, а также ослаблению функции размножения. Существуют также американские данные о том, что недостаток ванадия связан с развитием диабета. По крайней мере дефицит ванадия, наряду с недостатком хрома и цинка, является одним из важнейших индикаторов симптомов диабета. Депонируется ванадий в основном в костных и жировых тканях.
Уровень суточной потребности организма человека в ванадии не установлен, но по экспертным оценкам составляет около 2 мг в день.
I
.10. Области применения ванадия
Этот элемент получил вполне заслуженно название «витамин для стали». Половина легированных сталей всего мирового производства содержит добавки ванадия. Именно на это в виде феррованадия идет 95% от общего добываемого количества этого металла. Сплав, содержащий ванадий, становится тверже, выдерживает значительные динамические нагрузки и меньше истирается. Ванадий обладает высоким сродством к азоту, кислороду и углероду. Соединяясь с малыми их количествами, он значительно повышает качество стали, делает ее мелкозернистой и более вязкой. Она легче переносит удар и изгиб, лучше противостоит разрыву. Легкость ванадия передается сплавам, и они становятся особенно ценными там, где масса играет решающую роль, — в авиации и автомобилестроении.
Другая основная область его применения — химическая промышленность. Ванадиевые катализаторы сочетают способность ускорять получение весьма ценных продуктов со стойкостью к большинству контактных ядов. Такие катализаторы сыграли решающую роль по усовершенствованию технологии получения серной кислоты и увеличению мощности установок. Другие важные процессы, где используются соединения ванадия: производства анилина, щавелевой кислоты, переработка нафталина и др. Одна массовая часть катализирует превращение 200 тыс. массовых частей соли анилина в краситель — черный анилин.
Из других областей использования ванадия можно указать медицину, где некоторые соединения ванадия применяют как дезинфицирующие и лечебные препараты, а также производство сплавов с алюминием, медью и никелем. Такие сплавы, содержащие добавки ванадия от 0,5 до 20%, улучшают качество бронз и латуней, придают химическую стойкость никелевым сплавам, а золоту сообщают не свойственную ему твердость.
Глава II. Характеристика элементов ниобия и тантала
По размеру, как атомов, так и ионов ниобий и тантал близки друг к другу, поэтому их свойства как элементов целесообразно рассмотреть одновременно. Одинаковые объемы атомов объясняются тем, что член VI периода — тантал следует в этом периоде почти сразу же за лантаноидами, у которых происходит заполнение электронами не внешнего, а третьего снаружи слоя. Это приводит к так называемому лантаноидному сжатию — увеличивающееся количество внутренних отрицательно заряженных электронов сильнее притягивается положительно заряженным ядром. Вследствие этого радиус атома с увеличением порядкового номера элемента не только не увеличивается, но даже несколько уменьшается.
По сравнению со свойствами ванадия характер элементов сдвигается заметно в сторону усиления металлических качеств. Степени окисления меняют свой характер и устойчивость. Низшие положительные степени окисления нестабильны, поэтому их соединения малочисленны и плохо изучены. Отличие от ванадия состоит и в том, что их единственным стабильным состоянием является не +4 (как у V), а .+.5. Причем характер соединений в этом случае для ниобия и тантала несколько различается (например, по кислотным свойствам оксидов).
Разница в химических свойствах ниобия и тантала основывается на различной структуре электронных оболочек их атомов. На внешнем слое у ниобия один электрон, а у тантала — два:
Nb 4d4
5 s1
Та 5d3
6 s2
Следовательно, у ниобия наблюдается отклонение от обычной последовательности заполнения электронами энергетических орбиталей.Один из двух электронов, имевшихся на внешнем слое у идущего перед ниобием элемента (циркония), переходит на 4d-орбиталь внутреннего второго снаружи слоя. Связь электронов с ядром в ячейках 4d4
и 5s1
примерно одинакова: разница составляет всего около 7 эВ. К тому же расположение электронов позволяет им иметь одинаково направленные спины. Эти особенности облегчают атому ниобия возможность использования всех своих пяти валентных электронов при химических реакциях.
Тантал находится в 5d-группе переходных металлов. Структура его атома такова, что в ней сохраняется два электрона на внешнем уровне. При химических взаимодействиях нужно затратить энергию, чтобы произошел переход одного из двух электронов с 6s2
-орбитали на р- или d-орбиталь соответственно внешнего или предвнешнего энергетического слоя. Необходимостью дополнительной энергии и объясняется химическая инертность тантала по сравнению с ниобием. Ниобий и в виде металла химически более активен, и его высший оксид обладает более выраженными кислотными свойствами, чем оксид тантала. В водных растворах ионы ниобия сравнительно легче восстанавливаются, тогда как у тантала все эти качества обнаруживаются в меньшей степени.
В исследованиях по химии этих двух элементов указывается на существование состояний окисления +5, +4, +3, +2 и даже +1. Однако во всех работах отмечается, что соединения ниобия и тантала низших степеней окисления образуются с. трудом и не имеют большого значения в практическом использовании элементов.
II
.1. История открытия элементов
Элементы, образующие в с
емействе V группы свою «
ветвь», похожи друг на друга не только по своим свойствам, но и «
родственники» по названиям: ванадии, ниобий, тантал. Во-первых, наименования всех трех относятся к области мифологи
и. Во-вторых, в названиях указана прямая родств
енная связь: в древнегреческой мифологи
и Ниобея
является дочерью Тантала.
Имя «ниобий» дал эле
менту немецкий химик
Генрих Розе.
Тем самым подчеркивалось сходство нового (как был уверен Г. Розе) элемента с уже известным к 1844 г. танталом. Как оказалось впоследствии, это было второе рождение элемента, первое произошло в 1801 г. Английский ученый Чарлз Хатчет
изучал черный минерал, присланный из н
едавно образовавшихся Соединенных
Штатов
А
мерики. Ра
бота
я с этим минералом, он
выде
лил оксид н
еизвестного прежде элемен
та. Элемент Хатчет
назвал колумбием,
подчеркивая его заокеанское происхождение
. Черный минерал получи
л название «
кол
умбит».
Через год в 1802 г. шведский химик Андерс
Густав Экеберг
обнаружил в одной из финляндски
х руд новый х
имический элемент. А. Экеберг не знал об открытии Ч.
Хатчета
и поэтому новому элементу дал наименова
ние «тантал», а руда стала наз
ываться танталитом. Сходство тантал и колумбия и их соеди
нений между собой было так велико (с точки зрения тогдашних химиков), что свыше сорока лет подавляющее большинство химиков считало: Колумбии
и тантал—один и тот же элемент.
За этим элементом прочно закрепилось названи
е «тантал». Пов
одом к такому названию послужило необычное для металлического оксида
свойство: он не способе
н «насыщаться» — образовывать соли
с кисл
отами
.
Как известно, ми
фологический герой Тантал был осужден богами на вечный голод и жажду. Муки
его усугублялись видом все время ускользающ
их от его уст водян
ых
струй и сочных плодов
.
Сильно меняющаяся от образца к образцу плотность окси
да тантала заставила предположить присутствие в ней какого-
то другого элемента, очень похожего на тантал, а потому трудно отделимого от него. Поэтому, когд
а в 1844 г. Г. Розе и
сследовал образ
цы колумбита, найде
нн
ые в Баварии, он вновь столкнулся с оксидами не одного, а сразу двух металлов. Поскольку считалось, что Колумбии
и
тантал — это один элемент, то Роз
е счел воз
можным дать название элемен
ту, образующему втор
ой окси
д. Подчеркивая сходство, он назвал этот второй элемент, входящий в минерал, ниобием, по имени Ниобеи,
доч
ери легендарного Та
нтала. Впрочем, как Г. Розе, так
и Ч. Хатчет не сумели получить ни
обий в сво
бодном сост
ояни
и. Металлическнй
ни
оби
й был впервые получен
ли
шь в 1866 г. шведским ученым Бломстрадом
при восстановлении хлорида ни
обия водородом.
Приключения же с названием элемен
та ниобия кончи
лись лишь в 1950 г. До этого в разных странах его называли по-разному. Если металл колумби
и (как его назвали в Амери
ке) попадал из США в Англию, то он продолжал называться колумбием.
Если металл попадал в други
е страны, то становился ниоби
ем. Конец этой разн
оголоси
це положил Международный
союз по теоретической и прикладной химии (
IUPAC).
Было решено,
узакони
ть повсюду назв
ание элемента «ниоби
й», а за основным минералом состава (
Fе,
М
n)(Nb, Та)2
О
6
закрепить название «
колумбит»
Глава III. Ниобий
Ниобий — это химический элементXX в.в прямом и переносном смысле. Хотя как элемент его открыли в самом начале XIX в. (1801 г.),
но как металл был получен лишь век спустя (1907 г.), а сейчас без него не может обойтись техника двадцатого столетия. Получение коррозионноустойчивых и сверхжаропрочных сталей, конструирование аппаратуры для атомных реакторов, ракетная и космическая техника — вот далеко не полный перечень отраслей современной Промышленности, которые не могут обходиться без этого металла.
В свободном виде ниобий в природе не встречается, а в минералах почти всегда находится с танталом. Ниобиево-танталовых минералов сейчас насчитывается более семидесяти. Основные—это колумбит-танталит (Fe, Мn) (Та, Мn)2
O6
, в нем 85% - высших оксидов ниобия и тантала; лопарит (Na, Се, Са, Sr) (Nb, Ti) O3
содержит 8—10% ниобия; (Nb, Та)2
O5
; в пирохлор (Na, Ca)2
(Nb, Ti) 2
O6
(F, ОН) входит до 65% оксида ниобия (V).
III
.1. Ниобий в свободном состоянии
Он настолько красив, что одно время пытались из него делать ювелирные изделия: своим светло-серым цветом ниобий напоминает платину. Несмотря на высокие температуры плавления (2500°С) и кипения (4840°C), из него легко можно сделать любое изделие. Металл настолько пластичен, что его можно обрабатывать на холоду. Очень важно, что ниобий сохраняет свои механические свойства при высоких температурах. Правда, как и в случае ванадия, даже небольшие примеси водорода, азота, углерода и кислорода сильно уменьшают пластичность и повышают твердость. Ниобий становится хрупким при температуре от — 100 до — 200 °С.
Получение ниобия в сверхчистом и компактном виде стало возможным с привлечением техники последних лет. Весь технологический процесс сложен и трудоемок. В принципе он делится на 4 этапа:
1) получение концентрата: феррониобия или ферротанталониобия;
2) вскрытие концентрата — перевод ниобия (и тантала) в какие-либо нерастворимые соединения, чтобы отделить от основной массы концентрата;
3) разделение ниобия и тантала и получение их индивидуальных соединений;
4) получение и рафинирование металлов.
Первые два этапа довольно просты и обычны, хотя и трудоемки. Степень разделения ниобия и тантала определяется третьим этапом. Стремление получить как можно больше ниобия и особенно тантала заставило изыскать новейшие методы разделения: избирательной экстракции, ионного обмена, ректификации соединений этих элементов с галогенами. В результате получают либо оксид, либо пятихлориды тантала и ниобия в отдельности. На последнем этапе применяют восстановление углем (сажей) в токе водорода при 1800°С, а затем температуру повышают до 1900°С и понижают давление. Получившийся при взаимодействии с углем карбид вступает в реакцию с Nb2
O5
:
2Nb2
O5
+ 5NbC = 9Nb + 5CO3
,
и появляется порошок ниобия. Если в результате отделения ниобия от тантала получен не оксид, а соль, то ее обрабатывают металлическим натрием при 1000°С и также получают порошкообразный ниобий. Поэтому при дальнейшем превращении порошка в компактный монолит проводят переплавку в дуговой печи, а для получения монокристаллов особо чистого ниобия используют электроннолучевую и зонную плавку.
III
.2. Химические свойства ниобия
Ниобий особенно ценится за его устойчивость к действию неорганических и органических веществ.
Есть разница в химическом поведении порошкообразного и кускового металла. Последний более устойчив. Металлы на него не действуют, даже если нагреть их до высоких температур. Жидкие щелочные металлы и их сплавы, висмут, свинец, ртуть, олово могут находиться в контакте с ниобием долго, не меняя его свойств. С ним ничего не могут поделать даже такие сильные окислители, как хлорная кислота, «царская водка», не говоря уж об азотной, серной, соляной и всех прочих. Растворы щелочей на ниобий тоже не действуют.
Существует, однако, три реагента, которые могут переводить металлический ниобий в химические соединения. Одним из них является расплав гидроксида какого-либо щелочного металла:
4Nb+4NaOH+5О2
= 4NaNbO3
+2H2
О
Двумя другими являются плавиковая кислота (HF) или ее смесь с азотной (HF+HNO). При этом образуются фторидные комплексы, состав которых в значительной степени зависит от условий проведения реакции. Элемент в любом случае входит в состав аниона типа [NbOF5
]2-
или [Nb(OH)2
F5
]2-
.
Если же взять порошкообразный ниобий, то он несколько более активен. Например, в расплавленном нитрате натрия он даже воспламеняется, превращаясь в оксид. Компактный ниобий начинает окисляться при нагревании выше 200°С, а порошок покрывается окисной пленкой уже при 150°С. При этом проявляется одно из чудесных свойств этого металла — он сохраняет пластичность.
В виде опилок при нагревании выше 900°С он полностью сгорает до Nb2
O5
. Энергично сгорает в токе хлора:
2Nb + 5Cl2
= 2NbCl5
При нагревании реагирует с серой. С большинством металлов он сплавляется с трудом. Исключение, пожалуй, составляют лишь два: железо, с которым образуются твердые растворы разного отношения, да алюминий, имеющий с ниобием соединение Al2
Nb.
Какие же качества ниобия помогают ему сопротивляться действию сильнейших кислот—окислителей? Оказывается, это относится не к свойствам металла, а к особенностям его оксидов. При соприкосновении с окислителями на поверхности металла возникает тончайший (поэтому он и незаметен), но очень плотный слой оксидов. Этот слой встает неодолимой преградой на пути окислителя к чистой металлической поверхности. Проникнуть сквозь него могут только некоторые химические реагенты, в частности анион фтора. Следовательно, по существу металл окисляется, но практически результатов окисления незаметно из-за присутствия тонкой защитной пленки. Пассивность по отношению к разбавленной серной кислоте используют для создания выпрямителя переменного тока. Устроен он просто: платиновая и ниобиевая пластинки погружены в 0,05 м. раствор серной кислоты. Ниобий в пассивированном состоянии может проводить ток, если является отрицательным электродом — катодом, т. е. электроны могут проходить сквозь слой оксидов только со стороны металла. Из раствора путь электронам закрыт. Поэтому, когда через такой прибор пропускают переменный ток, то проходит только одна фаза, для которой платина — анод, а ниобий — катод.
III.3. Оксиды ниобия, кислоты и их соли
Число соединений с кислородом у ниобия невелико, значительно меньше, чем у ванадия. Объясняется это тем, что в соединениях, соответствующих степени окисления +4, +3 и +2, ниобий крайне неустойчив. Если атом этого элемента начал отдавать электроны, то он стремится отдавать все пять, чтобы обнажить стабильную электронную конфигурацию.
Если сравнивать ионы одной и той же степени окисления двух соседей по группе — ванадия и ниобия, то обнаруживается усиление свойств в сторону металлов. Кислотный характер оксида Nb2
O5
заметно слабее, чем у оксида ванадия (V). Кислоту при растворении он не образует. Лишь при сплавлении со щелочами или карбонатами проявляются его кислотные свойства:
Nb2
O5
+ 3Nа2
СО3
= 2Nа3
NbO4
+ ЗС02
Эта соль - ортониобат натрия - похожа на такие же соли ортофосфорной и ортованадиевой кислот. Однако у фосфора и мышьяка ортоформа самая устойчивая, а попытка получить ортониобат в чистом виде не удается. При обработке сплава водой выделяется не соль Nа3
NbO4
, а метаниобат NaNbO3
. Это бесцветный труднорастворимый в холодной воде мелкокристаллический порошок. Следовательно, у ниобия в высшей степени окисления более устойчива не орто- , а мета-форма соединений.
Из других соединений оксида ниобия (V) с основными оксидами известны диниобаты K4
Nb2
O7
, напоминающие о пирокислотах, и полиниобаты (как тень полифосфорных и поливанадиевых кислот) с примерными формулами K7
Nb5
O16
.
nH2
O и K8
Nb6
O19
.
mH2
O. Упомянутые соли, отвечающие высшему оксиду ниобия, содержат этот элемент в составе аниона. Форма этих солей позволяет считать их производными ниобиевых. кислот. В чистом виде эти кислоты получить нельзя, так как их скорее можно рассматривать как оксиды, имеющие связь с молекулами воды. Например, мета-форма —
это Nb2
O5
.
H2
O, а орго-форма Nb2
O5
.
3H2
O. Наряду с такого рода соединениями у ниобия есть и другие, где он уже входит в состав катиона. Ниобий не образует простых солей типа сульфатов, нитратов и т. д. При взаимодействии с гидросульфатом натрия NaHSО4
или с оксидом азота N2
О4
появляются вещества со сложным катионом: Nb2
О2
(SО4
)3
. Катионы в этих солях напоминают катион ванадия с той лишь разницей, что здесь ион пятизарядный, а у ванадия степень окисления в ионе ванадила равна четырем. Такой же катион NbO3+
входит, в состав некоторых комплексных солей. Оксид Nb2
O5
довольно легко растворяется в водной фтористоводородной кислоте. Из таких растворов можно выделить комплексную соль K2
[NbOF6
].
H2
O.
На основании рассмотренных реакций можно сделать вывод, что ниобий в своей высшей степени окисления может входить как в состав анионов, так и в состав катиона. Это значит, что пятивалентный ниобий амфотерен, но все же со значительным преобладанием кислотных свойств.
Существует несколько способов получения Nb2
O5
. Во-первых, взаимодействие ниобия с кислородом при нагревании. Во-вторых, прокаливание на воздухе солей ниобия: сульфида, нитрида или карбида. В-третьих — наиболее обычный метод — обезвоживание гидратов. Из водных растворов солей концентрированными кислотами осаждается гидратированный оксид Nb2
O5
.
xH2
O. Затем при разбавлении растворов происходит выпадение белого осадка оксида. Обезвоживание осадка Nb2
O5
.
xH2
O сопровождается выделением теплоты. Вся масса накаляется. Происходит это из-за превращения аморфного оксида в кристаллическую форму. Оксид ниобия может быть двух цветов. В обычных условиях белый, но при нагревании приобретает желтую окраску. Стоит, однако, охладить оксид, как цвет исчезает. Оксид тугоплавок (tпл
=1460°С) и нелетуч.
Более низким степеням окисления ниобия соответствуют NbО2
и NbО. Первый из этих двух представляет собой черный с голубым отливом порошок. Получают NbO2
из Nb2
O5
, отбирая кислород магнием или водородом при температуре около тысячи градусов:
Nb2
O5
+ Н2
= 2NbО2
+ Н2
О
На воздухе это соединение легко переходит обратно в высший оксид Nb2
O5
. Характер его довольно скрытный, так как оксид нерастворим ни в воде, ни в кислотах. Все же ему приписывают кислотный характер на основании взаимодействия с горячей водной щелочью; при этом, однако, идет окисление до пятизарядного иона.
Казалось бы, разница в один электрон не так уж велика, но в отличие от Nb2
O5
, оксид NbO2
проводит электрический ток. Очевидно, в этом соединении существует связь металл - металл. Если воспользоваться этим качеством, то при нагревании сильным переменным током можно заставить NbO2
отдать свой кислород.
При потере кислорода NbO2
переходит в оксид NbO, в дальнейшем довольно быстро отщепляется и весь кислород. О низшем оксиде ниобия NbО известно немного. Он имеет металлический блеск и по виду схож с металлом. Прекрасно проводит электрический ток. Словом, ведет себя так, будто кислорода в его составе вовсе и нет. Даже, подобно типичному металлу, бурно реагирует с хлором при нагревании и превращается в оксихлорид:
2NbO + 3Cl2
=2NbOCl3
Из соляной кислоты вытесняет водород (будто и не оксид он вовсе, а металл вроде цинка):
2NbO + 6HCl = 2NbOCl3
+ 3H2
Получить в чистом виде NbО можно прокаливанием уже упоминавшейся комплексной соли K2
[NbOF5
] с металлическим натрием:
К2
[NbOF5
] + 3Na = NbO + 2KF + 3NaF
Оксид NbO имеет самую высокую из всех ниобиевых оксидов температуру плавления 1935°
С.
Чтобы очистить ниобий от кислорода, температуру повышают до 2300 — 2350°
С,
тогда одновременно с испарением происходит распад NbO на кислород и металл. Происходит рафинирование (очистка) металла.
III
.4. Соединения ниобия
Рассказ об элементе был бы не полным без упоминания о его соединениях с галогенами, карбидами и нитридами. Это важно по двум причинам. Во-первых, благодаря фторидным комплексам удается отделить ниобий от его вечного спутника тантала. Во-вторых, эти соединения приоткрывают нам качества ниобия как металла.
Взаимодействие галогенов с металлическим ниобием:
2Nb + 5Cl2
= 2NbCl5
могут быть получены, все возможные пентагалогениды ниобия.
Пентафторид NbF5
(tпл
= 76 °С) в жидком состоянии и в парах бесцветен. Подобно пятифтористому ванадию, в жидком состоянии он полимерен. Атомы ниобия соединены друг с другом через атомы фтора. В твердом виде имеет структуру, состоящую из четырех молекул (рис. 2).
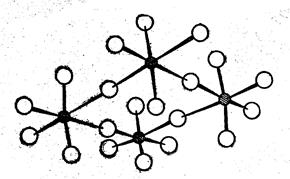
Рис. 2. Структура
NbF
5
и
TaF
5
в твердом виде состоит из четырех молекул.
Растворы в фтористоводбродной кислоте H2
F2
содержат различные комплексные ионы:
NbF5
+ H2
F2
= Н2
[NbF7
] ;
NbF5
+ H2
O = H2
[NbOF5
]
Калиевая соль K2
[NbOF5
] .
H2
O важна для отделения ниобия от тантала, так как в отличие от соли тантала она хорошо растворима.
Остальные пентагалогениды ниобия ярко окрашены: NbCl5
желтый, NbBr5
пурпурно-красный, NbI2
коричневый. Все они возгоняются без разложения в атмосфере соответствующего галогена; в паре они мономеры. Температуры их плавления и кипения возрастают при переходе от хлора к брому и иоду. Некоторые из способов получения пентагалогенидов таковы:
2Nb+5I2
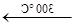 2NbI5
; 2NbI5
;
Nb2
O5
+5C+5Cl2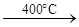 2NbCl5
+5CO;.
2NbCl5
+5CO;.
2NbCl5
+5F2
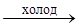 2NbF5
+5Cl2
2NbF5
+5Cl2
Пентагалогениды хорошо растворяются в органических растворителях: эфире, хлороформе, спирте. Водой, однако, полностью разлагаются -гидролизуются. В результате гидролиза получаются две кислоты -галогеноводородная и ниобиевая. Например,
NbCl5
+ 4H2
О = 5HCl + H3
NbО4
Когда гидролиз нежелателен, то вводят какую-либо сильную кислоту и равновесие написанного выше процесса смещается в сторону NbCl5
. В таком случае пентагалогенид растворяется, не подвергаясь гидролизу,
Особую признательность у металлургов заслужил карбид ниобия. В любой стали, есть углерод; ниобий, связывая его в карбид, повышает качества легированной стали. Обычно при сварке нержавеющей стали, шов имеет меньшую прочность. Введение ниобия в количестве 200 г на тонну помогает исправить этот недостаток. При нагревании ниобий раньше всех других металлов стали образует соединение с углеродом - карбид. Это соединение достаточно пластичное и в то же время способно выдерживать температуру до 3500°
С.
Слоя карбида толщиной всего в полмиллиметра достаточно, чтобы оградить от коррозии металлы и, что особенно ценно, графит. Карбид может получаться при нагревании металла или оксид ниобия (V) с углеродом или углеродсодержащими газами (СН4
, СО).
Нитрид ниобия - соединение, на которое не действуют никакие кислоты и даже «царская водка» при кипячении; устойчив по отношению к воде. Единственное, с чем его можно заставить вступить во взаимодействие, - кипящая щелочь. В этом случае он разлагается с выделением аммиака.
Нитрид NbN светло-серый с желтоватым оттенком. Он тугоплавок (тем. пл. 2300°С), имеет замечательную особенность — при температуре, близкой к абсолютному нулю (15,6 К, или -267,4 °С), обладает сверхпроводимостью.
Из соединений, содержащих ниобий в более низкой степени окисления, более всего известны галогениды. Все низшие галогениды - твердые кристаллические вещества темного цвета (от темно-красного до черного). Устойчивость их уменьшается по мере понижения степени окисления металла.
Глава IV. Тантал
В честь древнего героя Тантала назван металл, значение которого в наши дни неизменно растет. С каждым годом расширяется круг его применений, а вместе с этим и потребность в нем. Однако руды его редки и содержание в них тантала невысокое.
Одним из сырьевых источников тантала являются шлаки оловянных концентратов. Промышленность поистине испытывает «танталовы муки» по поводу нехватки тантала.
IV.1. Тантал в свободном состоянии
Синеватый металл серого цвета, с исключительно прочной связью между атомами, что обусловливает большие значения его температур плавления (3000°С) и кипения (5300°С), Легко обрабатывается на холоду давлением. Механические свойства тантала лучше, чем у ниобия. Как при высоких, так и при низких температуpax он бывает пластичен и не становится хрупким даже при температуре жидкого азота ( -196°С). Если содержит примеси азота, водорода, кислорода и углерода,тосвойства резко ухудшаются. Поэтому получение его в возможно чистом виде - основная задача при переработке танталового сырья. Даже если его значительно меньше, чем ниобия, и содержание составляет 0,01%, все равно это сырье представляет промышленную ценность. Кропотливой обработкой: обогащением, рудоразборкой, гравитационными методами с последующей флотацией, электромагнитной, электростатической или радиометрической сепарацией - создают танталовые концентраты. Они содержат до 60% (и даже больше) оксидов тантала и ниобия. Дальнейшая обработка происходит, как уже описано в разделе о ниобии. Конечными продуктами разделения обычно являются: оксид тантала Ta2
O5
, фторотанталат калия K2
TaF7
или пентахлорид TaCl5
.
Существо проблемы получения металлического тантала связано с двумя его свойствами, которые, казалось бы, противоречат друг другу: он тугоплавок, но при небольшом нагревании легко вступает в реакцию окисления. Это преодолевают, применяя электрохимическое восстановление, а также восстановлением натрием или углем. Полученный в виде порошка или брикетов металлический тантал подвергают дальше спеканию с одновременным рафинированием в вакууме (рис. 39). В последние годы, так же как и для выплавки ниобия, все шире применяется дуговая или электронно-лучевая плавка, при этом происходит особенно сильная очистка металлов. Несмотря на трудность обработки и получения, сейчас за рубежом в год выпускают примерно 300 — 400 т чистого металла.
 Тантал более редкий и дорогой металл, чем ниобий: применение этого элемента отчасти сдерживается высокой его ценой. Потребность в тантале особенно велика в новейших отраслях производства. Атомная техника: самые ответственные части ядерных реакторов делаются из металлического тантала. Он может выдерживать большие температуры, не вступая во взаимодействие с теплоносителями и металлическим топливом. Металлургия: в состав сверхтвердых сплавов на ряду с карбидами вольфрама и титана входит карбид тантала ТаС (tпл
= 3800°С). Химическая промышленность: используется высокая коррозийная устойчивость тантала, не снижающаяся при нагревании. Тантал более редкий и дорогой металл, чем ниобий: применение этого элемента отчасти сдерживается высокой его ценой. Потребность в тантале особенно велика в новейших отраслях производства. Атомная техника: самые ответственные части ядерных реакторов делаются из металлического тантала. Он может выдерживать большие температуры, не вступая во взаимодействие с теплоносителями и металлическим топливом. Металлургия: в состав сверхтвердых сплавов на ряду с карбидами вольфрама и титана входит карбид тантала ТаС (tпл
= 3800°С). Химическая промышленность: используется высокая коррозийная устойчивость тантала, не снижающаяся при нагревании.
Рис. 3. Методы получения металлов,
Непрерывная плавка (а):
А - расплав,
Б - вращающаяся затравка,
В-медные трубки охлаждения.
Восстановление водородом (б)
:
1- кварцевая ила металлическая труба,
2 - держатели или кольцевые нагреватели,
3 - лодочка или емкость для образца,
4 - образцы,
5 - рычаг управления движением образцов.
Перечень хороших качеств металлического тантала (твердость, ковкость на холоду, пластичность, устойчивость к химическим воздействиям) следует дополнить особым свойством.. В отличие от других металлов тантал совершенно не раздражает соприкасающуюся с ним живую ткань. Тонкие пластиной и проволока из тантала — ценнейший материал костной и пластической хирургии. Танталовые заплаты на черепе, скрепление костей и даже сшивание нервов стали возможны благодаря такому удивительному свойству этого металла.
IV
.2. Химические свойства тантала
Различие свойств тантала в виде кусков и порошкообразного так велико, что кажется, будто это два разных металла. Порошок при нагревании довольно энергично взаимодействует с кислородом (280°С):
4Та+5О2
= 2Та2
О5
,
с галогенами (250 — 300°С):
2Ta + 5Cl2
= 2TaCl5
,
с серой
Ta + 2S = TaS2
и даже с азотом (при накаливании до 600о
С в токе азота):
2Ta +N2
= 2TaN
Металлический тантал же устойчив в подавляющем большинстве агрессивных сред. На него не действуют никакие кислоты и даже «царская водка». Исключение составляет лишь плавиковая кислота H2
F2
, но это из-за присутствия в ней иона фтора. Очень слабо действуют на него даже расплавы щелочей.
Секрет устойчивости металлического тантала состоит в том, что на его поверхности всегда имеется тонкая, но прочнейшая пленка оксида Ta2
O5
. Если вещество или соединение может вступать во взаимодействие с этой пленкой или проникать сквозь нее, то оно будет разрушать металл, а если нет, то тантал будет сохранять свою «неприступность». К реагентам, обладающим разрушительной способностью, относятся: ионы фтора, оксид серы (VI) да еще расплавы щелочей. Эта же пленка препятствует протеканию электрического тока от металла в раствор при электролизе (когда танталовый электрод служит анодом). Поэтому тантал используется в электронной технике для изготовления выпрямителей тока.
В отсутствие кислорода и азота тантал устойчив ко многим жидким металлам. Обескислороженный металлический натрий не действует на него даже при 1200°С, магний и сплавы — уран-магний и плутоний-магний — при 1150°С. Это позволяет использовать тантал для изготовления некоторых деталей ядерных реакторов.
Тантал способен поглощать довольно значительные количества (до 1%) водорода, кислорода и азота. Происходит процесс, который называется абсорбцией, — явление поглощения какого-либо вещества всем объемом поглотителя без образования прочных соединений. Подобный процесс обратим. Поглощенный водород при нагревании металла в вакууме при 600°С весь выделяется. Металл, которому водород придал хрупкость, восстанавливает свои прежние механические качества. Свойством тантала растворять газы пользуются, когда вводят его в качестве добавки в сталь.
При. повышенной температуре происходит образование соединений. При 500°С могут существовать гидриды Та2
Н или ТаН в зависимости от содержания водорода в металле. Выше 600 — 700°С при взаимодействии с кислородом возникает оксид Та2
О5
, примерно при такой же температуре идет реакция с азотом — появляется нитрид тантала TaN. Углерод при высокой температуре (1200—1400°С) соединяется с танталом, давая ТаС — тугоплавкий и твердый карбид.
В расплавленных щелочах тантал окисляется с образованием солей танталовой кислоты, которые скорее можно считать смешанными оксидами 4Na2
O.
3Та2
О5
.
25Н2
О; 4К2
О.
3Та2
О5
.
16Н2
О. В плавиковой кислоте тантал растворяется с образованием фторидных комплексов типа [ТаF6
]-
, [TaF7
]2-
, [TaF8
]3-
. Так как комплексы неустойчивы и гидролизуются, то в растворе находятся комплексы - продукты гидролиза [ТаОF5
]2-
, [TaOF6
]3-
.
IV
.3. Химия танталовых соединений
Соединения тантала повторяют довольно близко свойства таких же образований ниобия. В основном известны соединения, где тантал имеет степень окисления +5. Однако при действии восстановителей могут возникать вещества с более низкими степенями окисления этого элемента. Наиболее хорошо изучены оксид Ta2
O5
и пятигалогениды TaF5
и TaCl5
, так как именно из них получают металл в свободном состоянии:
3Та2
О5
+ 10А1 = 5А12
О3
+ 6Та;
2TaCl5
= Ta + 5Cl2
;
K2
TaF7
+5Na = Ta + 5NaF + 2KF
Оксид тантала (V) —белый порошок, нерастворимый ни в воде, ни в кислотах (кроме H2
F2
). Очень тугоплавкий (tпл
= 1875°С). Кислотный характер оксида выражен довольно слабо и в основном проявляется при реакции с расплавами щелочей:
Та2
О5
+ 2NаОН = 2NаТаО3
+ Н2
О
или карбонатов:
Та2
О5
+ 3Nа2
СО3
= 2Nа3
ТаО4
+ 3СО2
В основном оксид тантала (V) повторяет свойства аналогичного соединения ниобия. Поэтому я покажу их отличия друг от друга. Отличие первое— температура плавления оксида тантала (V) на 400°С выше, чем у оксида ниобия (V). Отличие второе - Ta2
O5
(плотность 8,71 г/см3
) почти в два раза тяжелее Nb2
O5
(4,55 г/см3
). Такое большое различие позволяет ориентировочно оценить состав смеси по ее плотности. Отличие третье — сплавление с карбонатом натрия в случае оксида тантала происходит труднее. Отличие четвертое — соли «танталовой кислоты» и щелочных металлов гидролизуются сильнее ниобатов. Уже при значении рН=6 (т. е. при концентрации ионов водорода 10~6
моль/л) происходит выделение студенистого осадка так называемой «танталовой кислоты». Однако она даже свежеприготовленная не растворяется ни в соляной, ни в азотной кислотах и в этом не похожа на ниобиевую. Пятое отличие — гель оксида тантала (V) легче, чем гель оксида ниобия (V), отщепляет воду. После удаления всей воды масса накаляется из-за мгновенной кристаллизации.
Соли, содержащие тантал в состоянии окисления -4, -5, могут быть нескольких видов: метатанталаты NaTaO3
, ортотанталаты Nа3
ТаО4
, но существуют полиионы пента-и гекса-, кристаллизующиеся вместе с молекулами воды, [Ta5
O16
]7-
и [Ta6
O19
]8-
. Эти формы позволяют проводить аналогию не только с ниобием, но и с элементами главкой подгруппы—фосфором и мышьяком. С ниобием аналогия более полная, так как пятизарядный тантал образует при реакциях с кислотами катион ТаО3+
и соли ТаО(NО3
)3
или Nb2
О5
(SO4
)3
, продолжая «традицию» побочной подгруппы, введенную ионом ванадия VO2+
.
При 1000°С Ta2
O5
взаимодействует с хлором и хлороводородом:
Та2
O5
+ 10НС1==2ТаС15
+5Н2
О
Следовательно, можно утверждать, что и для оксида тантала (V) характерна амфотерность с превосходством кислотных свойств над свойствами основания.
В технике Та2
O5
получают из двойного фторидя 2KF.
TaF5
разложением его разбавленной серной кислотой:
2K2
TaF7
+ 2H2
SO4
+ 5H2
O = Ta2
O5
+ 2K2
SO4
+ 14HF
Полученная таким способом студенеобразная масса загрязнена адсорбируемыми из раствора веществами. В чистом виде оксид получают прокаливанием металла в токе кислорода или окислением соединений, например карбидов:
4ТаС+9О2
= 2Та2
О5
+4СО2
Чистый Ta2
O5
не изменяется при прокаливании на воздухе, в атмосфере сероводорода и парах серы. Соединения почти все производятся от оксида тантала (V). Известны соединения и меньшей степени окисления, но они менее стабильны. При высокой температуре в смеси с углем оксид тантала (V) превращается вТаО2
:
2Та2
O5
+ С = 4ТаО2
+ СO2
Гидроксид, соответствующий оксиду тантала (V), получается нейтрализацией кислых растворов четырехлористого тантала. Эта реакция, также, подтверждает неустойчивость степени окисления +4.
При низких степенях окисления наиболее стабильные соединения -галогениды (см. рис. 3), Проще всего их получить через пиридиновые комплексы. Пентагалогениды TaX5
(где Х- это С1, Вг, I) легко восстанавливаются пиридином (обозначается Ру) с образованием комплексов состава МХ4
(Ру)2
.
Затем небольшим нагреванием до 200°
С можно разрушить пиридиновый комплекс;
TaI4
(Py)2
=TaI4
+2Py
Тетрагалогениды представляют собой твердые кристаллические вещества с темной окраской от темно-оранжевой до черно-коричневой.
Взаимодействием тантала с серой при высоких температурах может быть подучен сульфид;
Ta + S2
= TaS2
Он не очень стоек и горячей водой разлагается с выделением сероводорода и водорода. В растворе выпадает студенистый осадок Та2
О5
.
xН2
О.
Чем ниже степень окисления, тем менее устойчивы соединения. Хлориды ТаС13
(черно-зеленый) и ТаСl2
(оливковый) еще могут существовать при обычной температуре, а бромиды и иодиды нестойки и трудны для исследования.
Из других соединений интересны нитрид и карбид тантала.По существу их несколько. Известны низшие нитрид Ta2
N и карбид Ta2
C и высшие TaN и ТаС. Нитриды тугоплавки, серого цвета с голубоватым отливом; при температуре, близкой к абсолютному нулю, переходят в сверхпроводящее состояние. Нитриды более стойки, чем тантал, к действию кислорода. Получаются нагреванием тантала или Ta2
O5
до 1000 - 1500°
С в атмосфере азота и водорода. Высокая температура плавления (около 3000°С) привлекает к ним внимание.Их используют как тугоплавкое покрытие для различных технических изделий.
Карбиды тантала исключительно высоко ценятся металлургами. Высший карбид ТаС имеет золотистый цвет и необычайно высокую температуру кипения 3800 °С (тем пл. 3500 °С). Это близко к температуре на поверхности Солнца. Введение карбидов в сплав повышает его прочность, жаростойкость и уменьшает хрупкость. Сами карбиды применяются в производствах, связанных с действием высоких температур, в качестве нагревателей, деталей печей, анодов и т. п.
IV.4. Применение тантала и ниобия
Рассматривая характер элемента и тех веществ, которые он образует, я уже обращала внимание на особенности, представляющие ценность для практического использования. Тантал, как и ниобий, применяется преимущественно в электровакуумной технике и химической промышленности. Однако все чаще и чаще мелькают в печати сообщения об использовании тантала наряду с ниобием в самолето- и ракетостроении, а вместе с тем, вероятно, и в космической технике.
Оба элемента обладают ценным сочетанием качеств. Способность поглощать газы хороша для поддерживания высокого вакуума: химическая инертность позволяет использовать их в высокоагрессивных средах, вплоть до атомных реакторов, и применять в медицине при костной и пластической хирургии. Металлы нисколько не вредят деятельности живых тканей организма. Настоящий переворот вызвало применение тантала, ниобия и их соединений в металлургии. Появилась возможность резко расширить ассоримент различных сталей и сплавов. Причем не только ниобий и тантал меняют характер сплавов, но и, наоборот, добавка к этим элементам других металлов придает им иные качества. Алюминий, например, повышает прочность металлического ниобия и тантала. Вольфрам и молибден увеличивают их теплостойкость. С добавлением меди увеличивается способность металлов проводить электрический ток. При этом сплав почти вдвое становится прочнее и тверже, чем медь.
Из тантала изготовляют фильеры для протяжки нитей в производстве искусственных волокон. Раньше такие фильеры делали из платины и золота. Самые твердые сплавы получают из карбида тантала с никелем в качестве цементирующей добавки. Они настолько тверды, что оставляют царапины даже на алмазе, который считается эталоном твердости.
За время, прошедшее после издания этой книги в 1973 г., накопилось немало новых данных о применении ниобия и тантала. Так, по сведениям, относящимся к январю 1975 г., первое место по величине критической температуры перехода в сверхпроводящее состояние было отдано германиду ниобия Nb3
Ge. Его критическая температура составляет 23,2 К (примерно—250 °С). Другое соединение — станнид ниобия — становится сверхпроводником при немного более низкой температуре —255 °С. Чтобы полнее оценить этот факт, укажем, что большинство сверхпроводников известны лишь для температур жидкого гелия (2,172 К). Сверхпроводники из ниобиевых материалов позволяют изготавливать магнитные катушки, создающие чрезвычайно мощные магнитные поля. Магнит диаметром 16 см и высотой 11 см, где обмоткой служит лента из такого материала, способен создать поле колоссальной напряженностью. Необходимо только перевести магнит в сверхпроводящее состояние, т. е. охладить, а охлаждение до менее низкой температуры произвести, конечно, легче.
Важна роль ниобия в сварочном деле. Пока сваривали обычную сталь, никаких особых трудностей этот процесс не представлял и сложностей не создавал. Однако, когда начали сваривать конструкции из специальных сталей сложного химического состава, сварные швы стали терять многие ценные качества свариваемого металла. Ни изменения состава электродов, ни усовершенствование конструкций сварочных аппаратов, ни сварка в атмосфере инертных газов никакого эффекта не давали. Вот тут-то на помощь и пришел ниобий. Сталь, в которую как небольшая добавка введен ниобий, можно сваривать, не опасаясь за качество сварного (рис. 4) шва. Хрупкость шву придают возникающие при сварке карбиды, но способность ниобия соединяться с углеродом и препятствовать образованию карбидов других металлов, нарушающих свойства сплавов, спасли положение. Карбиды же самого ниобия, как и тантала, обладают достаточной вязкостью. Это особенно ценно при сварке котлов и газовых турбин, работающих под давлением и в агрессивной среде.,
 Ниобий и тантал способны поглотить значительные количества таких газов, как водород, кислород и азот. При комнатной температуре 1 г ниобия способен поглотить 100 см3
водорода. Но даже при сильном нагревании это свойство практически не слабеет. При 500°С ниобий еще может поглотить 75 см3
водорода, а тантал в 10 раз больше. Этим свойством пользуются для создания высокого вакуума или в электронных приборах, где необходимо сохранить точные характеристики при высоких температурах. Ниобий и тантал, нанесенные на поверхность деталей, как губка, поглощают газы, обеспечивая стабильную работу приборов. С помощью этих металлов больших успехов достигла восстановительная хирургия. В медицинскую практику вошли не только пластинки из тантала, но и нити из тантала и ниобия. Хирурги успешно используют такие нити для сшивания порванных сухожилий, кровеносных сосудов и нервов. Танталовая «пряжа» служит для возмещения мускульной силы. С ее помощью хирурги укрепляют после операции стенки брюшной полости. Ниобий и тантал способны поглотить значительные количества таких газов, как водород, кислород и азот. При комнатной температуре 1 г ниобия способен поглотить 100 см3
водорода. Но даже при сильном нагревании это свойство практически не слабеет. При 500°С ниобий еще может поглотить 75 см3
водорода, а тантал в 10 раз больше. Этим свойством пользуются для создания высокого вакуума или в электронных приборах, где необходимо сохранить точные характеристики при высоких температурах. Ниобий и тантал, нанесенные на поверхность деталей, как губка, поглощают газы, обеспечивая стабильную работу приборов. С помощью этих металлов больших успехов достигла восстановительная хирургия. В медицинскую практику вошли не только пластинки из тантала, но и нити из тантала и ниобия. Хирурги успешно используют такие нити для сшивания порванных сухожилий, кровеносных сосудов и нервов. Танталовая «пряжа» служит для возмещения мускульной силы. С ее помощью хирурги укрепляют после операции стенки брюшной полости.
Рис. 4. Конструкция хвостового оперенья самолета из жаропрочной ниобиевой стали.
Тантал имеет исключительно прочную связь между атомами. Это обусловливает его чрезвычайно высокую температуру плавления и кипения. Механические качества и химическая стойкость приближают тантал к платине. Химическая промышленность использует такое благоприятное сочетание качеств тантала. Из него готовят детали кислотостойкого оборудования химических заводов, нагревательные и охладительные устройства, имеющие контакт с агрессивной средой.
В бурно развивающейся атомной энергетике находят применение два свойства ниобия. Ниобий обладает удивительной «прозрачностью» для тепловых нейтронов, т. е. способен пропускать их через слой металла, практически с нейтронами не реагируя. Искусственная радиоактивность ниобия (получающаяся при контакте с радиоактивными материалами) невелика. Поэтому из него можно делать контейнеры для хранения радиоактивных отходов и установки по их переработке. Другим не менее ценным (для ядерного реактора) свойством ниобия является отсутствие заметного взаимодействия с ураном и другими металлами даже при температуре 1000 °С.
Расплавленные натрий и калий, применяемые в качестве теплоносителей в атомных реакторах некоторых типов, свободно могут циркулировать по ниобиевым трубам, не причиняя им никакого вреда.
Ниобий и тантал находят все больше и больше потребителей. Однако применение сдерживается трудностями их получения и, самое главное —высокой стоимостью очистки этих металлов. С удешевлением производства будет расширяться и сфера их использования.
Глава
V
. Нильсборий
Экспериментальн
о установл
ен
о ранее неизвестное явление образования хими
ческого элемента с порядковым ном
ером 105. Из
отоп э
того элемента с периодом полураспада Т1
/2
~ 2 с получен при обл
учении амери
ция ядрами не
она.
В статье «Рождение сто пятого», помещенной в га
зете «Известия» 13 ав
густа 1970 г., при
ведено следующее высказыван
ие академика Г. Н.
Флерова:
«В сообщени
и Объедин
енного института яде
рных
исследов
ани
й от 18 февраля 1970 года мы писали о синтезе
спон
танно делящегося изотопа 105-го элемента...
Наш
а лаборатория хотела бы назвать этот э
лемент в честь в
ыдающегося физ
ика XX в. Нильса
Бора. Это предложение мы уже направи
ли в Международный союз чистой
и прикладной химии»
.
Следуя прекрасной традиции, сложившейся среди ученых, сообщение о синтезе сто пятого элемента было разослано практически во все крупные лаборатории ми
ра. Работы по синтезу этого элемен
та получили международное признани
е.
Данные,
касающиеся синтеза нильсборня
105
Ns, указывают на возможность получени
я сходным путем и более тяжелых эле
ментов (например, 106) и позволяют до
вольно уверенно оцени
ть их свойства.
Пожалуй, не мен
ее ценное с точки зрения ядерной физики открытие состоит в том, что исследователями н
айден принципиально новый метод синтеза сверхтяжелых элемен
тов. Если с 1943 по 1956 г., в результате це
пных ядерных реакций при добавлении нейтронов к ядру опре
деленного вида атомов, были получены элементы по сот
ый включи
тельно, то в дальнейшем этот метод не дал
результатов. Нейтрон не успевает слиться с ядром 100-го элемен
та, потому что это ядро делится быстрее, чем прои
сх
оди
т реакция.
Новый путь основан на процессе
взаим
одействия ускоренных
ионов с ядром тяжелого элемента. Так и
были синтезированы курчатовий
и нильсборий
. Пучок ионов неона ускорялся на циклотроне и при интенснвности
~5.
1012
в 1с сталкивался с мишенью, состоящей нз
нескольких миллиграммов изотопа америци
я 243
А
m. Происходил процесс слияни
я ядер мишени с налетающей частицей:
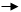  243
Am + 22
N
e 265
Ns*
265-x.n
Ns + x.
n 243
Am + 22
N
e 265
Ns*
265-x.n
Ns + x.
n
После «
испарения» нескольких нейтронов (4 и 5) из возбужденн
ого составного ядра получается атом, имеющий в ядре 105 протонов, а общую массу 261 и
ли
260. За сутки
не
прерывной работы циклотрона удается получить и обнаружить одно новое ядро. При облучении америция 243
Am ионами неона 22
Ne зарегистрирован спонта
нно делящийся излучатель с периодом полурасп
ада 1
,8 ± 0,6 с.
Очень важен вопрос о химических свойствах 104-го и 1
05-го элементов. Согласно теоретически
м представле
ни
ям, основанным на современном пони
мании периоди
ческой сис
темы, 104-й и 105-й элементы должны резко отличаться от актиноидов
и
один от другого. Они должн
ы быть хими
чес
кими
аналогами соответственн
о гафния и тантала, т. е.
исти
нными экагафнием
и экатанталом,
как назвал бы и
х Дмитрий Ив
анович Мен
делеев.
 Рис. 7, Схе
ма устан
овки для экспрессного разделе
ния и излучения
короткоживущих
радиоактивных изотоп
ов: Рис. 7, Схе
ма устан
овки для экспрессного разделе
ния и излучения
короткоживущих
радиоактивных изотоп
ов:
1—
поток газообраз
ных
носителей
(
температ
ура Э50°
С)
,
2—
мишень, н
а которую
направляется пучок ускоренных ионов,
3—поток носителя с хлори
дами
элементом
III, IV и Vгрупп,
4—ловуш
ка д
ля твердых частиц хлоридов,
5—
детекторы
определения из
отопов элемен
те
» № 104
, 105
Химической реакцией в газ
ообразной фазе удалось доказать, что 104-й элемент действительно является ана
логом гафния и проявляет валентность, равную четырем. Это первый тяжелый искусственный элемент,
не входящий в сем
ейство актиноидов.
Следовательно, элементы
105-й, 106-й и т. д.
будут находиться в V, VI и т.д. груп
пах п
ериодической системы.
Идентификация 105-
го элемента была проведена тремя принципиально различн
ыми методами. Изучены основные типы распада ядер нового элемента, а также выяснено сходство его химических свойств с танталом. В частности, устан
овлено сходство пентахлоридов
и, вероя
тно, оксихлоридов
тантала и нильсбория.
Литература :
1. Браун Т., Лемей Г.Ю., Химия в центре наук. М.: Мир. 1983.
2. Конареев Б.Н. Любознательным о химии. Неорганическая химия. М.: Химия. 1984.
3. Николаев Л.А. Нелрганическая химия. М.: Просвещение. 1982.
4. С.С. Олегин, Г.Н. Фадеев. Неорганическая химия. М.: Высшая школа. 1979.
5. Павлов Н.Н. Неорганическая химия. М.: Высшая школа. 1986.
6. Петров М.Н. Неорганическая химия. М.: Химия. 1981.
7. Популярная библиотека химических элементов – серебро, нильсборий и далее. М.: Наука. 1983.
8. Г.Н. Фадеев. Пятая вертикаль – элементы V группы переодической системы
Д.И. Менделеева. М.: Просвещение. 1985.
9. Ю.М. Шилов, М.И. Тарасенко, Ю.И. Слушкович, П.М. Чукуров. Общая химия. М.: Медицина. 1983.
|