ОТЧЁТ ПО ХИМИИ
ЛЕКЦИЯ №4
ТЕМА
:
ГЛАВНЫЕ ЭЛЕМЕНТЫ
ЖИЗНИ:
АЗОТ И ФОСФОР
Масленниковой Инны
9 «Б» класс
Общая характеристика подгруппы азота.
Подгруппу азота составляют пять элементов: азот, фосфор, сурьма, мышьяк и висмут. Это элементы V группы периодической системы Д. И. Менделеева На внешнем энергетическом уровне их элементы имеют по пять электронов – ns2
np3
. Поэтому высшая степень окисления этих элементов равна +5, низшая -3, характерна и +3.
Свойства элементов подгруппы азота
| Свойства
|
N
|
P
|
As
|
Sb
|
Bi
|
| Заряд ядра |
7 |
15 |
33 |
51 |
83 |
| Валентные электроны |
2s2
2p3
|
3s2
3p3
|
4s2
4p3
|
5s2
5p3
|
6s2
6p3
|
| Энергия ионизации атома, эВ |
14,5 |
19,5 |
9,8 |
8,6 |
7,3 |
| Относительная электроотрицательность |
3,07 |
2,1 |
2,2 |
1,87 |
1,67 |
| Степень окисления в соеденениях |
+5, +4, +3, +2, +1, -3, -2, -1 |
+5, +4, +3, +1, -3, -2 |
+5, +3, -3 |
+5, +3, -3 |
+5, +3, -3 |
| Радиус атома |
0,071 |
0,13 |
0,15 |
0,16 |
0,18 |
| Температура плавления |
-209,9 |
44,3 |
816,9 |
630,8 |
271,4 |
| Температура кипения |
-195,9 |
279,9 |
615,9 |
1634,9 |
1559,3 |
С водородом элементы подгруппы азота образуют соединения состава RH3
. Молекулы RH3
имеют пирамидальную форму. В соединениях связи с водородом более прочные, чем в соответствующих соединениях подгруппы кислорода и особенно подгруппы галогенов. Поэтому водородные соединения элементов подгруппы азота в водных растворах не образуют ионов водорода. С кислородом элементы подгруппы азота образуют оксиды общей формулы R2
O3
и R2
O5
. Оксидам соответствуют кислоты HRO2
и HRO3
(и ортокислоты H3
RO4
, кроме азота). В пределах подгруппы характер оксидов изменяется так: N2
O3
– кислотный оксид; P4
O6
– слабокислотный оксид; As2
O3
– амфотерный оксид с преобладанием кислотных свойств; Sb2
O3
- амфотерный оксид с преобладанием основных свойств; Bi2
o3
– основный оксид. Таким образом, кислотные свойства оксидов состава R2
O3
и R2
O5
уменьшаются с ростом порядкового номера элемента. В подгруппе с ростом порядкового номера неметаллические свойства убывают, а металлические усиливаются. Этим объясняется уменьшение прочности водородных соединений RH3
от NH3
к BiH3
, а также уменьшение прочности кислородных соединений в обратном порядке.
Элементы V А-подгруппы открывались в разное время, знания о них накапливались на протяжении столетий, постепенно увеличиваясь и углубляясь.
Хронология открытия химических элементов
V
А-подгруппы
| Элемент |
Дата и авторы открытия |
Город, страна |
| N |
1772г, Д. Резердорф |
Эдинбург, Шотландия |
| P |
1669г, Х. Брант |
Гамбург, Германия
|
| As |
1250г, Альберт Великий |
Больштедт, Германия |
| Sb |
Известен с древних времён |
| Bi |
Известен с XV века |
Степени окисления
N
и Р и отвечающие им соединения
| N-3
|
NH3
, Mg3
N2
, NH4
OH, NH4
Cl |
| N-2
|
N2
H4
|
| N-1
|
N2
H2
, NH2
OH |
| N0
|
N, N2
|
| N+1
|
N2
O |
| N+2
|
NO |
| N+3
|
N2
O3
, HNO2
, NaNO2
, NCl3
|
| N+4
|
NO2
, N2
O4
|
| N+5
|
N2
O5
, HNO3
, KNO3
|
| P-3
|
PH3
|
| P-2
|
P2
H4
|
| P0
|
P, P2
, P4
|
| P+3
|
PCl3
, P2
O3
, H3
PO3
|
| P+5
|
PCl5
, P2
O5
, P4
O10
, HPO3
, H3
PO4
, H4
P2
O2
, Na3
PO4
, CaHPO4
|
Азот.
Азот в природе встречается главным образом в свободном состоянии. В воздухе объёмная доля его составляет 78,09%. Соединения азота в небольших количествах содержатся в почвах. Азот входит в состав белковых веществ и многих естественных органических соединений. Общее содержание азота в земной коре 0,01%. В технике азот получают из жидкого воздуха: воздух переводят в жидкое состояние, а затем испарением отделяют азот от менее летучего кислорода (tкип
азота -195,8о
С, кислорода -183о
С). Полученный таким образом азот содержит примеси благородных газов (преимущественно аргона). Чистый азот можно получить в лабораторных условиях, разлагая при нагревании нитрит аммония:
Реклама

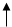 t t
NH4
OH2
=N2
+ H2
O
Атом азота имеет следующее строение:
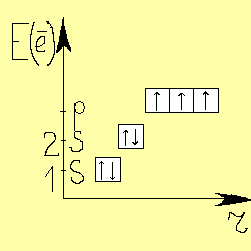
Молекула азота образована тройной ковалентной связью атомов: двумя пи-связями и одной сигма - связью. Молекула азота распадается на атомы при температуре 2000о
С. Жидкий азот хранится в сосуде Дьюра.
Физические свойства азота.
Азот – газ без цвета, вкуса и запаха, легче воздуха, растворимость в воде меньше, чем у кислорода.
Химические свойства азота.
Молекула азота состоит из двух атомов, длина между ними очень мала, Тройная связь и её малая длина делают молекулу весьма прочной. Этим объясняется малая реакционная способность азота при обычной температуре.
При комнатной температуре азот непосредственно соединяется с литием:
6Li + N2
= 2Li3
N
C другими металлами он реагирует лишь при высоких температурах, образуя нитриды:
t o
t o
3Сa + N2
= Ca3
N2
2Al + N2
= 2AlN
С водородом азот соединяется в присутствии катализатора при высоком давлении и температур
   N2
+ 3H3
2NH3 N2
+ 3H3
2NH3
При температуре электрической дуги (3000-4000о
С) азот соединяется с кислородом:
  N2 +
O2
2NO N2 +
O2
2NO
Азот образует с водородом несколько прочных соединений, из которых важнейшим является аммиак. Электронная формула молекулы аммиака такова:
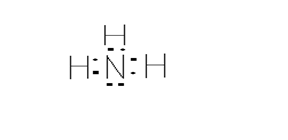
 Получение и применение аммиака.
В лабораторных условиях аммиак обычно получают слабым нагреванием смеси хлорида аммония с гашеной известью: Получение и применение аммиака.
В лабораторных условиях аммиак обычно получают слабым нагреванием смеси хлорида аммония с гашеной известью:
2NH4
Cl + Ca (OH)2
= CaCl2
+ 2NH3
+ 2H2
O
Основным промышленным способом получения аммиака является синтез его из азота и водорода. Реакция экзотермичная и обратимая:
  N2 +
3H2
2NH3
+ 92кДж N2 +
3H2
2NH3
+ 92кДж
Она протекает только в присутствии катализатора Губчатого железа с добавками активаторов - оксидов алюминия, калия, кальция, кремния (иногда и магния)
Физические свойства аммиака.
Аммиак – бесцветный газ с характерным резким запахом, почти в два раза легче воздуха. При увеличении давления или охлаждении он легко сжимается в бесцветную жидкость. Аммиак хорошо растворим в воде. Раствор аммиака в воде называется аммиачной водой или нашатырным спиртом. При кипячении растворённый аммиак улетучивается из раствора.
Реклама

Химические свойства аммиака.
Большая растворимость аммиака в воде обусловлена образованием водородных связей между их молекулами. Гидроксид – ионы обуславливают слабощелочную (их мало) реакцию аммиачной воды. При взаимодействии гидроксид - ионов с ионами NH4
+
снова образуются молекулы NH3
и H2
O, соединённые водородной связью, т. е. реакция протекает в обратном направлении. Образование ионов аммония и гидроксид – ионов в аммиачной воде можно выразить уравнением.
    NH3
+ H2
O NH3
.
H2
ONH4
+
+ OH— NH3
+ H2
O NH3
.
H2
ONH4
+
+ OH—
В аммиачной воде наибольшая часть аммиака содержится в виде молекул NH3
, равновесие смещено в сторону образования аммиака, поэтому она пахнет аммиаком. Тем не менее водный раствор аммиака по традиции обозначают формулой NH4
OH и называют гидроксидом аммония, а щелочную реакцию раствора аммиака объясняют как результат диссоциации молекул NH4
OH:
  NH4
OH NH4
+
+ OH— NH4
OH NH4
+
+ OH—
А так как в растворе аммиака в воде концентрация гидроксид – ионов невелика, то гидроксид аммония относится к слабым основаниям.
Аммиак сгорает в кислороде и в воздухе (предварительно подогретом) с образованием азота и воды:
4NH3
+ 3O2
= 2N2
+ 6H2
O
В присутствии катализатора [например, оксида хрома (III )] реакция протекает с образованием оксида азота (II) и воды:
Cr2
O3
4NH3
+ 5O2
= 4NO + 6H2
O
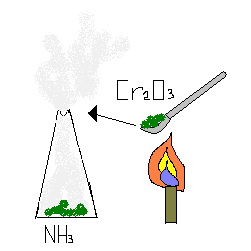
Аммиак взаимодействует с галогенами, при этом выделяется азот и водородное соединение галогена:
2NH3
+ 3Br2
= 6HBr + N2
2NH3 + 3Cl2
= 6HCl + N2
Аммиак – сильный восстановитель. При нагревании он восстанавливает оксид меди (II), а сам окисляется до свободного азота:
3Cu+2
O + 2N—3
H3
= 3Cu0
+ N2
0
+ 3H2
O
2N—3
– 6e = N2
1
Cu2+
+ 2e = Cu 3
Аммиак взаимодействует с перманганатом калия:
NH3
+ KMnO4
= N2
+ H2
O + MnO2
+KOH
Добавление аммиака изменяет цвет раствора:
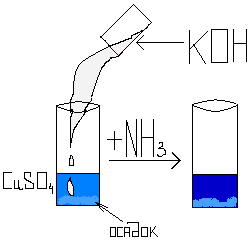
Важным химическим свойством аммиака является его взаимодействие с кислотами с образованием солей аммония
. В этом случае к молекуле аммиака присоединяется ион водорода кислоты, образуя ион аммония, входящей в состав соли:
H
  NH3
+ H+
Cl--
[H N H]Cl NH3
+ H+
Cl--
[H N H]Cl
H
Связь между ионами NH4
и Cl ионная, в ионе NH4
четыре связи ковалентные, причём три из них полярные и одна по донорно – акцепторном механизму.
Соли аммония.
Соли аммония и аниона кислоты. По строению они аналогичны соответствующим солям однозарядных ионов металлов. Соли аммония получаются пи взаимодействии аммиака или его водных растворов с кислотами. Например:
NH3
+ HNO3
= NH4
NO3
NH3
.
H2
O + HNO3
= NH4
NO3
+ H2
O
Они проявляют общие свойства солей, т.е. взаимодействуют с растворами щелочей, кислот и других солей:
(NH4
)Cl + NaOH = NaCl + H2
O + NH3
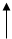 КОНЦ
. КОНЦ
.
2NH4
Cl + H2
SO4
= (NH4
)2
SO4
+ 2HCl
(NH4
)2
SO4
+ BaCl2
= 2NH4
Cl + BaSO4
Все аммонийные соли при нагревании разлагаются или возгоняются, например:
  (NH4
)2
CO3
= 2NH3
+ H2
O CO2 (NH4
)2
CO3
= 2NH3
+ H2
O CO2
 NH4
NO2
= 2H2
O + N2 NH4
NO2
= 2H2
O + N2
  NH4
Cl NH3
+ HCl NH4
Cl NH3
+ HCl
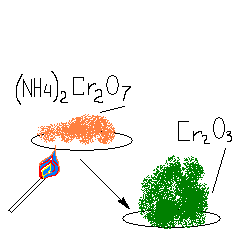
(NH4
)2
Cr2
O7
= Cr2
O3
+ 4H2
O + N2
Качественная реакция на ион аммония.
Очень важным свойством солей аммония является их взаимодействие с растворами щелочей. Этой реакцией обнаруживают соли аммония (ион аммония) по запаху выделяющегося аммиака или по появлению синего окрашивания влажной лакмусовой бумажки:
  NH4
+
+ OH H2
O + NH3 NH4
+
+ OH H2
O + NH3
Реакцию проводят так: в пробирку с испытуемой солью или раствором вводят раствор щелочи и смесь осторожно нагревают. В случае присутствия иона аммония выделятся аммиак.
Оксиды азота.
Азот образует шесть кислородных соединений, в которых проявляет степени окисления от +1 до +5: N2
+1
O, N+2
O, N2
+3
O3
, N+4
O2
, N2
+4
O4
, N2
+5
O5
. При непосредственном соединении азота с кислорода образуется только оксид азота (II) NO, другие оксиды получают косвенным путем. N2
O и NO – несолеобразующие оксиды, остальные – солеобразующие. Из всех оксидов азота наибольшее значение имеют оксиды азота (II) и азота (IV) как промежуточные продукты в производстве азотной кислоты.
Оксид азота (
II
)
NO
– бесцветный газ, плох растворимый в воде (его можно собирать в цилиндре над водой). Оксид азота (II) соединяется с кислородом воздуха, образуя бурый газ – оксид азота (IV):
2NO +O2
= 2NO2
В лабораторных условиях оксид азота (II) получают при взаимодействии разбавленной азотной кислоты и меди:
 3Cu + 8HNO3
= 3Cu(NO3
)2
+ 4H2
O + 2NO 3Cu + 8HNO3
= 3Cu(NO3
)2
+ 4H2
O + 2NO
Оксид азота (II) получают также окислением аммиака кислородом воздуха в присутствии катализатора платины. Он постоянно образуется в воздухе во время грозы под действием электрических зарядов.
 Оксид азота (
IV
)
NO
– газ бурого цвета со специфическим запахом, тяжелее воздуха, ядовит, раздражает дыхательные пути. В лабораторных условиях NO2
получают при взаимодействии концентрированной азотной кислоты и меди: Оксид азота (
IV
)
NO
– газ бурого цвета со специфическим запахом, тяжелее воздуха, ядовит, раздражает дыхательные пути. В лабораторных условиях NO2
получают при взаимодействии концентрированной азотной кислоты и меди:
Cu + 4HNO3
= Cu(NO3
)2
+ H2
O + 2NO2
  или при прокаливании кристаллического нитрата свинца: или при прокаливании кристаллического нитрата свинца:
2Pb(NO3
)2
= 2PbO + 4NO2
+ O2
При взаимодействии оксида азота (IV) с водой образуется азотная и азотистая кислоты:
2NO2
+ H2
O = HNO3
+ HNO2
HNO2
малоустойчива, особенно при нагревании. Поэтому при растворении NO2
в теплой воде образуется азотная кислота и оксид азота (II):
3NO2
+ H2
O =2HNO3
+ NO
В избытке образуется только азотная кислота:
4NO2
+ 2H2
O + O2
= 4HNO3
Оксид азота (IV) – сильный окислитель; уголь, фосфор, сера горят в нем, а оксид серы (IV) окисляется до оксида серы (VI).
Азотная кислота.
Получение азотной кислоты.
В лабораторных условиях азотная кислота получается из её солей действием концентрированной серной кислоты:
KNO3
+ H2
SO4
= HNO3
+ KHSO4
Реакция протекает при слабом нагревании (сильное нагревание разлагает HNO3
).
В промышленности азотная кислота получается каталитическим окислением аммиака, который в свою очередь, образуется как соединения водорода и азота воздуха. Весь процесс получения азотной кислоты можно разбить на три этапа:
1. Окисление аммиака на платиновом катализаторе до NO:
4NH3
+ 5O2
= 4NO +6H2
O
2. Окисление кислородом воздуха NO до NO2
:
2NO + O2
=2NO2
3. Поглощение NO2
водой в присутствии избытка кислорода:
4NO2
+ 2H2
O + O2
= 4HNO3
Физические свойства.
Азотная кислота – бесцветная жидкость с едким запахом. Она гигроскопична, «дымит» на воздухе, т. к. пары её с влагой воздуха образуют капли тумана. Смешивается с водой в любых соотношениях. Кипит при 86о
С.
Химические свойства.
В HNO3
валентность азота равна 4, степень окисления +5
Разбавленная азотная кислота проявляет все свойства кислот. Она относится к сильным кислотам. В водных растворах диссоциирует:
  HNO3
H+
+NO3
— HNO3
H+
+NO3
—
Под действием теплоты и на свету частично разлагается:
4HNO3
= 4NO2
+ 2H2
O + O2
Поэтому хранят её в прохладном месте.
Важнейшее химическое свойство азотной кислоты состоит в том, что она является сильным окислителем и взаимодействует почти со всеми металлами.
Применение.
Большие количества её расходуются на приготовление азотных удобрений, взрывчатых веществ, лекарственных веществ, красителей, пластических масс, искусственных волокон других материалов. Дымящая азотная применяется в ракетной технике в качестве окислителя ракетного топлива.
При взаимодействии азотной кислоты, с металлами водород, как правило, не выделяется: он окисляется, образуя воду. Кислота же, в зависимости от концентрации и активности металла, может восстанавливается до соединений:
+5 +4 +3 +2 +1 0 -3 -3
HNO3
---- NO2
----HNO2
---- NO ---- N2
O ----N2
---- NH3
(NH4
NO3
)
Образуется также соль азотной кислоты. От концентрации азотной кислоты зависит и продукт, образовавшийся в результате реакции:
Концентрированная азотная кислотане действует на железо, хром, алюминий, золото, платину и тантал, при взаимодействии с другими тяжелыми металлами образуется оксид азота (IV), при взаимодействии с щелочными и щелочно – земельными металлами образуется оксид азота (I).
Разбавленная азотная кислота при взаимодействии с щелочно – земельными металлами, а также с цинком и железом с образованием NH3
(NH4
NO3
). При взаимодействии с тяжелыми металлами образуется оксид азота (II).Например,
Конц.
Ag + 2HNO3
= AgNO3
+ NO2
H2
O
Разб.
3Ag + 4HNO3
= 3AgNO3
+ NO + 2H2
O
Достаточно активный металл цинк в зависимости от концентрации азотной кислоты может восстанавливать ее до оксида азота (I) N2
O, свободного азота N2
и даже до аммиака NH3
, который с избытком азотной кислоты дает нитрат аммония NH4
NO3
. В последнем случае уравнение реакции следует записать так:
4Zn + 10HNO3
(очень разб.) = 4Zn(NO3
)2
+ NH4
NO3
+ 3H2
O
Азотная кислота взаимодействует со многими неметаллами, окисляя их до соответствующих кислот:
3P + 5HNO3
+ H2
O = 3H3
PO4
+ 5NO
C + 4HNO3
= CO2
+ H2
O + 4NO2
Одноосновная кислота образует только соли, называемыенитратами. Они получаются при действии ее на металлы, их оксиды и гидроксиды. Нитратынатрия, калия, аммония и кальция называютсяселитрами: NaNO3
– натриевая селитра, KNO3
– калийная селитра, NH4
NO3
– аммиачная селитра, Ca(NO3
)2
– кальциевая селитра. Селитры используются главным образом как минеральные азотные удобрения. Кроме того, KNO3
применяется для приготовления черного пороха.
Фосфор.
Фосфор – аналог азота, т. к. электронная конфигурация валентных электронов, как и у азота, s2
p3
. Однако по сравнению с атомом азота атом фосфора характеризуется меньшей энергией ионизации и имеет больший радиус. Это означает, что неметаллические признаки у фосфора выражены слабее, чем у азота. Поэтому для фосфора реже встречаются степень окисления -3 и чаще +5. Мало характерны и другие степени окисления.
Нахождение в природе.
Общее содержание фосфора в земной коре составляет 0,08%. В природе фосфор встречается только в виде соединений; важнейшее из них – фосфат кальция – минерал апатит.
Физические свойства.
Фосфор, в отличие от азота имеет несколько аллотропных модификаций: белый, красный, черный и др.
Белый фосфор– бесцветное и очень ядовитое вещество. Получается конденсацией паров фосфора. Не растворяется в воде, но хорошо растворяется в сероуглероде. При длительном слабом нагревании белый фосфор переходит в красный.
Красный фосфор– порошок красно – бурого цвета, не ядовит, нерастворим в воде и сероуглероде, представляет смесь нескольких аллотропных модификаций, которые отличаются друг от друга цветом и некоторыми свойствами.
Черный фосфорпо внешнему виду похож на графит, жирный на ощупь, обладает полупроводниковыми свойствами. Получается длительным нагреванием белого фосфора при очень большом давлении.
Химические свойства.
В химическом отношении белый фосфор сильно отличается от красного. Так, белый фосфор легко окисляется и самовоспламеняется на воздухе, поэтому его хранят под водой. Красный фосфор не воспламеняется на воздухе, но воспламеняется при нагревании свыше 240о
С. При окислении белый фосфор светится в темноте – происходит непосредственное превращение химической энергии в световую. В жидком и растворенном состоянии, а также в парах при температуре ниже 800о
С фосфор состоит из молекул Р4
. При нагревании выше 800о
С молекулы диссоциируют:
  Р4
2Р2
. Последние при температуре выше 2000о
С распадаются на атомы: Р4
2Р2
. Последние при температуре выше 2000о
С распадаются на атомы:
  Р2
2Р. Атомы фосфора могут объединяться в молекулы Р2
, Р4
и полимерные вещества. Р2
2Р. Атомы фосфора могут объединяться в молекулы Р2
, Р4
и полимерные вещества.
Фосфор соединяется со многими простыми веществами – кислородом, галогенами, серой и некоторыми металлами, проявляя окислительные и восстановительные свойства:
2P + 3S =P2
S3
2P + 3Ca = Ca3
P2
Реакции с белым фосфором идут легче, чем с красным. Соединения фосфора сметаллами называютсяфосфидами; они легко разлагаются водой с образованием фосфина РН3
– очень ядовитого газа с чесночным запахом:
 Ca3
P2
+ 6H2
O = 3Ca(OH)2
+ 2PH3 Ca3
P2
+ 6H2
O = 3Ca(OH)2
+ 2PH3
По аналогии с NH3
фосфин способен к реакциям присоединения:
РН3
+ НI = РН4
I
Оксиды фосфора.
Оксид фосфора (III) Р2
О3
– воскообразная кристаллическая масса, плавящаяся при 22,5о
С. Получается сжиганием фосфора при недостатке кислорода. Сильный восстановитель. Не ядовит.
Оксид фосфора (V) Р2
О5
– белый гигроскопичный порошок. Получается при горении фосфора в избытке воздуха или кислорода. Он очень энергично соединяется с водой, а также отнимает воду от др. соединений. Применяется как осушитель для жидкостей и газов.
Оксиды и все кислородные соединения фосфора намного прочнее аналогичных соединений азота, что следует объяснить ослаблением неметаллических свойств у фосфора по сравнению с азотом.
Фосфорные кислоты.
Оксид фосфора (V) взаимодействуя с водой, образует кислоту НРО3
, последняя при кипячении с избытком воды образует фосфорную кислоту Н3
РО4
, при нагревании Н3
РО4
, образуется дифосфорная кислота Н4
Р2
О7
.
3Р4
О10
+ 6Н2
О = 4Н3
(РО3
)3
Н3
(РО3
)3
+ 3Н2
О = 3Н3
РО4
2Н3
РО4
= Н4
Р2
О7
+ Н2
О
Наибольшее практическое значение имеет фосфорная кислота, т. к. её соли – фосфаты – используются в качестве удобрений.
Фосфорная кислота – белое твердое вещество. С водой смешивается в любых соотношениях. В отличие от азотной кислоты не является окислителем и не разлагается при нагревании, что объясняется наибольшей устойчивостью степени окисления +5 из всех возможных для фосфора.
Азот и фосфор – это главные элементы жизни, они находятся в человеческом организме и необходимы для роста и питания каждому.
|