Механизмы возникновения огромного разнообразия клеточных типов и морфологических форм в процессе развития высших организмов всегда интересовали биологов разных специальностей. В ранних опытах прошедшего тысячелетия по пересадке тканей от одних эмбрионов другим у многоклеточных организмов было показано, что ведущую роль в регуляции развития животных играют межклеточные взаимодействия. Было сделано предположение о том, что пути развития клеток регулируются секретируемыми сигнальными молекулами, и взаимодействие эмбриональных закладок через детерминацию и дифференцировку приводит к формообразовательному эффекту. В последние два десятилетия генетики и биохимики значительно продвинулись в изучении процессов распространения информации в онтогенезе (Гилберт, 1995; Корочкин, 1999; Jonhston, Gallant, 2002).
Роль сигнальных систем в развитии организмов и их свойства
Хорошо показано, что в развивающихся эмбрионах различных представителей позвоночных и беспозвоночных животных межклеточные взаимодействия координируются набором сигнальных путей. Большую часть межклеточных сигналов передает небольшое число в разной степени изученных основных сигнальных каскадов генов, связанных с активностью определенных сигнальных молекул (лигандов, рецепторов и др.) и получивших соответствующие обозначения (Mumm, Kopan, 2000; Тарчевский, 2002; Серов, 2003; Pires-daSilva, 2003). Среди них сигнальные пути Hh (Hedgehog) (Ingham, McMahon, 2001); Wnt (wingless) (Cadigan, Nusse, 1997); Notch (Mumm, Kopan, 2000); ростовых факторов: TGF-? (Massague, Chen, 2000), EGFR (Freeman, 2002), RTK (Шемарова, 2003), JAK/STAT (Luo, Dearolf, 2001); ядерных рецепторов гормонов (Glass, Rosenfeld, 2002). Прототипы разных многокомпонентных сигнальных систем с высокой степенью гомологии молекулярных механизмов передачи сигнала можно найти уже у прокариот и низших эукариот. При переходе к многоклеточным эукариотам сигнальные белки претерпевают структурные изменения, образуют белковые комплексы; повышается эффективность сигнальной трансдукции (Шемарова, 2003; Шпаков и др., 2003).
Несмотря на разные конечные результаты детерминации и дифференцировки в онтогенезе беспозвоночных и позвоночных, наблюдается консерватизм в развертывании одного и того же сигнального каскада у разных живых организмов. В геномах разных видов гены, контролирующие развитие, эволюционно консервативны и имеют сходные функции. Например, сигнальная система Hh, в которой секретируемыми лигандами являются белки семейства Hedgehog, обнаружена у человека, мыши, курицы, лягушки, рыбы, морского ежа, пиявки и насекомых (Ingham, McMahon, 2001). Wnt-путь также широко распространен среди животных. Белки Wnt составляют одно из наибольших семейств сигнальных молекул у человека, мыши, лягушки, Caenorhabditis elegans, дрозофилы (Cadigan, Nusse, 1997; Baonza, Freeman, 2002).
Наряду с жестким консерватизмом генные сигнальные системы обладают высокой степенью гибкости в ответах на межклеточные сигналы. Каждая из них неоднократно включается в разных тканях в течение развития индивидуумов, регулируя пространственное и временное разделение экспрессии генов, определяющих различные судьбы клеток. Так, белки семейства Hh считаются участниками клеточной детерминации и дифференцировки, деления клеток, посредниками многих основных процессов эмбрионального роста и развития. У позвоночных развитие только небольшого числа морфологических отделов тела не подвержено влиянию Hh-сигнала (Ingham, McMahon, 2001). У дрозофилы Hh-белки экспрессируются в клетках заднего отдела каждого имагинального диска. Им принадлежит центральная роль в эмбриональном развитии крыла, глаза, конечностей, гонад, брюшка, кишки и трахеи (Mohler, Vani, 1992; Zhang, Kalderon, 2000; Glazer, Shilo, 2001). В то же время члены семейства белков Wnt участвуют в разных процессах развития. У дрозофилы они необходимы для организации центральной нервной системы, детерминации области крылового и глазного примордиев, ограничения размера глазной области в диске, инициации границы между глазными и прилежащими структурами головы, специализации клеток глаза и кутикулы головы (Ng et al., 1996).
Реклама

Передача сигналов может идти по короткой или длинной цепи через активацию другого каскада, быть прямой или непрямой. Примером короткого каскада может являться STAT-путь. Здесь после агрегации рецепторов факторов роста ассоциированные с ними JAK-протеинкиназы активируются путем трансфосфорилирования. Активированные JAK-киназы прямо активируют транскрипционные факторы, STAT-белки, локализованные в цитоплазме (Шемарова, 2003). В эмбриональной эктодерме дрозофилы сигнал Hh тоже передается на короткое расстояние и ограничивается воздействием на близлежащие клетки. На границе каждого сегмента эмбриона белок Нh секретируется узкой полосой клеток и выступает в роли морфогена, детерминирующего позиционную информацию в сегментах. В одной части соседних клеток поддерживается транскрипция гена wingless (wg), в другой – подавляется экспрессия гена Serrate (Ser) (Mohler, Vani, 1992; Hatini, DiNardo, 2001).
Примером разветвленного сложного пути может являться Ras/MAP-киназный каскад. Активаторами каскада являются способные к автофосфорилированию регуляторные киназы. Полифункциональный фермент МАР-киназа фосфорилирует и активирует цитоплазматические, мембранные и ядерные белки, превращая последние в факторы транскрипции (Шемарова, 2003). В имагинальном диске крыла дрозофилы позиционная детерминация возникает в результате длинноразмерного эффекта лиганда Hh. Секретируемый клетками заднего компартмента Hh распространяется через несколько клеточных рядов в передние компартменты, формируя градиент концентраций. В этом контексте Hh активирует разные гены-мишени по типу дозовой зависимости не только в близлежащих клетках. Клетки в зависимости от положения в морфогенетическом градиенте и интенсивности сигналов по-разному отвечают на присутствие Hh: они, включая разные программы дифференцировки, активируют или репрессируют разные комбинации генов и формируют разные типы клеток (Vervoort, 2000). У лягушки, рыбы, курицы и мыши белок Shh, родственный Hh, также производит действие на значительной дистанции от места его секреции. Формируя градиент концентрации в вентральной части нейтральной трубки или зачатках конечностей сквозь десятки клеточных диаметров, Shh активирует или репрессирует разные группы регуляторов транскрипции, определяет направление дифференцировки клеток или образование передне-задней полярности (Zeng et al., 2001). В развивающемся эмбрионе белки Wg также могут действовать в пределах короткой и длинной дистанции, распространяясь в разных тканях на расстояние нескольких диаметров клеток от места синтеза. Паттерн экспрессии генов в клетках, отвечающих на сигнал, зависит от концентрации Wg (Neumann, Cohen, 1997).
Реклама

Результаты сигнальной индукции существенно зависят от взаимодействия между каскадами. Разные сигнальные системы связываются между собой через боковые передающие цепочки, возникающие на многих ступенях трансдукции, активируя друг друга промежуточными продуктами. На сегодняшний день известно немало фактов взаимного влияния сигнальных путей. Так, у дрозофилы во время развития крыла взаимодействуют Hh-, Dpp- и EGFR-каскады (Crozatier et al., 2002), в специализации клеток ног участвуют RAS/MAPK- и EGFR-пути (Alamo et al., 2002), с развитием почечных канальцев связаны сигнальные системы EGFR и Wg (Sudarsan et al., 2002). Пока нет ясного понимания конкретных молекулярных механизмов этих взаимодействий. Однако возможность возникновения сети сигнальных путей может определяться некоторыми свойствами передающих сигналы белков. Так, одни и те же лиганды способны связываться с разными рецепторами и активировать альтернативные пути развития клеток. Такие неоднозначные действия могут быть следствием альтернативного сплайсинга транскриптов соответствующих генов и образования множества независимых изоформ лигандов и рецепторов с измененными внеклеточными доменами (Missler, Sudhof, 1998). В свою очередь, один и тот же рецептор в разных тканях может активировать разные внутриклеточные передатчики. В регуляции экспрессии генов-мишеней могут одновременно участвовать несколько сигнальных путей, образуя общий сигнальный белок или действуя совместно на разные модули энхансеров генов, причем одинаковые сигналы могут вызывать разные паттерны экспрессии. Активная конформация транскрипционных факторов может формироваться одновременно протеинкиназами из разных сигнальных систем. Наконец, специфичность ответа может зависеть от компартментализации сигнала на клеточной поверхности (Тарчевский, 2000; Millor, Altaba, 2002; Pires-daSilva, 2003).
Структурно-функциональные элементы сигнального пути
Общим в деятельности сигнальных каскадов, различающихся наборами генов и биохимическими механизмами, является передача сигнала от клеточной поверхности в ядро, активация соответствующих генов-мишеней через регуляцию сигнал-зависимых транскрипционных факторов. Функции сигналов выполняют молекулы лигандов – гормоны, факторы роста или морфогены, секретируемые посылающими клетками в межклеточное пространство. Специфичность проведения сигнала зависит от компетентности воспринимающих клеток, от их способности распознавать индукцию определенными рецепторами. Белковые молекулы разных рецепторов состоят из трех основных доменов: внешнего N-концевого, трансмембранного и цитоплазматического С-концевого. Рецепторы пронизывают мембраны воспринимающих клеток один или несколько раз, выступая с обеих сторон над ее поверхностью. Обычно активация сигнального пути начинается с прямого физического контакта внеклеточного домена лиганда, поступившего в межклеточный матрикс после протеолизиса, с внешним участком трансмембранного рецептора на поверхности клетки (Гилберт, 1995; Pires-daSilva, 2003). Известно, что у дрозофилы сигнальными свойствами Hh и способностью удерживаться мембраной обладает
N-концевой модифицированный холестеролом фрагмент Hh-Np белка. Рецептор для этой системы Patched (Ptc), принадлежащий к семье ростовых интегрированных с мембраной белков и имеющий стерол-чувствительный домен, кодируется геном ptc (Ingham, 2001). Рецепторы для секретируемой формы лигандов Wnt, трансмембранные белки Frizzled (Fz) у дрозофилы, C. elegans, шпорцевой лягушки, мыши и человека кодируют гены fz. Белки этого семейства с характерными богатыми цистеином внеклеточными и трансмембранными доменами консервативны в большей части своей последовательности (Cadigan, Nusse, 1997).
Взаимодействие с лигандом меняет конформацию рецепторного белка, что делает его уязвимым для многих протеолитических ферментов. Ферменты расщепляют молекулу рецептора и внутренний домен освобождается от клеточной мембраны. Активизированная внутриклеточная часть рецептора поступает в цитоплазму и включается в модификацию цитоплазматических переносчиков сигнала. Они в свою очередь активируют транскрипционные факторы, регулирующие изменение экспрессии генов-мишеней. Модификация конформации и активности рецептора и других молекул, передающих сигнал на разных ступенях каскадов, обычно происходит путем протеолизиса, димеризации, олигомеризации, фосфорилирования, дефосфорилирования или других реакций (Тарчевский, 2002; Kheradmand, Werb, 2002). Фосфорилирование по остаткам серина, треонина и тирозина – наиболее частая посттрансляционная модификация сигнальных белков. У млекопитающих изменение тирозинкиназной активности белков сигнальных каскадов факторов роста (фибробластов – FGF, тромбоцитов – PDGF, эпидермального фактора роста – EGF) играет важную роль в индукции дифференцировки, пролиферации, роста разных типов клеток. Фосфорилирование катализируется ретровирусными протеинтирозинкиназами или тирозинкиназами, часто ассоциированными с С-концевыми цитоплазматическими доменами рецепторов факторов роста (RTK). Активированная RTK фосфорилирует другие участники проведения сигнала, в том числе и транскрипционные факторы STAT и ГТФазы Ras, так называемые G-белки (Шемарова, 2003).
Рассмотрим морфогенетические свойства, генетическую структуру, ход передачи сигнала на конкретном примере Notch-передающего каскада у дрозофилы.
Участие Notch в онтогенезе дрозофилы
Механизмы передачи сигнала каскадом Notch в животном мире универсальны, ему присущи все характерные свойства сигнальных систем. Белок Notch, который служит рецептором для Notch-сигнального пути, выделен как у беспозвоночных, так и позвоночных: дрозофилы, нематоды, лягушки, рыб, грызунов, человека. Путь Notch через латеральное ингибирование или индукцию участвует фактически во всех клеточных контактах у животных и наиболее изучен у Drosophila melanogaster. Подобно другим передающим каскадам, он определяет судьбу дифференцирующихся клеток в разное время и в разных зачатках развивающегося организма (Artavanis-Tsakonas et al., 1995; Portin, 2002; Вайсман и др., 2002). В эмбрионах дрозофилы в ходе морфогенеза центральной нервной системы (ЦНС) и сенсорных щетинок сигнальный каскад Notch служит для разделения нейрального и эпидермального зачатков в нейродерме, передавая сигналы от презумптивных нервных клеток, запрещающие соседним клеткам дифференцировку в нервную ткань. У Notch-мутантов с потерей функции гена меняется структура и клеточный состав сенсорных щетинок, а также за счет уменьшения числа эпидермальных клеток увеличивается число клеток-предшественниц нервной ткани, что приводит к эмбриональной летальности (Hartenstein et al., 1996; Корочкин, Михайлов, 2000).
Деятельность пути Notch связана с локальными взаимодействиями между стереотипными клетками в процессе формирования глаза. Уменьшение активности Notch приводит к выбору дифференцирующимися клетками сетчатки не свойственного им пути развития и формированию неполноценных фоторецепторов, изменению числа и расположения составляющих элементов глаза и щетинок, гибели клеток (Cagan, Ready, 1989; Baonza, Freeman, 2001). Показано участие сигнального пути гена Notch во взаимодействиях между соседствующими клетками из дорзального и вентрального отделов крылового имагинального диска на стадии пролиферации, в формировании края крыла и ограничении числа клеток, дифференцирующихся в жилки крыла. Мутации с полной потерей функции гена приводят к полной потере ткани крыла (Diaz-Benjumea, Cohen, 1993). Notch-путь контролирует у дрозофилы развитие полярных клеток в оогенезе. Редукция функции гена у мутантов Notch вызывает нарушения, вероятно, связанные с неправильной спецификацией фолликулярных клеток и изменением их взаимодействия с развивающимся ооцитом, изменением локализации белков в ооците. Это вызывает морфологические отклонения в гермариуме и вителлариуме и снижение скорости кладки яиц (Ruohola et al., 1991; Xu et al., 1992). У дрозофилы путь Notch контролирует также развитие сегментированных придатков, ног и антенн. Локальная экспрессия Notch необходима для роста ног и образования связок между сегментами, определения границы компартментов ног. Нарушение миогенеза с увеличением числа клеток-предшественниц и кластеров миобластов у мутантов Notch свидетельствует об участии этого пути в миогенезе (Rauskolb, 2001).
Гены Notch-сигнального пути у дрозофилы
В локальных межклеточных взаимодействиях между незрелыми клетками Notch-путь контролирует ответ на специфические сигналы во время развития и определяет судьбу широкого спектра клеток в онтогенезе. На основании данных о генетических и молекулярных взаимодействиях ряд генов у Drosophila melanogaster с определенностью относят к кодирующим элементам Notch-сигнального пути: Delta (Dl, 3-66.2; 92А1-2), Serrate (Ser, 3-92.5; 97F1-F2), Notch (N, 1-3.0; 3C7), kuzbanian (kuz; 34C4-5) и Presenilin (PS; 77C1-7) – кодирующие, связанные с мембраной белки; Hairless (H, 3-69.5; 92E14-92E14), Supressor of Hairless (Su(H), 2-50.5; 35B10) и Enhancer of split (E(spl), 3-89.1; 96F11-14) – контролирующие ядерные белки (Lindsley, Zimm, 1992).
Получено немало данных о плейотропном действии, сходстве фенотипов или взаимном влиянии мутаций генов сигнального пути и нормальных и мутантных аллелей Notch. Так, ген Delta играет важную роль в процессе развития дрозофилы. У гетерозигот Drosophila melanogaster по мутации Dl возникают дефекты крыла, нарушается порядок расположения фасеток глаза, формируются дополнительные щетинки на голове, тораксе и брюшке. Гомозиготные по Dl эмбрионы гибнут в результате гиперплазии нервной системы, а в гомозиготных клонах крылового диска нарушается дифференцировка клеток. Экспрессия Dl зависит от дозы нормального аллеля Notch. Одно только увеличение дозы Notch у нормальных мух приводит к возникновению Dl-фенотипа. В свою очередь редукция активности Dl у температурочувствительных мутантов на поздней второй и ранней третьей личиночной стадиях дает фенотип крыльев, подобный фенотипу гетерозигот по нуль-аллелям N. Известны и другие примеры генетических взаимодействий между Notch и Delta (Doherty et al., 1996; Lawrence et al., 2000; Губенко, 2001).
Плейотропное проявление характерно для мутаций другого гена Notch-каскада, Serrate. В гомозиготном состоянии мутанты Ser обычно гибнут на личиночной стадии из-за серьезных морфологических дефектов ЦНС, не развитых дыхалец, резко уменьшенного в размере крылового примордия. У редко выживающих взрослых гомозиготных мух видны рудиментарные крылья и полностью редуцированные гальтеры, уменьшенные и грубые за счет снижения числа и порядка расположения омматидиев глаза. Возникновение Ser-гомозиготных клонов в имагинальном крыловом диске сопровождается появлением протяженных вырезок в разных районах крыла у взрослых мух (Speicher et al., 1994). Serrate и Notch оказывают влияние на фенотипическое проявление друг друга. Например, одна доза доминантной мутации Ser D
вызывает у взрослых мух вырезки крыльев, напоминающие фенотип notchoid (nd), рецессивного аллеля локуса Notch. У самцов генотипа nd/Y; Ser D
/+ мутантный фенотип усиливается, исчезают передний и задний края крыла и ткань дистальной части пластины крыла. Дополнительная копия аллеля дикого типа Notch нормализует фенотип у мух Ser D
(Fleming et al., 1990).
Еще один участник Notch-пути с плейотропным действием, локус Hairless, задействован в развитии центральной и периферической нервной системы, крыльев и глаз. Уменьшение функции Hairless вызывает формирование дефектных макрохет или полную их редукцию, укорочение жилок крыла, отсутствие щетинок на крыльях и между омматидиями глаз. Повышенная экспрессия Hairless у трансгенных мух вызывает образование дополнительных щетинок. Отмечено фенотипическое сходство между Hairless-мутациями с потерей функции и Notch-мутациями с повышенной функцией (Lyman et al., 1995). Supressor of Hairless получил свое название на основании генетического взаимодействия с Hairless. Фенотип, контролируемый H-аллелями, доминантно подавляется аллелями с потерей функции и усиливается дупликациями или аллелями с повышенной функцией локуса Su(H). Мутации Su(H) с повышенной функцией вызывают нарушения глаз, характерные для faсet (fa), рецессивного аллеля локуса Notch, и появление вырезок на крыльях, как у гетерозигот N ts1
/fa g2
при температуре развития 23 °С. Такие Su(H)-аллели модифицируют фенотип nd и Ax, увеличивая вырезки и укорачивая жилки на крыльях. Делеция Su(H) подавляет образование утолщений жилок крыла у самок, мутантных по Delta, и гемизиготных по deltex самцов. Усиленная функция Su(H) вызывает сильную редукцию крыла у самцов deltex (Fortiny, Artavanis-Tsakonas, 1994).
Мутации в кластере генов комплекса Enhancer of split (E(spl)), подобно Notch, вызывают гиперплазию ЦНС и затрагивают развитие периферической нервной системы, крыльев. В области мутантных клонов, дефицитных по 7 генам комплекса, на тораксе щетинки и волоски образуются с большей плотностью и часто с измененной морфологией, а на крыльях наблюдается утолщение жилок (Heitzler et al., 1996). Ген m8 из этого комплекса получил наименование E(spl) на основании его взаимодействия с мутацией split (spl), расположенной в локусе Notch. У самцов, гемизиготных по spl, в присутствии аллеля E(spl)D
с повышенной функцией сильно уменьшается число фасеток глаза и нарушается порядок их расположения. Мутации Dl подавляют взаимодействие между spl и E(spl)D
, что сопровождается реверсией к фенотипу, характерному для spl. Обнаружено взаимодействие Delta и Notch с аллелями E(spl), которые обусловлены протяженными делециями, приводящими к понижению жизнеспособности мух (Shepard et al., 1989).
Возможная принадлежность гена kuzbanian с плейотропным действием к компонентам Notch-сигнального пути установлена сравнительно недавно. Мутации kuz могут вызывать личиночно-куколочную летальность, сопровождаемую деффектами и уменьшением в размере имагинальных дисков, особенно их крыловой области. У взрослых мух kuz резко уменьшаются крылья и грудь, сливаются тарзальные сегменты ног, нарушаются паттерн и форма сенсорных органов, формируются большие грубые глаза. Ген kuz взаимодействует со многими генами Notch-пути. В гетерозиготе с мутацией kuz наблюдается усиление фенотипа мутаций N и Ser, связанных с вырезками по краю крыла. В мутантных дисках kuz не обнаруживается экспрессия гена E(spl)m8. Наоборот, суперэкспрессия E(spl)m8 нормализует фенотип в генотипе с kuz. Зависимый от температуры HS-N int
-трансген, экспрессирующий молекулу белка без внеклеточного домена, в компаунде с мутацией kuz нормализует фенотип (Rooke et al., 1996; Sotillos et al., 1997; Lieber et al., 2002). У мух, трансгенных по температурочувствительному аллелю kuz DH
, на крыльях небольшие вырезки, продольные жилки утолщены, уменьшенные и грубые глаза, дополнительные щетинки на тораксе. Дупликация по локусу Delta полностью подавляет мутантный фенотип kuz DH
.
Активно исследуемый в последние годы ген Presenilin также причисляют к участникам Notch-пути. Эмбрионы, гомозиготные по нуль-аллелю PS–
, идентичны эмбрионам генотипа Notch–
. У них нарушается дифференцировка нейроэктодермы и сенсорных щетинок крыла, и в пронейральных кластерах вместо одного нейробласта образуется их группа. Личинки гибнут из-за гиперплазии нервной системы и отсутствия дорзальной и вентральной кутикулы. Мутантные крыловые отделы имагинальных дисков уменьшены в размере, маргинальные структуры не формируются. Из химерных крыловых имагинальных дисков, несущих PS–
-клеточные клоны, развиваются крылья с вырезками и утолщенными жилками (Ye et al., 1999; Struhl, Greenwald, 2001).
Известно несколько десятков генов, взаимодействующих с Notch и другими генами Notch-сигнального пути во время развития разных органов мухи (Portin, 2002). Список генов, имеющих отношение к Notch-пути, все время расширяется. Однако сеть взаимоотношений очень сложна, и решение вопроса о принадлежности генов к Notch-пути или иной цепи передачи информации – задача не из легких. Так, только часть авторов на основании данных о генетическом взаимодействии Notch и delta и сходстве мутантных фенотипов относят к Notch-сигнальному пути ген deltex.
Данные о связывании белка Dx с анкириновыми повторами Notch позволяют считать, что этот белок конкурирует с Su(H) (Diederich et al., 1994; Matsuno et al., 2002). К кандидатам на участие в Noch-пути относят ген fringe, продукт которого взаимодействует с внеклеточным доменом рецептора Notch и изменяет его способность связываться с лигандами (Ju et al., 2000). Возможно, после накопления достаточного количества данных к этому пути будут причислены и другие гены.
Передача сигнала белками Notch-каскада
Несмотря на огромный поток экспериментальных данных, некоторая ясность достигнута в понимании лишь отдельных звеньев Notch-сигнального пути. В последнее десятилетие предприняты шаги к объединению в единую систему полученных разрозненных фактов, но предлагаемые разными авторами модели могут в чем-то не совпадать. Наиболее полно Notch-путь, суть которого состоит в проведении сигнала с поверхности клетки в ядро, изучен во время эмбрионального нейрогенеза и формирования внешних сенсорных органов мухи. Согласно популярной обобщенной схеме, последовательность событий процесса латерального ингибирования на нейрогенном сигнальном пути начинается с генерации коротких ингибирующих сигналов клетками-предшественницами нейронов (рис. 1). Сигналы поступают в межклеточное пространство в виде секретируемых молекул лигандов Delta, которые воспринимаются близлежащими окружающими клетками. На клеточной поверхности воспринимающих сигнал и экспрессирующих рецептор клеток происходит взаимодействие внеклеточного домена лиганда Delta и трансмембранного рецепторного белка Notch. Белок рецептора состоит из трех доменов: внеклеточного, связывающегося с лигандом и подавляющего активность в отсутствие лиганда, внутримембранного и внутриклеточного, способного передавать сигнал к генам-мишеням. Молекула рецептора с измененной вследствие контакта с лигандом конформацией, подвергается расщеплению протеазами Kusbanian и Presenilin и, таким образом, отделению и активации его внутриклеточной части. Внутриклеточный домен Notch транспортируется в ядро и вместе с белком Suppressor of Hairless образует транскрипционный фактор, активирующий гены-мишени Enhancer of split complex. Накопление в отвечающей на сигнал клетке репрессорных белков E(SPL) – последняя ступень каскада Notch, на которой происходит подавление дифференцировки клеток по нейральному пути (Mumm, Kopan, 2000; Portin, 2002).
Нейрогенез начинается в пронейральных кластерах вентральной нейроэктодермы и процефалической области эмбриона. Обычно только 1 из 16 клеток каждого кластера превращается в нервную, остальные приобретают эпидермальный статус. Каждая клетка пронейрального кластера эктодермы экспрессирует ген achaеte-scute и имеет потенцию развития по нейральному пути. Каждая клетка кластера также синтезирует рецептор Notch и лиганд Delta и способна ингибировать и быть ингибируемой. Физиологические флюктуации концентраций этих белков внутри клеток усиливаются по цепи обратной связи, и клетки с высокой активностью Delta окружаются клетками с высокой активностью Notch. Молекулы белка Delta образуют гомо- и гетеротипические связи на поверхности клеток и конкурентно взаимодействуют с Notch. Связывание с Delta меняет конформацию Notch, делает его субстратом для протеаз и инициирует взаимодействие с другими белками (Heitzler et al., 1996).
Благодаря высокой степени сходства, известные рецепторы Noch-каскадов у C. elegans, дрозофилы, мыши, человека объединяют в семейство LIN 12/ Notch белков. Согласно данным секвенирования, ген Notch у Drosophila melanogaster кодирует белок, состоящий примерно из 3 000 аминокислот. Этот белок включает аминотерминальный гидрофобный лидер внеклеточного домена, богатый аргинином, характерный для сигнальных пептидов других белков, ассоциирующихся с мембраной. Еще более гидрофобная последовательность внутримембранной части белка, окруженная в определенном порядке гидрофильными остатками, тоже характерна для трансмембранных доменов известных, связывающихся с мембраной белков. Иммуноцитохимические методы анализа с использованием антител к разным частям белка в большинстве клеток выявляют Notch как долгоживущий, интегрированный с мембраной белок (Kidd et al., 1983; Wharton et al., 1985).

Рис. 1. Основные элементы Notch сигнального пути (По: Mumm, Kopan, 2000).
|
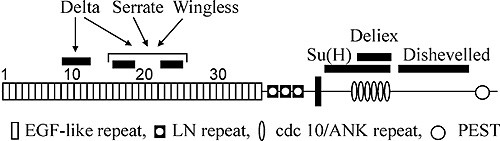
Рис. 2. Повторяющиеся мотивы в структуре Notch белка и сайтыего взаимодействия с другими белками (По: Arias, 2002).
|
Отличительная черта белка рецептора Notch – наличие трех мотивов повторяющихся последовательностей аминокислот. Два из них обнаружены во внеклеточном домене рецептора (рис. 2). Вслед за сигнальным пептидом располагается тандемный ряд повторенной 36 раз консервативной последовательности, напоминающей эпидермальный ростовой фактор млекопитающих (EGFL-повторы). Сразу за ним идет второй тандемный ряд из трех других богатых цистеином последовательностей, названных lin12/Notch-повторами. Биохимическими методами показано, что EGFL-повторы всегда располагаются на поверхности клетки, как и в других связывающихся с мембраной белках, и служат сайтами связывания с молекулами лигандов (Warton et al., 1985).
Внутриклеточная часть белка содержит 6 последовательных повторов мотива cdc10 (анкириновые повторы), который есть в последовательности цитоскелетного белка анкирина и в продукте гена cdc10 дрожжей. В районе между аминокислотами 2185 и 2300 выявлены три последовательности, напоминающие сайты связывания с фосфатами нуклеотидов у других известных белков. Далее район между 2637 и 2567 аминокислотами состоит из 30 глютаминовых остатков opa-повтора (strep-район). За ним следует С-терминальная последовательность PEST. Считается, что последовательности opa и PEST важны для регуляции стабильности белка (Warton et al., 1985).
Предполагается, что белок Notch – это димер, в котором цистеины внеклеточных EGFL-повторов образуют внутри- и межмолекулярные дисульфидные мостики, как в других подобных белках. Мутации в некоторых EGFL-повторах могут нарушать взаимодействие между полипептидными цепями Notch (Kheradmand, Werb, 2002).
В экспериментах с антителами к белку Notch показано, что он экспрессируется во время всего процесса развития в группах дифференцирующихся клеток: во время эмбриогенеза, начиная с бластулы, и далее в делящихся популяциях клеток на стадиях личинки, куколки и в половых клетках взрослой мухи. В вентральной нейрогенной области эктодермы эмбриона Notch сначала экспрессируется интенсивно и однородно, этим белком метятся предшественники нейробластов и эпидермобластов. Затем экспрессия становится дифференциальной, эпидермобласты показывают более высокий уровень содержания белка (Kidd et al., 1989; Artavanis-Tsakonas et al., 1995).
Внутриклеточная часть Notch-белка после удаления внеклеточного домена обладает нерегулируемой трансдуктивной активностью и локализуется преимущественно в ядре, в отличие от белка дикого типа, экспрессия которого наблюдается преимущественно на поверхности клеток. Экспрессия такой формы Notch в эмбрионах на стадии развития ЦНС и в имагинальных дисках во время формирования сенсорных органов, подобно мутациям с повышенной функцией, подавляет детерминацию нейробластов, и все нейроэктодермальные клетки превращаются в эпидермальные (Struhl, Adachi, 1998). Трансформанты, несущие делеции EGFL-повторов или всей внеклеточной части, по фенотипу также напоминают мутации Notch с повышенной функцией. Делеции всей внутриклеточной области Notch-белка дают фенотип, характерный для нуль-мутаций – грубые глаза, потерю микрохет на тораксе, вырезки на крыльях (Rebay et al., 1993).
Достаточно хорошо изучен трансмембранный белок лиганда Delta. Он тоже обнаруживается в разных тканях эмбриона, в том числе во всех клетках пронейральных кластеров, крыловом диске. В нем выделяют N-сигнальный терминальный участок, необходимый для транспорта через мембрану, большой внеклеточный домен с девятью повторами EGF-подобного фактора и относительно короткий внутриклеточный домен. В культуре шнейдеровских клеток (S2) методом иммунофлюоресцентного специфического к внеклеточному домену белка окрашивания показана локализация Delta на клеточной поверхности. На поверхности клеток S2 после одновременной трансфекции конструкциями, включающими оба гена, Notch и Delta, наблюдается сходство в распределении Delta и Notch. Коиммунопреципитация к белковым экстрактам из таких S2 клеток и клеток эмбрионов показывает, что Notch и Delta образуют прочный межмолекулярный комплекс. Все это верно не только в случае экспрессии в клетках полной последовательности, но и в случае экспрессии части Notch с почти полностью удаленным внутриклеточным доменом (Doherty et al., 1996). Полученные данные о структуре и клеточной локализации Notch и Delta, их взаимодействии in vitro, функциональных особенностях разных доменов белков дают основания для построения схемы взаимодействий компонентов каскада и понимания механизмов передачи сигнала с поверхности клетки в ядро.
Белок лиганда Serrate играет сходную, но комплементарную роль с Delta в крыловом диске. Они действуют как компартмент-специфические лиганды на дорзовентральной границе во время роста крыловой пластины и формирования края крыла: Serrate – в дорзальном, а Delta – в вентральном отделах связывают одни и те же EGFL-повторы Notch. Структура последовательности белка лиганда Ser обнаруживает большое сходство с Dl, имея сигнальный пептид, 14 повторов EGF-подобного фактора в ее внеклеточном районе, внутримембранный домен и совсем маленькую внутриклеточную часть. Экспрессия трансмембранного белка Ser обнаруживается в области формирования края крыла в имагинальном диске (Fleming et al., 1990). Показано, что клетки S2, экспрессирующие Ser, образуют агрегаты с клетками, экспрессирующими Notch (Speicher et al., 1994). В обобщенных для разных животных схемах пути Notch сходные по структуре и функции белки Delta и Serrate у Drosophila melanogaster и Lag2 у C. elegans объединяют в одно семейство DSL трансмембранных лигандов.
Усилиями многих исследовательских групп за последнее десятилетие показано, что под воздействием связывания с лигандами изменяется конформация белка рецептора Notch, и он становится субстратом для различных протеаз. Металлопротеазы из семейства ADAM расщепляют рецептор во внеклеточном домене, оставляя в его молекуле 11–12 аминокислот от внеклеточного домена. Внутриклеточный домен после этого остается прикрепленным к клеточной мембране. Относительно недавние данные позволяют связывать такое расщепление рецептора Notch у Drosophila melanogaster с металлопротеазой Kuzbanian (Lieber et al., 2002). Есть и другие мнения о роли в цепи передачи Notch-сигнала трансмембранного белка Kuzbanian. Одни считают вероятным его участие в протеолизисе внеклеточной части Notch-белка на стадиях созревания рецептора и продвижения его к клеточной мембране, необходимых для взаимодействия Notch-рецептора с лигандами. Образующийся после этого посредством дисульфидных мостиков димер Notch теряет внутреннюю часть EGF-повторов во внеклеточном домене (Pan, Rubin, 1997). Другие предполагают, что Kuz на поверхности секретирующих клеток участвует в процессинге Delta, свобождающем его внеклеточный домен для связывания с Notch (Qi et al., 1999). Характер генетических взаимодействий kuz и N, Ser, E(spl)m8 и H, позволил предположить, что трансмембранный Kuz участвует в цепи передачи Notch-сигнала на стадии, предшествующей Su(H). Kuz экспрессируется в эмбриональной нейроэктодерме и личиночном глазном имагинальном диске.
На следующем этапе процессинга рецептора наблюдается расщепление во внутримембранном домене белка или в непосредственной близости от мембраны. На основании полученных на сегодняшний день данных лучшим кандидатом на участие в этом внутримембранном расщеплении считается фермент Presenilin (PS). Известно, что белки PS и Notch физически ассоциируют между собой и образуют комплекс в клеточной мембране (Ray et al., 1999). Иммуноокрашивание PS–
и нормальных глазных дисков показывает, что субклеточная локализация и распределение Notch и Delta y них примерно одинаковы. В то время как уровень Notch-белка и его локализация в клеточной мембране у PS–
-эмбрионов не отличается от дикого типа, транспорт внутриклеточной части Notch в ядро зависит от генотипа по PS. Использование конструкций с сигнальными генами показало, что активированная форма Nint
, в которой делетированы внеклеточная и трансмембранная части белка, достигает ядер в отсутствие активности PS. Белок NEGF
, в котором удален только внеклеточный район, не накапливается в ядрах PS–
-эмбрионов (Ye et al., 1999; Mumm, Kopan, 2000; Struhl, Greenwald, 2001). В результате контролируемого ферментом PS протеолизиса в районе внутримембранного домена внутриклеточная часть белка Notch освобождается от мембраны и приобретает способность передвигаться и доставлять сигнал в ядро (Struhl, Adashi, 1998; Mumm, Kopan, 2000). В свою очередь, экстраклеточный домен белка Notch подвергается транс-эндоцитозу в клетках, экспрессирующих лиганд (Parks et al., 2000).
Активированный внутриклеточный домен белка рецептора Notch при участии анкириновых сdc10 повторов связывается с регуляторами транскрипции группы CSL (CBF1, Su(H), Lag-1), к которым относится Su(H) у Drosophila melanogaster. Белок Su(H) в культуре клеток S2, несущих конструкцию с полноразмерной копией Su(H), локализуется преимущественно в ядре. После одновременной трансфекции в S2 полноразмерных копий генов Su(H) и Notch белки Su(H) и Notch обнаруживаются в цитоплазме с одинаковой вариацией их относительных уровней в различных частях клетки. В случае когда трансфекция выполнена с использованием последовательности Notch-локуса, делетированной по сdc10-району, колокализация белков не наблюдается и Su(H) первоначально концентрируется в ядре. В системе трансформированных дрожжей полноразмерный белок Su(H) ассоциируется с внутриклеточным сегментом Notch, если только он содержит все 6 cdc10-повторов. В смешанной S2 культуре, когда клетки, экспрессирующие Su(H) и Notch, агрегируют с клетками, экспрессирующими Dl, цитоплазматическая локализация Su(H) и Notch меняется на ядерную
В отсутствие активности внутриклеточного домена Notch белок Su(H) в агрегате с комплексами корепрессоров выступает в роли репрессора транскрипции генов. Notch действует как антагонист этого объединения. Связываясь в цитоплазме или ядре с корепрессорами и с Su(H), Notch вызывает каскад взаимодействий Su(H) с рядом других белков и переключение Su(H) на роль активатора транскрипции (Mumm, Kopan, 2000).
В ядре Su(H) запускает гены-мишени комплекса E(spl), белки которых вместе с продуктами генов-мишеней Notch-пути у разных животных объединены в класс HES (от Hairy и E(spl)). В опытах с последовательностями Su(H) разной длины определена примерная протяженность области белка, необходимая для связывания с ДНК. Способность Su(H) распознавать сайт связывания ДНК теряется после образования белок-белкового комплекса Н-Su(H). Обнаружен участок Su(H) для прямого взаимо-действия с Н in vitro. Увеличение in vitro концентрации Н коррелирует с ослаблением связывания между Su(H) и ДНК, когда их количество не меняется (Brou et al., 1994; Barolo et al., 2002).
Белки 7 нейрогенов комплекса E(spl) содержат bHLH-мотивы, способные к образованию гомо- и гетеродимеров и к связыванию со специфическими последовательностями ДНК. Их относят к группе негативных регуляторов транскрипции. Транскрипты E(spl) экспрессируются в определенной динамике в эмбриогенезе и на личиночных и куколочных стадиях. Нейрогенные локусы комплекса транскрибируются в нейроэктодерме, в крыловом имагинальном диске в местах будущего формирования сенсорных органов, вблизи дорзовентральной границы крыла, в местах формирования жилок пластины крыла, во всей морфогенетической бороздке глазного диска, в яичниках взрослой самки (Knust et al., 1987). С потерей функции Notch или Delta нарушается нормальная аккумуляция белков E(spl)bHLH в ядрах клеток вентральной нейроэктодермы (Jennings et al., 1994).
Каскад событий Notch-сигнального пути завершается включением E(spl). В свою очередь, белки-репрессоры E(spl)bHLH предотвращают клетки в пронейральных кластерах эктодермы от развития по нейральному пути, ингибируя пронейральные гены achaete, scute, lethal of scute (Jennings et al., 1994; Heitzler et al., 1996).
Аналогично действию в нейрогенезе Notch-путь контролирует судьбу недифференцированных бипотентных клеток-предшественниц в оогенезе. Напротив, во время развития крыла и глаза Notch-путь может выполнять не ингибирующую, а индуктивную функцию (Mumm, Kopan, 2000; Portin, 2002).
Взаимодействие Notch-пути с другими генами и сигнальными каскадами (сеть сигнальных путей)
Плейотропное действие Notch предполагает его взаимодействие с другими генами, модулирующими его активность и не входящими в Notch-сигнальный путь. Данные генетических экспериментов на Drosophila melanogaster позволяют предполагать влияние генов wingless и Notch на функции друг друга. Недавние биохимические эксперименты доказали наличие прямого физического контакта между Wingless и Notch, не приводящего к расщеплению молекулы Notch. Кроме того, Notch взаимодействует с Dishevelled, участником Wg-каскада (Axelrod et al., 1996). Интересно, что внутриклеточный домен Notch может образовывать белковый комплекс не только с Su(H), но и с другими регуляторами транскрипции, такими, как ацетилазы гистонов (Klein et al., 2000).
Наблюдаемые взаимодействия между генами и их белками, возможно, отражают взаимосвязь между известными сигнальными путями, наличие сети сигнальных путей. Например, приобретение нейрального статуса предшественниками нейронов в глазном имагинальном диске происходит под контролем и при взаимодействии передающих каскадов Hh и Notch. Белок Nоtch выступает в роли регулятора негативных репрессоров транскрипционного фактора Atonal, зависящего опосредованно от Hh-пути через секретируемый белок Dpp из семейства TGFЯ (Baonza, Freeman, 2001). Дифференцировка клеток-предшественниц сенсорных макрохет мезоторакса связана с антагонистическими отношениями между EGFR- и Notch-сигнальными путями (Culi et al., 2001). Координированные взаимодействия систем, образующих сигнальную сеть, являются основой согласованной регуляции функционирования генома живых организмов. Нарушение передачи сигнала на каком-либо этапе приводит к различным патологиям, из которых у позвоночных наиболее известны такие, как болезнь Альцгеймера, заболевания различными типами рака и другие (Гилберт, 1995; Ray et al., 1999).
Список литературы
Вайсман Н.Я., Захаров И.Л., Корочкин Л.И. Ген Notch и судьба плодовой мушки Drosophila melanogaster // Успехи соврем. биологии. 2002. Т. 122, № 1. С. 95–108.
Гилберт С. Биология развития. М.: Мир, 1995. Т. 3. 352 с.
Губенко И.С. Локус Delta в Notch сигнальной системе: организация и плейотропная функция // Цитология и генетика. 2001. Т. 35, № 4. С. 59–80.
Корочкин Л.И. Введение в генетику развития. М.: Наука, 1999. 253 с.
Корочкин Л.И., Михайлов А.Т. Введение в нейрогенетику. М.: Наука, 2000. 274 с.
Серов О.Л. Генный и хромосомный уровни контроля развития // Информ. вестник ВОГиС. 2003. № 24/25. С. 2–8.
Тарчевский И.А. Сигнальные системы клеток растений. М.: Наука, 2002. 294 с.
Тарчевский И.А. Элиситор-индуцируемые сигнальные системы и их взаимодействие // Физиология растений. 2000. Т. 47, № 2. С. 321–331.
Шемарова И.В. Роль фосфорилирования по тирозину в регуляции пролиферации и клеточной дифференцировки у низших эукариот // Цитология. 2003. Т. 45, № 2. С. 196–215.
Шпаков А.О., Деркач К.В., Перцева М.Н. Гормональные сигнальные системы низших эукариот // Цитология. Т. 45 № 3. . 223–234.
Alamo D., Terriente J., Diaz-Benjumea F.J. Spitz/EGFr signalling via the Ras/MAPK pathway mediates the induction of bract cells in Drosophila legs // Development. 2002. V. 129. P. 1975–1982.
Arias A.M. New alleles of Notch drow a blueprint for multifunctionality // Trends in Genet. 2002. V. 18. P. 168–170.
Artavanis-Tsakonas S., Matsuno K., Fortiny M.E. Notch signalling // Science. 1995. V. 268. P. 225–232.
Axelrod J.D., Matsuno K., Artavanis-Tsakonas S., Perrimon N. Interection between Wingless and Notch signaling pathways mediated by Dishevelled // Science. 1996. V. 271. P. 1826–1831.
Baonza A., Freeman M. Notch signalling and the initiation of neural development in the Drosophila eye // Development. 2001. V. 128. P. 3889–3898.
Baonza A., Freeman M. Control of Drosophila eye specification by Wingless signaling // Development. 2002. V. 129. P. 5313–5322.
Barolo S., Stone T., Bang A.G., Posakony J.W. Default repression and Notch signaling: Hairless acts as an adaptor to recruit the corepressors Groucho and dCtBP to Suppressor of Hairless // Genes Dev. 2002. V. 15. P. 1964–1976.
Brou C., Logeat F., Lecourtois M., Vandekerckhove J., Kourilsky Ph., Schweisguth F., Israell A. Inhibition of the DNA-binding activity of Drosophila Supressor of Hairless and of its human homolog, KBF2/RBP-J ?, by direct protein-protein interection with Drosophila Hairless // Genes Dev. 1994. V. 8. P. 2491–2503.
Cadigan K.M., Nusse R. Wnt signaling: a common theme in animal development // Genes Dev. 1997. V. 11. P. 3286–3305.
Cagan R.L., Ready D.F. Notch is required for successive cell decisions in the developing Drosophila retina // Genes Dev. 1989. V. 3. P. 1099–1112.
Crozatier M., Glise B., Vincent A. Connecting Hh, Dpp and EGF signalling in patterning of the Drosophila wing; the pivotal role of collier/knot in the AP organiser // Development. 2002. V. 129. P. 4261–4269.
Culi J., Martin-Blanco E., Modolell J. The EGF receptor and N signalling pathways act antagonistically in Drosophila mesothorax bristle patterning // Development. 2001. V. 128. P. 299–308.
Diaz-Benjumea F.J., Cohen C.M. Interection between dorsal and ventral cells in the imaginal disc directs wing development in Drosophila // Cell. 1993. V. 75. P. 741–752.
Diederich R.J., Matsuno K., Hing H., Artavanis-Tsakonas S. Cytosolic interection between deltex and Notch ankyrin repeats implicates deltex in the signalling pathway // Development. 1994. V. 120. P. 473–481.
Doherty D., Feger G., Younger-Shepherd S., Jan L.Y., Jan Y.N. Delta is a ventral to dorsal signal complementary to Serrate, another Notch ligand, in Drosophila wing formation // Genes Dev. 1996. V. 10. P. 421–434.
Fleming R.J., Scottgale T.N., Diederich R.G., Artavanis-Tsakonas S. The gene Serrate encodes a putative EGF-like transmembrane protein essential for proper ectodermal development in Drosophila melanogaster // Genes Dev. 1990. V. 4. P. 2188–2201.
Fortiny M.E., Artavanis-Tsakonas S. The Supressor of Hairless protein participate in Notch receptor signaling // Cell. 1994. V. 79. P. 273–282.
Freeman M. A fly's eye view of EGF receptor signaling // EMBO J. 2002. V. 21. P. 6635–6642.
Glass Ch.K., Rosenfeld M.G. The coregulator exchange in transcriptional functions of nuclear receptors // Genes Dev. 2002. V. 14. P. 121–141.
Glazer L., Shilo B. Hedgehog signaling patterns the tracheal branches // Development. 2001. V. 128. P. 1599–1606.
Hartenstein V., Tepass U., Gruszynski-de Feo E. Proneural and neurogenic genes control specification and morphogenesis of stomatogastric nerve cell precursors in Drosophila // Dev. Biol. 1996. V. 173. P. 213–227.
Hatini V., DiNardo S. Divide and conquer: pattern formation in Drosophila embryonic epidermis // Trends in Genet. 2001. V. 17. P. 574–579.
Heitzler P., Bourouis M., Ruel L., Carteret C., Simpson P. Genes of the Enhancer of split and achaete-scute complexes are required for a regulatory loop between Notch and Delta during lateral signalling in Drosophila // Development. 1996. V. 122. P. 161–167.
Ingham P.W. Hedgehog signaling: a tale of two lipids // Science. 2001. V. 294. P. 1879–1881.
Ingham P.W., McMahon A.P. Hedgehog signaling in animal development: paradigms and principles // Genes Dev. 2001. V. 15. P. 3059–3087.
Jennings B., Preiss A., Delidakis C., Bray S. The Notch signalling pathway is required for Enhancer of split bHLH protein expression during neurogenesis in the Drosophila embryo // Development. 1994. V. 120. P. 3537–3548.
Jonhston L.,A., Gallant P. Control of growth and organ size in Drosophila // BioEssays. 2002. V. 24. P. 54–64.
Ju B.G., Jeong S., Bae E., Hyun S., Carroll S.B., Yim J., Kim J. Fringe forms a complex with Notch // Nature. 2000. V. 405. P. 191–195.
Kheradmand F., Werb Z. Shedding light on sheddases: role in growth and development // BioEssays. 2002. V. 24. P. 8–12.
Kidd S., Lockett T.D., Young M.W. The Notch locus of Drosophila melanogaster // Cell. 1983. V. 34. P. 421–433.
Kidd S., Baylies M.K., Gasic G.P., Young M.W. Structure and distribution of the Notch protein in development Drosophila // Genes Dev. 1989. V. 3. P. 1113–1129.
Klein T., Seugnet L., Haenlin M., Arias A.M. Two different activities of Suppressor of Hairless during wing development in Drosophila // Development. 2000. V. 127. P. 3553–3566.
Knust E., Tietze K., Campos-Ortega J.A. Molecular analysis of the neurogenic locus Enhancer of split of Drosophila melanogaster // EMBO J. 1987. V. 6. P. 4113–4123.
Lawrence N., Klein T., Brennan K., Arias A.M. Structural requirements for Notch signalling with Delta and Serrate during the development and patterning of the wing disc of Drosophila // Development. 2000. V. 127. P. 3185–3195.
Lieber T., Kidd S., Young M.W. Kuzbanian-mediated cleavage of Drosophila Notch // Genes Dev. 2002. V. 16. P. 209–211.
Lindsley D.L., Zimm G.G. The genome of Drosophila melanogaster. New York: Academic Press, 1992.
Luo H., Dearolf C.R. The JAK/STAT pathway and Drosophila development // BioEssays. 2001. V. 23. P. 1138–1147.
Lyman B., Yedvobnik B. Drosophila Notch recepter activity supresses Hairless functon during adult external sensory organ development // Genetics. 1995. V. 141. P. 1491–1505.
Massague J., Chen Y. Controlling TGF-signaling // Genes Dev. 2000. V. 14. P. 627–644.
Matsuno K., Ito M., Hori K., Miyashita F., Suzuki S., Kishi N., Artavanis-Tsakonas S., Okano H. Involvement of proline-rich motif and RING-H2 finger of Deltex in the regulation of Notch signaling // Development. 2002. V. 129. P. 1049–1059.
Millor J.L., Altaba A.R. Growth, hedgehog and the price of GAS // BioEssays. 2002. V. 24. P. 22–26.
Missler M., Sudhof T.S. Neurexins: three genes and 1001 products // TIG. 1998. V. 14. P. 20–26.
Mohler J., Vani K. Molecular organisation and embryonic expression of the hedgehog gene involved in cell-cell communication in segmental patterning in Drosophila // Development. 1992. V. 115. P. 957–971.
Mumm J.S., Kopan R. Notch Signaling: аrom the Outside In // Dev. Biol. 2000. V. 228. P. 151–165.
Neumann C., Cohen S. Morphogens and pattern formation // BioEssays. 1997. V. 19. P. 721–772.
Ng M., Diaz-Benjumea F.J., Vincent J.P., Wu J., Cohen S.M. Specification of the wing by localized expression of Wingless protein // Nature. 1996. V. 381. P. 316–318.
Pan D., Rubin G.M. Kuzbanian controls proteolytic processing of Notch and mediates lateral inhibition during Drosophila and vertebrate neurogenesis // Cell. 1997. V. 90. P. 271–280.
Parks A.L., Klueg K.M., Stout J.R., Muskavitch M.A. Ligand endocytosis drives receptor dissociation and activation in the Notch pathway // Development. 2000. V. 127. P. 1373–1385.
Pires-daSilva A., Sommer R.J. The evolution of signaling pathways in animal development // Nature Reviews, Genetics. 2003. V. 4. P. 39–49.
Portin P. General outlines of the molecular genetics of the Notch signalling pathway in Drosophila melanogaster: a review // Hereditas. 2002. V. 136. P. 89–96.
Qi H., Rand M.D., Wu X., Sestan N., Wang W., Rakic P., Xu T., Artavanis-Tsakonas S. Processing of the Notch ligand Delta by the metalloprotease Kuzbanian // Science. 1999. V. 283. P. 91–94.
Ray W.J., Yao M., Nowotny P., Mummdagger J., ZhangDagger W., WuDagger J.Y., Kopandagger R., Goate A.M. Evidence for a physical interaction between Presenilin and Notch // Proc. Natl Acad. Sci. 1999. V. 96. P. 3263–3268.
Rauskolb C. The establishment of segmentation in the Drosophila leg // Development. 2001. V. 128. P. 4511–4521.
Rebay I., Fehon R., Artavanis-Tsakonas S. Specific truncations of Drosophila Notch define dominant activated and dominant negative forms of the receptor // Cell. 1993. V. 74. P. 319–329.
Rooke J., Pan D., Xu T., Rubin G.M. Kuz a conserved metalloprotease-disintegrin protein with two roles in Drosophila neurogenesis // Science. 1996. V. 273. P. 1227–1231.
Ruohola H., Bremer K.A., Baker D., Swedlow J.R., Jan L.Y., Jan Y.N. Role of neurogenic genes in establishment of follicle cell fate and oocyte polarity during oogenesis in Drosophila // Cell. 1991. V. 66. P. 433–449.
Shepard S.B., Broverman S.A., Muskavitch M.A.T. A tripartite interection among of allele of Notch, Delta and Enhancer of split during imaginal development of Drosophilа melanogaster// Genetics. 1989. V. 122. P. 429–438.
Sotillos S., Roch F., Campuzano S. The metalloprotease-desintegrin Kusbanian perticipates in Notch activation during growth and partenning of Drosophila imaginal discs // Development. 1997. V. 124. P. 4769–4779.
Speicher S.A., Thomas U., Knust U.H., Knust E. The Serrate locus of Drosophila and its role in morphogenesis of the wing imaginal discs: control of cell proliferation // Development. 1994. V. 120. P. 535–544.
Struhl G., Adachi A. Nuclear access and action of Notch in vivo // Cell. 1998. V. 93. P. 649–660.
Struhl G., Greenwald I. Presenilin mediated transmembrane cleavage is required for Notch signal transduction in Drosophila // Proc. Natl Acad. Sci. USA. 2001. V. 98. P. 229–234.
Sudarsan V., Pasalodos-Sanchez S., Wan S., Gampel A., Skaer H. A genetic hierarchy establishes mitogenic signalling and mitotic competence in the renal tubules of Drosophila // Development. 2002. V. 129. P. 935–944.
Vervoort M. hedgehog and wing development in Drosophila: a morphogen at work? // BioEssays. 2000. V. 22. P. 460–468.
Warton K.A., Jahansen K.M., Xu T., Artavanis-Tsakonas S. Nucleotide sequence from the neurogenic locus Notch implies a gene product that shares homology with protein containing EGF-like repeats // Cell. 1985. V. 43. P. 567–581.
Xu T., Caron L.A., Fehon R.G., Artavanis-Tsakonas S. The involvement of the Notch locus in Drosophila oogenesis // Development. 1992. V. 115. P. 913–922.
Zeng X., Goetz J., Suber L., Scott W.J., Schreiner C., Robbin D. A freely diffusible form of Sonic hedgehog mediates long-range signaling // Nature. 2001. V. 411. P. 716–720.
Zhang Y., Kalderon D. Regulation of cell proliferation and patterning in Drosophila oogenesis by Hedgehog signaling // Development. 2000. V. 127. P. 2165–2176.
Ye Y., Lukinova N., Fortiny M.E. Neurogenic phenotypes and altered Notch processing in Drosophila presenilin mutants // Nature. 1999. V. 398. P. 525–529.
|