| Свойства растворов высокомолекулярных соединений. Набухание ВМС. Их растворение. Давление набухания. Степень набухания. Пластификаторы. Уравнение Хаггинса
Растворы высокомолекулярных соединений (ВМС) представляют собой лиофильные системы, термодинамически устойчивые и обратимые. Большие размеры макромолекул вносят специфику в свойства и поведение этих систем по сравнению с низкомолекулярными обычными гомогенными системами. Молекулярные коллоиды образуются путем растворения высокомолекулярных систем (ВМС) в растворителе. Высокомолекулярные системы (ВМС) обладают большой молекулярной массой порядка 104
– 10 7
1/моль. При взаимодействии высокомолекулярных систем (ВМС) с растворителем происходит увеличение объема и массы полимера во времени. Этот процесс называется набуханием, и характеризуется степенью набухания.
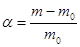 , где , где
m0
, m – массы исходной и набухшей высокомолекулярной системы (ВМС)
Набухание может быть ограниченным и неограниченным (рис. 5.1.1.1).
 В I случае a достигает постоянного предельного значения (например, желатин и вода). Во II случае значения aи массы проходят через максимум, после чего полимер растворяется (например, желатин и горячая вода). В этом случае набухание является началом растворения. Процесс набухания можно представить происходящим в две стадии: В I случае a достигает постоянного предельного значения (например, желатин и вода). Во II случае значения aи массы проходят через максимум, после чего полимер растворяется (например, желатин и горячая вода). В этом случае набухание является началом растворения. Процесс набухания можно представить происходящим в две стадии:
1. характерное выделение теплоты набухания и понижение общего объема системы.
2. тепла практически не выделяется, но происходит основное повышение объема.
Причина набухания заключается в различии свойств высокомолекулярной системы (ВМС) и растворителя. Сильное взаимодействие компонентов приводит к постепенному смещению и размыванию границы раздела фаз. Скорость этого процесса определяется подвижностью молекул, коэффициентом их диффузии. Поэтому переход макромолекул в фазу растворителя происходит медленно, тогда как молекула растворителя быстро проникает в сетку полимера, раздвигают его цепи и увеличивают объем. При этом происходит межмолекулярное взаимодействие, обусловленное главным образом сольватацией макромолекул, поэтому полимер набухает не в любом растворителе, а лишь в подходящем. Для полярных высокомолекулярных систем (ВМС) подходит полярный растворитель, для неполярных – неполярный. Набухание всегда сопровождается возникновением давления набухания, которое может достигать сотни МПа. Давление набухания эквивалентно внешнему давлению, которое нужно приложить, чтобы остановить увеличение объема набухшего вещества. Оно аналогично осмотическому давлению.
Реклама

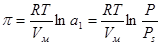 , ,
где Vм
– парциальный мольный объем растворителя.
Уравнение позволяет по давлению пара растворителя рассчитывать давление набухания. Давление набухания сильно понижается с увеличением давления пара растворителя или увеличением степени набухания.
При набухании молекулы растворителя внедряются между макромолекулами. При этом молекула полимера получает большую подвижность, т.е. гибкость и эластичность за счет снижения сил когезии. Наоборот, при уменьшении количества растворителя в межмолекулярном пространстве увеличиваются силы когезии и возрастает хрупкость систем. Иногда для придания определенных свойств высокомолекулярных систем (ВМС) в межмолекулярное пространство вводят вещества–пластификаторы, выполняющие роль растворителя.
Тема 5.1.2. Вязкость дисперсных систем и растворов ВМС.
Уравнение Бингама. Удельная, характеристическая,
относительная вязкости. Методы измерения вязкости.
Тиксотропия
Вязкость коллоидной системы зависит от концентрации дисперсной фазы, природы дисперсионной среды и дисперсной фазы, наличия стабилизатора.
Вязкость жидкости – это сопротивление передвижения одного слоя жидкости относительно другого слоя.
Если при изменении скорости течения в пределах ламинарности вязкость жидкости остается постоянной, т.е. скорость течения прямо пропорциональна приложенной силе жидкости, то жидкости называются ньютоновскими. Если условие не выполняется, значит, жидкости называются неньютоновскими. Чистые жидкости и разбавленные растворы коллоидов со сферическими частицами характеризуется как ньютоновские жидкости, тогда как растворы коллоидов с палочкообразными или нитевидными частицами обладают не ньютоновской вязкостью. Все коллоидные растворы имеют вязкость, превышающую вязкость дисперсионной среды. Для коллоидных систем, двигающихся ламинарно и имеющих дисперсную фазу в виде шарообразных частиц, не имеющих межмолекулярного взаимодействия, вязкость описывается уравнением Эйнштейна:
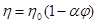 , ,
где j - объемная концентрация дисперсной фазы в зоне;
h0
- динамическая вязкость дисперсионной среды;
a - коэффициент, зависящий от формы частиц.
Видоизменив, получим:
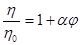 - относительная вязкость - относительная вязкость
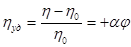 - удельная вязкость = hотн
-1 - удельная вязкость = hотн
-1
Из уравнения следует, что:
1) h пропорциональна концентрации дисперсной фазы;
2) hдисп. системы
>hдисп. среды
Для концентрированных систем уравнение Эйнштейна не применимо. Это объясняется целым рядом причин:
1. В жидкости около частиц возникает макропоток, затрудняющий движение системы;
Реклама

2. Сольватация частиц. Оно проявляется в увеличении объема частиц за счет адсорбции дисперсионной среды;
3. Проявление сил отталкивания между частицами, несущими одинаковые заряды. Смолуховский показал, что hзаряженных частиц
больше, чем hнезаряженных
.
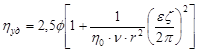 ,
,
где h0
– вязкость среды;
n - удельная электропроводность;
r - радиус частиц;
e - диэлектрическая проницаемость.
Структурная вязкость - вязкость структурированных систем, т.е. систем, где наблюдается явная тенденция образования пространственных молекулярных сеток между частицами дисперсной фазы. Они не подчиняются закону Ньютона и в случае образования структуры течение системы начинается лишь тогда, когда напряжение сдвига Р превысит какое-либо критическое значение 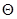 , необходимое для разрушения структуры, т.е. когда начинает выполняться условие Р > , необходимое для разрушения структуры, т.е. когда начинает выполняться условие Р > 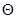 . Такое течение Бингам назвал пластическим, а критическое напряжение сдвига (предельное) – пределом текучести. . Такое течение Бингам назвал пластическим, а критическое напряжение сдвига (предельное) – пределом текучести.
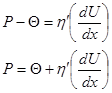 - уравнение Бингама, - уравнение Бингама,
где h
- вязкость, отвечающая пластическому течению системы или пластическая вязкость;
dU/dx – градиент скорости, если 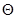 = 0, то уравнение переходит в уравнение Ньютона. = 0, то уравнение переходит в уравнение Ньютона.
Из рис. 5.1.2.1 видно: Бингам считал, что течение начнется сразу после превышения 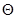 . В этом случае . В этом случае
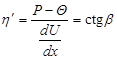
Реальные системы имеют зависимость, показанную на рис. 5.1.2.2. Причина отличия в том, что структура разрушается не сразу, а по мере увеличения градиента скорости движения жидкости. Можно различить 3 критических напряжения:
1. 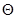 f
– минимальный предел текучести, соответствующий началу течения (началу разрушения системы). f
– минимальный предел текучести, соответствующий началу течения (началу разрушения системы).
2. 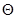 B
– предел текучести по Бингаму B
– предел текучести по Бингаму
3. 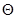 max
– максимальный предел текучести, соответствующий значению Р, когда структура разрушилась полностью. max
– максимальный предел текучести, соответствующий значению Р, когда структура разрушилась полностью.
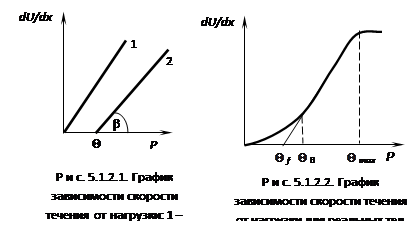
Теория Эйнштейна была использована Штаудингером для установления формулы вязкости разбавленных растворов полимеров. Для растворов, содержащих палочкообразные макромолекулы, должно соблюдаться соотношение
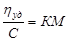 , ,
где 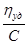 приведенная вязкость; hуд
= КМС приведенная вязкость; hуд
= КМС
Удельная вязкость прямо пропорциональна концентрации и молекулярной массе полимера; К определяют независимым методом, например, по растворам полимеров с известной молекулярной массой М. Она зависит от данного гомологического ряда и растворителя; С – массовая концентрация полимера.
Уравнение справедливо лишь для полимеров с короткими жесткими цепями, которые могут сохранять палочкообразную форму. Гибкие молекулы с длинными цепями, обычно свертываются в клубок, что уменьшает сопротивление движению. При этом К изменяется и зависимость становится нелинейной.
Широкое распространение для определения молекулярной массы полимера с гибкими и длинными макромолекулами получило уравнение Марка-Куна-Хаувинка:
[h]=КМа
,
где К и а – постоянные для данного гомологического ряда и растворителя.
В данном случае связывают с молекулярной массой полимера характеристическую вязкость [h], т.к. именно этой величиной оценивается прирост вязкости раствора, вызванный наличием макрочастиц и их вращением
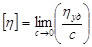
Для разбавленных растворов, полимеров широко используется зависимость удельной вязкости от концентрации.
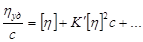 - уравнение Хаггинса, - уравнение Хаггинса,
включающая константу К/
, которая характеризует взаимодействие полимера с растворителем. Чем хуже растворитель, тем лучше значения К/
. Формула удобна для экстраполяции [h] при бесконечном разбавлении.
[h]характеристическая вязкость, она оценивает прирост вязкости раствора, вызванный наличием макрочастиц и их вращений.
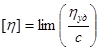 . .
Представлены три наиболее распространенных метода измерения вязкости:
1. Капиллярный метод (вискозиметр Оствальда).
В специальный капилляр заливают определенный объем жидкости V (см3
) и она вытекает под давлением Р (дин/см2
) в течение времени t(сек), высота l и радиус r. Пуазейль показал:
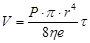 , где h - коэффициент вязкости. , где h - коэффициент вязкости.
Чаще проводят сравнительное определение вязкости. Для этого измеряют время истечения t и t1
одинаковых объемов испытуемой и стандартной жидкости, тогда
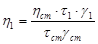 , ,
где g - плотность.
2. Метод падающего шарика.
Измеряется скорость v, с которой шарик из известного материала падает в вязкой среде. Стокс вывел уравнение:
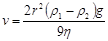 , ,
где r – радиус шарика;
r1
– плотность шарика;
r2
– плотность среды.
Можно проводить и относительные измерения:
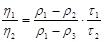 . .
3. Метод вращающегося цилиндра.
Внешний цилиндр вращается с постоянной скоростью. От него начинает вращаться жидкость в сосуде, а затем и сам внутренний цилиндр, подвешенный внутри на нити. По углу закручивания внутреннего цилиндра a и постоянной угловой скоростью w в двух различных жидкостях, для одной из них h известна.
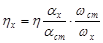 . .
После коагуляции структура дисперсных систем приобретает некоторое постоянство во взаиморасположении частиц, т.е. свободнодисперсная система переходит в связаннодисперсную. Структура этих систем характеризуется вязкостью, упругостью, пластичностью, прочностью. Эти свойства и называются структурно-механическими и зависят от интенсивности взаимодействия частиц со средой и между собой.
Анализ многообразия свойств в дисперсных системах позволил П.А. Ребиндеру разделить их на два основных класса, различающихся по видам взаимодействия частиц дисперсной фазы. Исходя из того, что коагуляция соответствует первичному и вторичному минимуму, на потенциальной кривой взаимодействия частиц, он предложил различать конденсационно-кристаллизационные и коагуляционные структуры. Конденсационно-кристаллизационное структурообразование, отвечающее коагуляции в первичном минимуме (яме), происходит путем непосредственного химического взаимодействия между частицами и их срастание с образованием жесткой объемной структуры.
Если частицы аморфные, то структуры, образующиеся в дисперсных системах называют конденсационными, если частицы кристаллические, то – кристаллизационным. При непосредственном срастании частиц механические свойства структур соответствуют свойством самих частиц. Первый тип структуры характерен для связно-дисперсных систем, т.е. систем с твердой дисперсионной средой. Такие структуры придают телам прочность, хрупкость и не восстанавливаются после разрушения. Течение такой системы возможно при наличии вакансий решетки частиц, т.е. незанятых частицами узлов, а также другими эффектами решетки. При деформировании кристаллоподобной структуры в ней возникают упругие напряжения, которые со временем исчезают, благодаря постепенному перемещению вакансий. Скорость этого перемещения может быть ограничена, что приводит к дилатантному типу зависимости, т.е. к увеличению вязкости с ростом напряжения. Начальная вязкость обратно пропорциональна концентрации вакансий. При отсутствии потенциального барьера 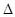 Umax
= 0 происходит непосредственный (фазовый) контакт частиц h0
= 0. Перекристаллизация дисперсной фазы в точках контакта ведет к образованию прочной, но хрупкой структурной сетки. Такие структуры называются кристаллизационными. Umax
= 0 происходит непосредственный (фазовый) контакт частиц h0
= 0. Перекристаллизация дисперсной фазы в точках контакта ведет к образованию прочной, но хрупкой структурной сетки. Такие структуры называются кристаллизационными.
Под коагуляционными структурами понимают структуры, которые образуются при коагуляции, соответствующей второму минимуму потенциальной кривой взаимодействия частиц. Взаимодействие частиц происходит через прослойки дисперсионной среды, является, как правило, Ван-дер-ваальсовским и поэтому пространственный каркас не обладает большой прочностью. Между частицами дисперсной фазы взаимодействие осуществляется через прослойки дисперсионной среды. Наиболее распространенный вид структурообразования – это возникновение рыхлой пространственной сетки за счет преобладания притяжения частиц на расстоянии h = h0
. Необходимым условием образования такой структуры является заметная величина потенциальной ямы и концентрация частиц больше 0,01 – 0,1 объемной доли, достаточное для образования сплошной пространственной сетки.
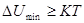
Механические свойства коагуляционных структур определяются свойствами частиц, образующих структуру, характером и особенностями межчастичных связей и прослоек среды. Они имеют обычно жидкую дисперсионную среду. Для них характерна способность восстанавливать свою структуру во времени после их механического разрушения. Т.к. обратимое изотермическое разрушение структуры при механическом воздействии и ее последовательное восстановление после снятия нагрузки называется тиксотропией, то соответствующие структуры часто называют коагуляционно – тиксотропными. Самопроизвольное восстановление коагуляционной структуры свидетельствует о том, что она обладает наибольшей механической прочностью при относительном минимуме энергии Гиббса. Такого соответствия нет у конденсационно-кристаллизационных структур, которые образуются обычно в условиях высоких пересыщений и поэтому термодинамически неустойчивы. Их высокая прочность обеспечивается одновременным уменьшением пересыщений и внутренних напряжений.
Коагуляционная структура способна разрушаться при механическом воздействии, например, при течении до отдельных частиц.
|