1)Предмет и задачи БХ:
БХ изуч. химич состав живых организмов,вкл человека, и природы химич процессов происходящих как в целостном организме, так и в изолированных органах и тканях на клеточном, субклеточном и молекулярном уровнях. БХ,изучающая химич основы жизнедеятельности организмов в норме и при патологии, призвана установить связь между молекулярной структурой и биологич фу-ей химич компонентов живой материи. живые существа могут существовать только при пост обновлении их структур. Для синтеза нов структур нужны исходные материалы и энергия, это все получают из окр среды.
Даже в сост покоя каждой клетке необходима Э. для обновления струтур,т е для выживания. Источник Э. у животных - распад органич в-в
2) Обмен веществ: Питание, метаболизм и выделение продуктов метаболизма. Состав пищи человека. Органические и минеральные компоненты. Основные и минорные компоненты:
Питании - в N приход калорий соотв энергозатратам, поэтому нет необходимости ни в запасании, ни в использ имеющихся запасов, процентное поступл калорий в виде белков, липилов, у глеводов, соотносится как 15:35:50. Минорные компоненты пищи - биофлавоноиды, индолы, фитостеролы, изотиоционаты и др.
Метаболизм - совокупность химических реакций и сопутствующих им
химических процессов в организме, в результате которых происходит
поступление веществ, их усвоение, использование в процессах
жизнедеятельности и выделение ненужных соединений в окружающую среду. N: 100–120 г белка в сутки
100—150 г жира в сутки
430—630 г углеводов в сутки.
4) Незаменимые факторы питания,их медико-биологическое значение:
Среди факторов питания обычно различают два класса пищевых в-в — макронутриентов, кот вкл белки, жиры и углеводы и микронутриентов или класс минорных пищевых в-в, присутств в пище в мин концентрациях, миллиграммах и микрограммах. Макронутриенты присутств в пище в относительно больших кол-ах и явл основн источниками Э. и строительных компонентов. Микронутриенты выполн широкий круг важных регуляторн, метаболич и защитных ф-ий. К микронутриентам относ:
- аминокислоты; - витамины;
- макроэлементы; - микроэлементы;
- полиненасыщенные жирные кислоты и фосфолипиды; - пищевые волокна; - различные органические растительные продукты.
Реклама

5)Незаменимые аминокислоты. Изменение Потребности в них в зависимости от возраста, от физиологического состояния и патологии:
Незаменимые аминокислоты — необходимые аминокислоты, которые не могут быть синтезированы в том или ином организме (человека). Поэтому их поступление в организм с пищей необходимо. Отсутствие или недостаток незаменимых аминок-т приводит к остановке роста, падению массы, нарушениям обмена в-в, при острой недостаточности - к гибели организма.
Незамен аминок-ты:
Аргинин
содержится в твороге, морепрод, кур мясе, грецк орехах, печени, шоколаде.
Валин
в зерновых, мясе, грибах, молочных прод, арахисе, сое
Гистидин
в тунце, лососеговяжьем филе, куриных грудках, сое, арахисе,
Изолейцин
в миндале, кешью, кур мясе, яйцах, рыбе, чечевице, печени,
Лейцин
в мясе, рыбе, бур рисе, чечевице, орехах, в семянах.
Лизин
в рыбе, мясе, молочн прод, пшенице,орехах.
Метионин
в молоке, мясе, рыбе, яйцах, бобах, фасоли, чечевице и сое.
Треонин
в молочных продуктах и яйцах, в умеренных количествах в орехах и бобах.
Триптофан
в мясе, овсе, бананах, сушёных финиках, арахисе, кунжуте, кедровых орехах, молоке, йогурте, твороге, рыбе, курице, индейке.
Фенилаланин
в говядине, кур мясе, рыбе, бобах, яйцах, твороге, молоке.
Потребность в незаменимых аминокислотах в различном возрасте мг / кг / сут
| Аминокислоты
|
Дети раннего возраста (3-4 мес.)
|
Дети (2 лет)
|
Школьники, мальчики (10-12 лет)
|
Взрослые
|
| Гистидин |
28 |
- |
- |
8-12 |
| Изолейцин |
70 |
31 |
28 |
10 |
| Лейцин |
161 |
73 |
44 |
14 |
| Лизин |
103 |
64 |
44 |
14 |
| Метионин + цистеин |
58 |
27 |
22 |
13 |
| Фенилаланин + тирозин |
125 |
69 |
22 |
14 |
| Треонин |
87 |
37 |
28 |
7 |
| Триптофан |
17 |
12,5 |
3,3 |
3,5 |
| Валин |
93 |
38 |
25 |
10 |
| Всего незаменимых аминокислот |
714 |
352 |
216 |
84 |
6)Представление об азотистом балансе и его состоянии в зависимости от возраста и вида патологии.
-о приходе и расходе белка судят по приходу и расходу азота, для этого кол-во азота умножают на 6,25 (напр с мочой выделилось 12 г азота, суточный расход равен = 12*6,25=75 г)
Возможны 3 варианта баланса - азотистое равновесие, отриц.(расход > приход – опухолевый рост) и положительный азот баланс(приход>расхода – рост, беременность, наращивание мыш массы).
7) Аминокислотный состав белков, пептидная связь, ее характ-ка:
Белки-высокомолекулярные биологич полимеры,составленные из 21 разл мономера- альфа аминокислотных остатков, соединенных пептидной связью. Если аминокислотн цепь содержит менее 10-20 остатков аминокислот, ее наз- пептидом, если более –полипептидом. Полипептиды сост из 50 и более аминокислотных остатков, наз – белками. Общ форм. аминок-т:
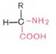
Пептидные связи
соедин аминогруппу одной аминок-ты с карбоксильной гр др аминок-ты. (т о - образование полимера).
Пепт. сязи оч. прочные,для их разруш вне организма требуются выс температуры и давл, сильно кислая или сильно щелочная среда и длит время. В клетках ораганизма пептсвязи разры-ся протеолитич ферментами.Вращение вокруг связи C-N треб больш затрат Э. и затруднено. Пепт цепь имеет одно направление и два разн конца – N-конец несет свободную аминогр первой аминок-ты (начало белк цепи) и C-конец несет карбокс гр последнего аминокисл остатка.
Реклама

8)Уровни организации бел молекул. Структуры белка, их характ-ка:
Б. представл собой сложные полипептиды,аминок-ты в кот связаны пептидн связми,образ-мися при взаимод Альфа-карбоксильных и Альфа-аминогрупп аминок-т.
К дипептиду могут присоедин др аминок-ты, образуя три-, тетра-, пентапептид и т д вплоть до образ крупн полипептида.Последоват-сть расположения аминок-т в полипептиде предстал собой первичную структуру белка. Всего сущ 4 уровня структурной организации белка- первичная, вторичн, тетичн, четвертичная структура. Структура большинства белков сост из 3 уровней.
Первичная:
Последовательность расположения аминокислотн остатков в полипептиде. Особенности:
-первичн структура Б. генетически детерминирована и уникальна,замена аминок-т внутри полипетидной цепи привод к изменению структуры и фу-ии белка
- она стабильна,это обеспеч-ся дипептидными и дисульфидными связями
-число комбинаций аминок-т в полипептиде оч. велико,повторяющ-ся последоват-сти аминок-т редки. Идентичные последоват-стя аминок-т м встреч-ся в обл активных центров ферментов
-она детерминирует торичную,третичную и четвертичную структуру белк молекулы.
Вторичная:
-
конфигурация полипептидной цепи,более компактная ее упаковка в спиральную или какую-л др конформацию. Процесс конфигурации идет в соотв с программой,заложенной в первичн структуре Б. Сущ две осн конфигурации полипептидной цепи: Альфа-спираль и Бета-сладчатый слой.
Третичная:
-это пространственная ориентация полипептидной спирали, следующий за вторичн структурой способ компактизации белк. молекулы. Процесс укладки полипептидной цепи-фолдинг.Третичн струк Б формир-ся самопроизвольно и полностью детерминир-ся первичн структ Б.Основной движущий момент-взимод радикаловаминок-т с мол воды,сост в том,что гидрофобные радикалы аминок-т ориентир-ся внутрь мол Б, в то время как гидрофильные ридикалы ориентир-ся наружу.
Четвертичная:
-пространственная ориентация нескольких полипептидных цепей, облад. собственной первичной, вторичн или третичной структурой, с образ макромолекулярного образования.
9) Лабильность пространственной структуры Б. Факторы вызывающие денатурацию Белка.
Лабильность-св-во белков незначительно изменять конформацию посредством разрыва одних и образ др слабых связей без потери биологич активности. Связи участв в формир трехмерной простаранств структуры и четвертичн структ олигомерных белков относ к числу слабых: Э. водородных, ионных и гидрофоьбных связей при комнатн тмпературе сопоставима с Э. теплового движения атомов.Тепл движ атомов,вход в состав Б,вызыв разрыв одних и образ др слабых связей,что привод к наруш биологич фу-ии Б.Конформация Б м незначит измен-ся в некотор диапазоне физич(температ,давл), химич (pH, концентр ионов) параметров, при взаимод с др молекулами.
При экстремальн знач pH,выс температ или под действ денатурирующ факторо происх разрыв слаб сязей, наступ денатурация Б
– изменение натиной конформации Б, сопровожд потерей его биологич активности. Разруш активн центр Б. измен-ся трехмерная структура Б,но первичн структура не разруш,пептидн связи не разрыв-ся.
Факторы,вызыв Денатурацию:
Выс температ –выше 60 градусов (разруш слабые сязи-стерилизация ); кислоты и щелочи; мочевина гуанидинхлорид; спирт и фенол разруш гидрофобные и водородные связи; соли тяж металлов образ нераствор соли Б и этих металлов.
10)Тип связей формир третичную и четвертичн структуру Б:
Третичная структура:
-гидрофобные взимодействия (слаб взаимод между неполярными радикалами, кот привод к тому,что гидрофобныерадикалы аминок-т оказываются внутри глобулярной структуры Б,образовав гидрофобное ядро)
-ионные и водородные связи (между гидрофильными гр радикалов аминок-т,оказавшихся внутри гидрофобного ядра. Ионные и вобородные связи, а также гидрофобные взаимод относ-ся к числу слабых,их Э. не намного превышает Э тепл движ мол при комн температуре.)
-ковалентные дисульфидные связи –S-S (между цистеиновыми остатками,наход в разных местах полипепт цепи).это инсулин и иммуноглобулины. Четвертичная структура:
-это пространственное взаиморасположение полипептидных цепей (субединиц или протомеров), объединенных слабыми (гидрофобными,ионными, водородными) взаимодействиями.Б,сост из 2 и более субъединиц,наз олигомерами. Белк субъединица -протомер, может сост из одной,так и дух полипептидных цепей.
денатурация Б
– изменение натиной конформации Б, сопровожд потерей его биологич активности. Разруш активн центр Б. измен-ся трехмерная структура Б,но первичн структура не разруш,пептидн связи не разрыв-ся.
Факторы,вызыв Денатурацию:
Выс температ –выше 60 градусов (разруш слабые сязи-стерилизация ); кислоты и щелочи; мочевина гуанидинхлорид; спирт и фенол разруш гидрофобные и водородные связи; соли тяж металлов образ нераствор соли Б и этих металлов.
11) Четвертичная структура белков. Особенности строение и функционирования олигомерных белков на примере гемсодержащих белков – гемоглобина и миоглобина
:
-пространственная ориентация нескольких полипептидных цепей, облад. собственной первичной, вторичн или третичной структурой, с образ макромолекулярного образования.
У олигомерных Б появл св-ва,отсутствующие у мономерных Б. Формирование четвертичн структуры ведет к усложнению фу-ии,появл возможность регуляции этих фу-ий. При взаимод одного из протомеров со специфич лигандом происх конформационные изменения всего олигомерного Б и меняется сродсто остальных протомеров к лигандам.
Напр олигомерный белок гемоглобн,сост из 4 протомеров - родственен миоглобину, глбулярному Б,сост из 1 полипепт цепи. Вторичн и третичн структура этих Б имеетмного общего, несмотря на различия в первин структуре. Миоглобин и кажд субъединица гемоглобина содержит 8 Альфа-спиральных участков,образ глобулу и связанных с небелковой частью- геном, в центре кот наход железо Fe. Гидрофобные части генма окружены гидрофобнымирадикалами аминокислотн остатков,кроме Гис F8 и Гис E7,располаг-ся с двух сторон от плоскости гемма.
Миоглобин депонир кислород в красных мыш волокнах и освобожд его при интенсивной мыш работе,после чего кислород использ для получ Э, необход мышцам. Ф-ии гемоглобина сложнее,главная- транспорт кислорода из легких в ткани, т е связывание кислорода в лугких и его диссоциация в капиллярах ткани.
12) Физико-химические свойства белков и их классификация:
- молекулярная масса, которая зависит от кол-ва аминокислотных остатков в полипептидной цепи, а у олигомеров - и от числа протомеров, входящих в его состав; ее величина колеблется в пределах 6000 - 1000000 Д, но может быть и выше;
-форма мол, кот м б глобулярной (компактной за счет того, что гидрофобные радикалы аминокислот сгруппированы в гидрофобное ядро) или фибриллярной. Форма белковой мол зависит от рН. В изоэлек-трич точке молекула наиболее компактна, а при изменении рН увеличивается;
-суммарный заряд мол, зависящий от соотношения ионизированных анионных радикалов глутаминовой и аспарагиновой кислот и катионных радикалов лизина, аргинина и гистидина. Степень ионизации зависит от рН среды:
- при рН=7 практически все ионогенные гр б ионизированы;
- в кислой среде увеличение концентрации Н+
подавляет диссоциацию карбоксильных гр и уменьш отрицат заряд б:
-СОО-
+ Н+
- -СООН
- в щелочной среде избыток ОН-
приводит к уменьш полож заряда б:
-NH3
+
+ ОН-
- -NH2
+H2
0
Величина рН среды, при кот суммарный заряд б равен нулю, наз изоэлектрич точкой. Б, облад кислотными св-ми (альбумины, глобулины, пепсины) имеют в составе больше анионогенных (—СООН) гр, их изоэлектрич точка лежит в слабокислой среде, а в нейтральной среде они имеют отрицат заряд. Б, обладающ основными св-ми (гистоны, протамины), имеют в составе больше катионо-генных гр, их изоэлектрич точка лежит в щелочной среде, в нейтральной среде они имеют полож заряд.
-растворимость в водной среде, кот определ-ся гидрофильностью (способностью образовывать гидратную оболочку). На растворимость так же влияет форма мол и состав растворителя: больш-во б лучше раствор-ся в слабом солевом р-ре, чем в дистиллиров воде. Б, имеющ любой, отличный от нуля заряд, лучше раствор, чем белки, находящ в изоэлектрич точке. Легкость осаждения белков в изоэлектрич точке - результат исчезновения их электростатич отталкивания, что приводит к агрегации мол б и выпадению их в осадок.Б, поверхности кот обогащены гидрофобными радикалами, лучше раствор-ся в липидах, чем в воде.
Глобулярным
б свойственна сферич (глобулярная) форма, они отлич высокоупорядоченной конформацией и обычно несут в клетке динамические ф-ии., внутрь глобулы собраны гидрофобные радикалы, образующ гидрофобное ядро, а на поверхности экспонированы гидрофильные остатки, обеспеч хорошую раствор-ть глобулярных б. К глоб. б относ почти все ферменты, at, некот гормоны (инсулин) и транспортные б.
Фибриллярные
б хар-ся вытянутой нитевидной структурой, они устойчивы, нераствор в воде и разбавленных солевых р-ах. Эти б - основные структурные элементы соединит тк.
По своему составу б раздел на :
Простые белки
содержат в своем составе только полипептидные цепи. При гидролизе они дают аминок-ы и не образ никаких др органич или неорганич прод (альбумины, глобулины облад кислым характером); протамины, гистоны (облад основным характером).
Сложные белки
(холопротеины) состоят из белковой части (апопротеина) и небелковой части (простетическая группа). Простетическая группа - ионы металлов или органич мол, присоедин-ся к б слабыми или ковалентными связями.
|