СОДЕРЖАНИЕ
1.Введение……………………………………………………………………….3
2.Общие сведения……………………………………………………………….5
2.1. Химические свойства………………………………………………………5
2.2.Физические свойства………………………………………………………..6
3.Атомно-кристаллическое строение металлов……………………………….8
4.Основы получения чугуна и стали…………………………………………...10
4.1.Получение чугуна…………………………………………………………...10
4.1.1Общие сведения…………………………………………………………....10
4.1.2Основы получения………………………………………………………....11
4.2.Производство стали………………………………………………………....12
4.2.1.Общие сведения о стали…………………………………………………..12
4.2.2Основы получения стали…………………………………………………..15
5.Механические свойства металлов……………………………………………19
5.1.Статистические испытания…………………………………………………19
5.2.Динамические испытания…………………………………………………...21
5.3.Усталостные (на выносливость) испытания………………………………..22
6.Влияние углерода и постоянных примесей на свойства сталей……………23
7.Заключение…………………………………………………………………….24
8.Список литературы……………………………………………………………25
1 ВВЕДЕНИЕ
Металлы – наиболее распространенные и широко используемые материалы в производстве и в быту человека. Особенно велико значение металлов в наше время, когда большое их количество используют в машиностроительной промышленности, на транспорте, в промышленном, жилищном и дорожном строительстве, а также в других отраслях народного хозяйства./1, стр. 4/
Термин «металл» произошёл от греческого слова métallon (от metalléuō – выкапываю, добываю из земли), которое означало первоначально копи, рудники (в этом смысле оно встречается у Геродота, 5 в. до н. э.). То, что добывалось в рудниках, Платон называл metalléia. В древности и в средние века считалось, что существует только 7 металлов: золото, серебро, медь, олово, свинец, железо, ртуть. По алхимическим представлениям, металлы зарождались в земных недрах под влиянием лучей планет и постепенно крайне медленно совершенствовались, превращаясь в серебро и золото. Алхимики полагали, что металлы – вещества сложные, состоящие из «начала металличности» (ртути) и «начала горючести» (серы). В начале 18 в. получила распространение гипотеза, согласно которой металлы состоят из земли и «начала горючести» – флогистона. М.В. Ломоносов насчитывал 6 металлов (Au, Ag, Cu, Sn, Fe, Pb) и определял металл как «светлое тело, которое ковать можно». В конце 18 в. А.Л. Лавуазье опроверг гипотезу Флогистона и показал, что металлы – простые вещества. В 1789 Лавуазье в руководстве по химии дал список простых веществ, в который включил все известные тогда 17 металлов (Sb, Ag, As, Bi, Co, Cu, Sn, Fe, Mn, Hg, Mo, Ni, Au, Pt, Pb, W, Zn). По мере развития методов химического исследования число известных металлов возрастало. В первой половине 19 в. были открыты спутники платины(Pt), получены путём электролиза некоторые щелочные и щёлочноземельные металлы, положено начало разделению редкоземельных металлов, открыты неизвестные металлы при химическом анализе минералов. В 1860-63 методом спектрального анализа были открыты Cs, Rb, Tl, In. Блестяще подтвердилось существование металлов, предсказанных Д. И. Менделеевым на основе его периодического закона. Открытие радиоактивности в конце 19 в. повлекло за собой поиски природных радиоактивных металлов, увенчавшиеся полным успехом. Наконец, методом ядерных превращений начиная с середины 20 в. были искусственно получены радиоактивные металлы, в частности трансурановые элементы.
Реклама

В конце 19-начале 20 в.в. получила физико-химическую основу металлургия- наука о производстве металлов из природного сырья .Тогда же началось исследование свойств металлов и их сплавов в зависимости от состава и строения/3, стр. 133/
Основы современного металловедения были заложены выдающимися русскими металлургами П.П. Аносовым (1799–1851) и Д.К. Черновым (1839–1921), впервые установившими связь между строением и свойствами металлов и сплавов.
П. П. Аносов заложил основы учения о стали, разработал научные принципы получения высококачественной стали, впервые в мире в 1831 г. применил микроскоп для исследования строения металлов.
Д. К. Чернов продолжил труды П. П. Аносова. Он по праву считается основоположником металлографии – науки о строении металлов и сплавов. Его научные открытия легли в основу процессов ковки, прокатки, термической обработки стали.
Открытые Д. К. Черновым критические точки в стали явились основой для построения современной диаграммы состояния системы железо – углерод.
Классические труды «отца металлографии» Д. К. Чернова развивали выдающиеся русские ученые. Первое подробное описание структур железоуглеродистых сплавов было сделано А. А. Ржешотарским(1898). Дальнейшее развитие металловедение получило в работах видных отечественных ученых Н. И. Беляева, Н. С. Курнакова, А. А. Байкова, С. С. Штейнберга, А. А. Бочвара, Г. В. Курдюмова и др.
Реклама

Наука о металлах развивается широким фронтом во вновь созданных научных центрах с применением электронных микроскопов и другой современной аппаратуры, с использованием достижений рентгенографии и физики твердого тела. Все это позволяет более глубоко изучить строение металлов и сплавов и находить новые пути повышения механических и физико-химических свойств. Создаются сверхтвердые сплавы, сплавы с заранее заданными свойствами, многослойные композиции с широким спектром свойств и многие другие металлические, алмазные и керамико-металлические материалы /1, стр. 58/.
2 ОБЩИЕ СВЕДЕНИЯ
В строительстве обычно применяют не чистые металлы, а сплавы. Наибольшее распространение получили сплавы на основе черных металлов (~94%) и незначительное – сплавы цветных металлов (рис. 1) /2, стр.288/
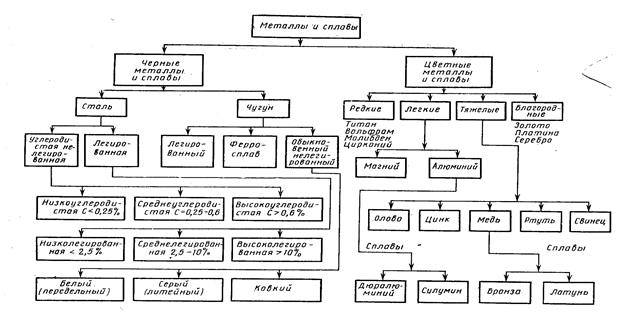
рис. 1
2.1 Химические свойства
В соответствии с местом, занимаемым в периодической системе элементов, различают металлы главных и побочных подгрупп. Металлы главных подгрупп (подгруппы а)
называются также непереходными. Эти металлы характеризуются тем, что в их атомах происходит последовательное заполнение s-и p-электронных оболочек. В атомах металлов побочных подгрупп (подгруппы б
), называемых переходными, происходит достраивание d- и f
-оболочек, в соответствии с чем их делят на d-группу и две f-группы – лантаноиды
и актиноиды.
Вподгруппыа
входят 22 металла: Li, Na, К, Rb, Cs, Fr (I a
); Be, Mg, Ca, Sr, Ba, Ra (II a
); Al, Ga, In, Tl (III a
); Ge, Sn, Pb (IV a
); Sb, Bi (V a
); Po (VI a
). Вподгруппыб
входят: 1) 33 переходныхметалла d-группы [Сu, Ag, Аи (I б
); Zn, Cd, Hg (II б
); Sc, Y, La, Ac (III 6
); Ti, Zr, Hf, Ku (IV б
); V, Nb, Та, элементс Z = 105 (V б
); Сr, Mo, W (VI б
);
Mn, Тс, Re (VII б
); Fe, Co, Ni, Ru, Rh, Pd, Os, Ir, Pt (VIII б
)]; 2) 28 металлов f-группы (14 лантаноидови 14 актиноидов).
Электронная структура атомов некоторых d-элементов имеет ту особенность, что один из электронов внешнего уровня переходит на d-подуровень. Это происходит при достройке этого подуровня до 5 или 10 электронов. Поэтому электронная структура валентных подуровней атомов d-элементов, находящихся в одной подгруппе, не всегда одинакова. Например, Cr и Мо (подгруппа VIб
) имеют внешнюю электронную структуру соответственно 3d5
4s1
и 4d5
5s1
, тогда как у W она 5d4
6s2
. В атоме Pd (подгруппа VIII6
)два внешних электрона «перешли» на соседний валентный подуровень, и для атома Pd наблюдается d10
вместо ожидаемого d8
s2
.
Металлам присущи многие общие химические свойства, обусловленные слабой связью валентных электронов с ядром атома: образование положительно заряженных ионов (катионов), проявление положительной валентности (окислительного числа), образование основных окислов и гидроокисей, замещение водорода в кислотах и т.д. Металлические свойства элементов можно сравнить, сопоставляя их электроотрицательность [способность атомов в молекулах (в ковалентной связи) притягивать электроны, выражена в условных единицах]; элементу присущи свойства металла тем больше, чем ниже его электроотрицательность (чем сильнее выражен электроположительный характер).
Если расположить металлы в последовательности увеличения их нормальных потенциалов,
получим так называемый ряд напряжений или ряд активностей
. Рассмотрение этого ряда показывает, что по мере приближения к его концу – от щелочных и щёлочноземельных металлам к Pt и Аи – электроположительный характер членов ряда уменьшается. Металлы от Li по Na вытесняют Н2
из Н2
О на холоду, а от Mg по Тl – при нагревании. Все металлы, стоящие в ряду выше Н2
, вытесняют его из разбавленных кислот (на холоду или при нагревании). Металлы, стоящие ниже Н2
, растворяются только в кислородных кислотах (таких, как концентрирированная H2
SO4
при нагревании или HNO3
), aPt, Аи – только в царской водке (Ir нерастворим и в ней).
Металлы от Liдо Na легко реагируют с О2
на холоду; последующие члены ряда соединяются с О2
только при нагревании, aIr, Pt, Аи в прямое взаимодействие с О2
не вступают. Окислы металлов от LinoAl и от LanoZn трудно восстановимы; по мере продвижения к концу ряда восстановимость окислов увеличивается, а окислы последних его членов разлагаются на металлы и О2
уже при слабом нагревании. О прочности соединений металлов с кислородом (и др. неметаллами) можно судить и по разности их электроотрицательностей: чем она больше, тем прочнее соединение /3, стр. 133-134/.
2.2Физические свойства
Большинство металлов кристаллизуется в относительно простых структурах – кубических и гексагональных ЛГУ, соответствующих наиболее плотной упаковке атомов. Лишь небольшое число металлов имеет более сложные типы кристаллических решёток. Многие металлы в зависимости от внешних условий (температуры, давления) могут существовать в виде двух или более кристаллических модификаций.
Электрические свойства.
Удельная электропроводность металлов при комнатной температуре σ~10-6
–10-4
ом
-1
см
-1
, тогда как у диэлектриков,
например, у серы, σ~10-17
ом
-1
см
-1
. Промежуточные значения удельной электропроводности σ соответствуют полупроводникам.
Характерным свойством металлов как проводников электрического тока является линейная зависимость между плотностью тока и напряжённостью приложенного электрического поля.
Носителями тока в металлах являются электроны проводимости, обладающие высокой подвижностью. Согласно квантово-механическим представлениям, в идеальном кристалле
электроны проводимости (при полном отсутствии тепловых колебаний кристаллической решётки)
вообще не встречают сопротивления на своём пути. Существование у реальных металлов электросопротивления является результатом нарушения периодичности кристаллической решётки. Эти нарушения могут быть связаны как с тепловым движением атомов, так и с наличием примесных атомов, вакансий, дислокаций
и др. дефектов в кристаллах.
На тепловых колебаниях и дефектах (а также друг на друге) происходит рассеяние электронов.
При нагревании металлов до высоких температур наблюдается «испарение» электронов с поверхности металлов (термоэлектронная эмиссия)
. Эмиссия электронов с поверхности металлов происходит также под действием сильных электрических полей примерно 107
в/см
в результате туннельного просачивания электронов через сниженный полем потенциальный барьер. В металлах наблюдаются явления фотоэлектронной эмиссии, вторичной электронной эмиссии
и ионно-электронной эмиссии.
Перепад температуры вызывает в металлах появление электрического тока или разности потенциалов
Тепловые свойства.
Теплоёмкость металлов обусловлена как ионным остовом (решёточная теплоёмкость Ср
), так и электронным газом (электронная теплоёмкость Сэ
). Хотя концентрация электронов проводимости в металлах очень велика и не зависит от температуры, электронная теплоёмкость мала и у большинства металлов наблюдается только при температурах в несколько градусов кельвина. Теплопроводность металлов осуществляется главным образом электронами проводимости.
Магнитные свойства
.
Переходные металлы с недостроенными f
-
и d-электронными оболочками являются парамагнетиками.
Некоторые из них при определённых температурах переходят в магнитоупорядоченное состояние. Магнитное упорядочение существенно влияет на все свойства металлов, в частности на электрические свойства: в электросопротивление вносит вклад рассеяние электронов на колебаниях магнитных моментов. Гальваномагнитные явления при этом также приобретают специфические черты.
Магнитные свойства остальных металлов определяются электронами проводимости, которые вносят вклад в диамагнитную и парамагнитную восприимчивости металлов, и диамагнитной восприимчивостью ионного состава. Магнитная восприимчивость X большинства металлов относительно мала (X ~ 10-6
) и слабо зависит от температуры.
3 АТОМНО-КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
Исследование структуры металла проводят путем изучения макроструктуры с увеличением до 10 раз и без увеличения; микроструктуры с увеличением от 10 до 2000 раз на оптических микроскопах и до 100 000 раз на электронных микроскопах, атомной структуры – рентгенографическим анализом.
Металлы представляют собой кристаллические тела с закономерным расположением атомов в узлах пространственной решетки.
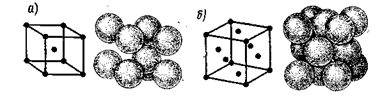
Элементарный кубический кристалл: а – объемно-центрированный; б –
гранецентрированный .рис 2
Решетки состоят из ряда кристаллических плоскостей, расположенных друг от друга на расстоянии нескольких нанометров (1 нм=10-9
м). Для железа эти расстояния 28,4 нм (α-железо) и 36,3 нм (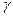 -железо). Большинство металлов имеет пространственные решетки в виде простых геометрических фигур. Отдельные участки кристаллической решетки прочно связаны между собой в комплексы – зерна. Взаимное расположение зерен отдельных элементов и сплавов определяет структуру металлов и их свойства. -железо). Большинство металлов имеет пространственные решетки в виде простых геометрических фигур. Отдельные участки кристаллической решетки прочно связаны между собой в комплексы – зерна. Взаимное расположение зерен отдельных элементов и сплавов определяет структуру металлов и их свойства.
Атомы металлов характеризуются малым количеством электронов (1,2) на наружной оболочке, легко отдают их, что подтверждается высокой электропроводностью.
Черные металлы имеют простые кубические ячейки решеток (рис. 3) двух видов: а) центрированный или объемно-центрированный куб (9 атомов в ячейке), объем шаров занимает 68 %; б) гранецентрированный или куб с центрированными гранями (14 атомов), объем шаров занимает 74 %. Некоторые цветные металлы и их сплавы имеют гексагональную (шестигранную) решетку.
Железо, олово, титан и другие металлы обладают свойствами аллотропии,
т.е. способностью одного и того же химического элемента при различной температуре иметь разную кристаллическую структуру. Аллотропические превращения сопровождаются выделением или поглощением теплоты. Железо имеет четыре аллотропические формы: α-Fe; β-Fe, γ-
Fe
,
δ-Fe. Практическое значение имеют α -Fe и γ -Fe, так как p-Fe и б-Fe отличаются от a-Fe только величиной межатомного расстояния, а для β-Fe характерно отсутствие магнитных свойств.
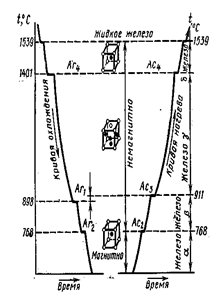
Рис.3-кривые охлаждения и нагревания железа.
Температура, при которой происходит переход металла из одного аллотропического вида в другой, называется критической. Величины этих температур видны на диаграмме охлаждения и нагревания чистого железа (рис. 3) в виде участков, свидетельствующих о том, что фазовые превращения происходят с выделением теплоты при нагревании.
Все металлы находятся в твердом состоянии до определенной температуры. При нагреве металла амплитуда колебания атомов достигает некоторой критической величины, при которой происходят разрушение кристаллической решетки и переход металлов из твердого в жидкое состояние. Процесс кристаллизации заключается в росте кристаллов путем отложения новых кристаллических групп вокруг возникших зародышей. Рост кристаллических образований происходит в определенных направлениях. Вначале образуются главные оси кристалла путем роста в трех взаимно перпендикулярных направлениях, а затем от каждой из этих осей образуются новые и возникает не полностью завершенный кристалл, называемый дендритом.
В дальнейшем все промежутки между осями дендрита заполняются упорядоченно расположенными атомами.
В условиях несвободной кристаллизации образующиеся кристаллы получают неправильные очертания и форму и называются кристаллитами или зернами. Величина зерен оказывает существенное влияние на механические свойства металлов: чем мельче зерна, тем прочнее металл.
Технические металлы и сплавы представляют собой поликристаллические тела, состоящие из большого числа различно ориентированных кристаллических зерен (поперечные размеры зерен – 0,001...0,1 мм). Поэтому в целом металлы и сплавы можно считать условно изотропными телами.
4 ОСНОВЫ ПОЛУЧЕНИЯ ЧУГУНА И СТАЛИ
Способы их промышленного получения многочисленны и разнообразны. Однако перед металлургией стоят две общие задачи: восстановление металла из его оксида или какого-либо другого соединения и отделение металла от других одновременно образующихся веществ.
4.1 Получение чугуна
4.1.1 Общие сведения
Чугунами называют железоуглеродистые сплавы, содержащие более 2 %. углерода. Чугун обладает более низкими механическими свойствами, чем сталь, но дешевле и хорошо отливается в изделия сложной формы. Различают несколько видов чугуна.
Белый чугун,
в котором весь углерод (2,0...3,8%) находится в связанном состоянии в виде Fe3
C (цементита), что и определяет его свойства: высокие твердость и хрупкость, хорошую сопротивляемость износу, плохую обрабатываемость режущими инструментами. Белый чугун применяют для получения серого и ковкого чугуна и стали.
Серый чугун
содержит углерод в связанном состоянии только частично (не более 0,5%). Остальной углерод находится в чугуне в свободном состоянии в виде графита. Графитовые включения делают цвет излома серым. Чем излом темнее, тем чугун мягче. Образование графита происходит в результате термической обработки белого чугуна, когда часть цементита распадается на мягкое пластичное железо и графит. В зависимости от преобладающей структуры различают серый чугун на перлитной, ферритной или ферритоперлитной основе.
Свойства серого чугуна зависят от режима охлаждения и наличия некоторых примесей. Например, чем больше кремния, тем больше выделяется графита, а потому чугун делается мягче. Серый чугун имеет умеренную твердость и легко обрабатывается режущими инструментами. Серый чугун, применяемый в строительстве, должен иметь предел прочности при растяжении не менее 120 МПа, а предел прочности при изгибе 280 МПа.
Из серого чугуна отливают элементы конструкций, хорошо работающие на сжатие: колонны, опорные подушки, башмаки, тюбинги, отопительные батареи, трубы водопроводные и канализационные, плиты для полов, станины и корпусные детали станков, головки и поршни двигателей, зубчатые колеса и другие детали.
Ковкий чугун
получают после длительного отжига %
белого чугуна при высоких температурах, когда цементит почти полностью распадается с выделением свободного углерода на ферритной или перлитной основе. Углеродные включения имеют округлую форму. В отличие от серых ковкие чугуны являются более прочными и пластичными и легче обрабатываются.
Высокопрочные (модифицированные) чугуны
значительно превосходят обычные серые по прочности и обладают некоторыми пластическими свойствами. Их применяют для отливок ответственных деталей.
При испытании серого и высокопрочного чугунов определяют предел прочности при растяжении, изгибе и сжатии, а при испытании ковкого чугуна – предел прочности при растяжении, относительное удлинение и твердость.
При маркировке серого и модифицированного чугуна, например СЧ12-28, первые две цифры обозначают предел прочности при растяжении, последующие две – предел прочности при изгибе. /2, стр. 325-326/
4.1.2 Основы получения
Чугун получают в ходе доменного производства, основанного на восстановлении железа из его природного оксидов, содержащихся в железных рудах, коксом при высокой температуре. Кокс, сгорая, образует углекислый газ. При прохождении через раскаленный кокс он превращается в оксид углерода, который и восстанавливает железо в верхней части печи по обобщенной схеме: Fe2
O3
→Fe3
O4
→FeO→Fe. Опускаясь в нижнюю горячую часть печи, железо плавится в соприкосновении с коксом и, частично растворяя его, превращается в чугун. В готовом чугуне содержится около 93% железа, до 5 % углерода и небольшое количество примесей кремния, марганца, фосфора, серы и некоторых других элементов, перешедших в чугун из пустой породы.
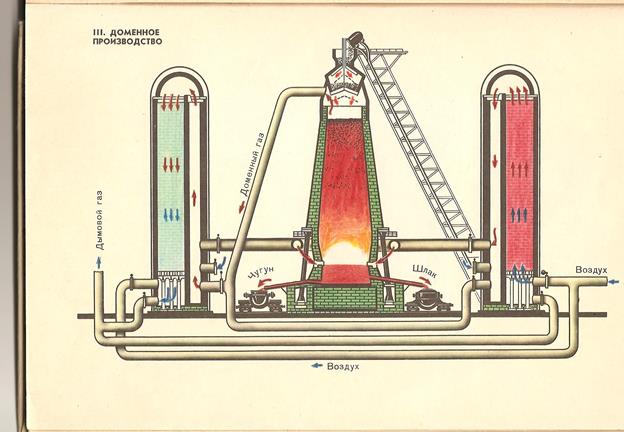
Рис.4-доменное производство.
4.2 ПРОИЗВОДСТВО СТАЛИ
4.2.1 Общие сведения о стали
Сталь углеродистая обыкновенного качества.
Решающее влияние на механические свойства в углеродистых сталях оказывает содержание углерода (рис. 5). При увеличении содержания углерода повышаются прочность, твердость и износоустойчивость, но понижаются пластичность и ударная вязкость, а также ухудшается свариваемость.
Примесь фосфора вызывает хладноломкость, а примесь серы – красноломкость стали. Для различных марок стали допустимое содержание фосфора 0,04...0,09 %, а серы 0.04..Д07 %. Вредное влияние на свойства стали оказывает кислород: содержание его более 0,03% вызывает старение стали, а более 0,1 % – красноломкость. Примеси марганца и кремния в количестве 0,8...1 % не оказывают практически влияния на механические свойства углеродистых сталей. В стали, предназначенной для сварных конструкций, содержание кремния не должно превышать 0,12...0,25 %. Содержание азота повышает прочность и твердость стали и снижает пластичность.
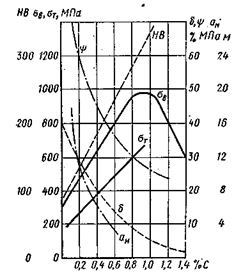
Рис.5-влияние углерода на механические свойства отожженных сталей.
При обозначении марок стали могут быть указаны: группы, по которым сталь поставляется («А» – по механическим свойствам, «Б» – по химическому составу, «B» – по механическим свойствам и дополнительным требованиям по химическому составу); методу производства («М» – мартеновский и др.); дополнительные индексы («сп» – спокойная сталь, «пс» – полуспокойная Сталь, «кп» – кипящая сталь). В группе «А» индекс «М» часто опускается, но имеется в виду сталь мартеновская, а при отсутствии индексов «сп», «пс», «кп» имеется в виду сталь спокойная.
Спокойная сталь является более качественной, но по стоимости она на 12...15 % дороже кипящей. Полуспокойная сталь занимает по свойствам промежуточное положение между спокойной и кипящей сталью, но в результате и незначительного расхода раскислителей стоимость ее меньше, чем спокойной.
Механические характеристики стали зависят также от формы и толщины проката. Углеродистые стали обыкновенного качества применяют без термообработки. В таблице 1 приведены нормы на механические свойства стали углеродистой обыкновенного качества (группа А).
Табл.1
Марки стали
группы А |
Предел прочности при растяжении, МПа |
Предел теку, чести, МПа |
Относительное
удлинение, % |
Ст0
Ст1сп, пс
Ст2сп, пс
Ст3сп, пс
Ст3Гпс
Ст4сп, пс
Ст5Гпс
Ст6сп, пс
|
310
320...420
340...440
380...490
380...500
420...540
460...600
Не менее 600
|
–
–
200...230
210...250
210...250
240...270
260...290
300...320
|
20...30
31…34
29...32
23...26
23...26
21...24
17...20
12…15
|
Примечание
: В стали марок Ст3Гпс и Ст5Гпс повышенное содержание марганца. /2, стр.318-320/
Сталь углеродистая качественная конструкционная.
Качественная конструкционная сталь выплавляется в мартеновских и электрических печах (спокойная, полуспокойная, кипящая).
В зависимости от химического состава эта сталь делится на две группы: I – с нормальным содержанием марганца и II – с повышенным содержанием марганца. Марки стали и требования к механическим свойствам стали I группы в состоянии нормализации приведены в таблице 2. В марке стали двузначные цифры означают среднее содержание углерода в сотых долях процента. Сталь в соответствии с требованиями может поставляться в термически обработанном состоянии (отожженная, нормализованная, высокоотпущенная).
Табл. 2
Сталь углеродистая качественная по ГОСТ 2050-74
| Марки стали |
Содержание
углерода, % |
Предел прочности при растяжении, МПа |
Предел текучести, МПа |
Относительное удлинение, % |
08 кп, пс
10 кп, пс
15 кп, пс
20 кп, пс
25 –
30 –
35 –
40 –
45 –
50 –
60 –
70 –
80 –
|
0,05...0,11
0,07...0,14
0,12...0,19
0,17...0,24
0,22...0,30
0,27...0,35
0,32...0,40
0,37...0,45
0,42...0,50
0,47...0,55
0,57...0,65
0,67...0,75
0,77...0,85
|
330
340
380
420
460
500
540
580
610
640
690
730
1100*
|
200
210
230
250
280
300
320
340
360
380
410
430
950*
|
35
31
27
25
23
21
20
19
16
14
12
9
6*
|
* Механические свойства после закалки и отпуска.
Примечание
: В таблице приведены только некоторые марки сталей.
Инструментальные качественные углеродистые стали предназначены для изготовления режущего, мерительного и штамповочного инструмента небольших размеров. Марки этих сталей обозначаются буквой У и цифрой, показывающей содержание углерода в десятых долях процента (У7, У8, У9,..., У13). Высококачественные стали имеют низкое содержание серы (до 0,02 %) и фосфора (до 0,03%), меньше неметаллических включений, обладают повышенными механическими свойствами. В обозначениях марок высококачественных сталей в отличие от качественных ставится буква А (например, У7А,У8Аит. д.). /2, стр.320-321/
Сталь легированная.
При введении в углеродистые стали специальных легирующих добавок (Cr, Mn, Ni, Si, W, Mo, Ti, Co, V и др.) достигается значительное улучшение их физико-механических свойств (например, повышение предела текучести без снижения пластичности и ударной вязкости и т.д.).
Легирующие добавки,
растворяясь в железе, искажают и нарушают симметрию его кристаллической решетки, так как они имеют другие атомные размеры и строение внешних электронных оболочек. Чаще всего увеличивается карбидосодержащая фаза за счет уменьшения углерода в перлите, что соответственно увеличивает прочность стали. Многие легирующие элементы способствуют измельчению зерен феррита и перлита в стали, что значительно повышает вязкость стали. Некоторые легирующие элементы расширяют область аустенита, снижая критические точки Ас3
, а другие, наоборот, сужают эту область. Большое значение на практике имеет способность большинства легирующих элементов повышать прокаливаемость, стали на значительную толщину, задерживая переход аустенита в другие структуры, что создает возможность закаливать стали при умеренных скоростях охлаждения. При этом уменьшаются внутренние напряжения, и снижается опасность появления закалочных трещин.
Согласно существующим стандартам легированные стали классифицируют по назначению, химическому составу и микроструктуре.
По назначению
легированные стали разделяют на три класса: конструкционные
(машиноподелочные и строительные), инструментальные
и стали с особыми физико-химическими свойствами.
Для обозначения марок сталей принята буквенно-цифровая система. Легирующие элементы обозначаются буквами: С – кремний, Г – марганец, X – хром, Н – никель, М – молибден, В – вольфрам, Р – бор, Т – титан, Ю – алюминий, Ф – ванадий, Ц – цирконий, Б – ниобий, А – азот, Д – медь, К – кобальт, П – фосфор и т.д. Цифры, стоящие перед буквами, показывают содержание углерода в конструкционных сталях в сотых долях процента, в инструментальных - в десятых долях процента. Цифры, стоящие за буквами, показывают содержание легирующих элементов в процентах. Если содержание элементов не превышает 1,5 %, то цифры не ставят. Буква А, стоящая в конце марки, означает, что сталь высококачественная. Например, сталь марки 35ХНЗМА – высококачественная, содержащая 0,3. % С, 1 % Сr, 3 % Ni, 1 % Mo.
По химическому составу
легированные стали делят на три класса: низколегированные с
общим содержанием легирующих элементов до 2,5 %; среднелегированные –
от 2,5 до 10% и высоколегированные,
содержащие более 10 % таких элементов, например нержавеющая сталь 1Х18Н9.
В зависимости от структуры,
которую получают легированные стали после нормализации, их делят на пять классов: перлитная, мартенситная, аустенитная, ферритная и карбидная
(ледебуритная). Большинство конструкционных и инструментальных сталей относится к сталям перлитного класса. Такие стали содержат незначительное количество легирующих элементов (не более 5...6 %), хорошо обрабатываются давлением и резанием.
После нормализации имеют структуру перлита (сорбита, троостита). После закалки и отпуска заметно повышают механические свойства.
Основным преимуществом легированных сталей по, сравнению со сталью марки СтЗ является их большая прочность при сохранении достаточно высокой пластичности и свариваемости, что позволяет повысить допускаемые напряжения и уменьшить расход металла на изготовление конструкций, а также повышенная стойкость к атмосферной коррозии. /2, стр. 321-323/
4.2.2 Основы получения стали
Конвертерный способ получения стали.
Этот способ позволяет использовать в качестве шихты жидкий чугун, до 50% металлического лома, руду, флюс (рис.6). Сжатый воздух под давлением (0,3…0,35 МПа) поступает через специальные отверстия. Теплота, необходимая для нагрева стали, получается за счет химических реакций окисления углерода и примесей, находящихся в чугуне.
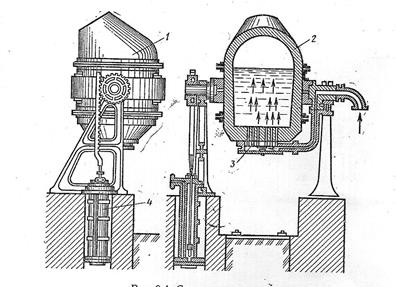
1-вращающийся грушевидный сосуд; 2-футеровка; 3-фурменные отверстия для подачи воздуха; 4-поворотные механизм. Рис.6
Особенностями конверторного способа производства стали являются: быстрота процесса, применение чугуна с минимальным содержанием фосфора и серы, трудность управления процессом, так как продолжительность плавки не превышает 15…25 мин, большой угар металла, повышенное содержание азота.
Производство стали в конверторах постепенно вытесняет ее в мартеновских печах. Емкость современных конверторов достигает 600т. Наибольшее развитие получает кислородно-конверторное производство стали, так как дополнительное использование кислорода обеспечивает резкое повышение производительности (на 25…30%), а также уменьшение содержания вредных примесей в стали, особенно азота, и увеличивает стойкость футеровки. Себестоимость конверторной стали на 3…5% ниже мартеновской, а производительность труда на 40% выше. Недостатки способа: повышенный расход огнеупоров и высокий угар металлов.
Мартеновский способ производства.
Мартеновский способ осуществляется в специальных мартеновских печах, в которых чугун сплавляется вместе с железной рудой и металлоломом (скрапом). Выгорание примесей происходит за счет кислорода воздуха, поступающего в печь вместе с горючими газами и железной рудой в составе оксидов. Состав стали хорошо поддается регулированию, чсто позволяет получать в мартеновских печах высококачественные стали для ответственных конструкций.
В мартеновских печах может быть произведена переплавка металлического лома(до 60…70%), возможны автоматизация процесса плавки, повышенная точность химического состава стали. Недостатки плавки стали в мартеновских печах: периодичность процесса плавки(одна плавка 8…12 ч), сложность оборудования, более высокая стоимость выплавляемой стали.
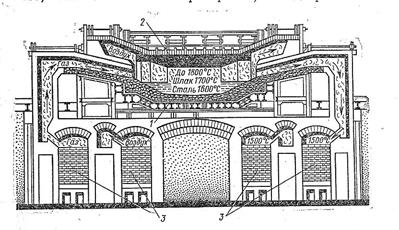
1-под; 2-свод; 3-регенераторы. Рис.7-схема мартеновской печи.
Электроплавление.
Производство стали в электрических печах - наиболее совершенный способ получения специальных и высококачественных видов сталей. Сталь выплавляют в дуговых или индукционных электропечах. Наиболее распространены дуговые электропечи емкостью до270 т (рис.8).
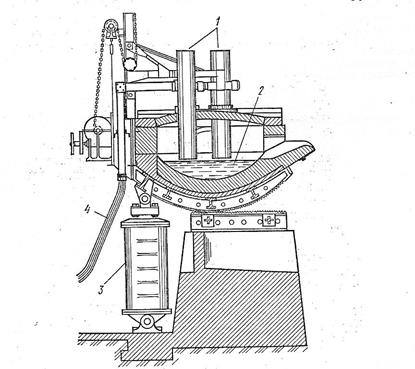
1-электроды; 2-ванна расплавленного металла; 3-поворотный механизм; 4-электропровод. Рис.8-схема дуговой электропечи.
При электроплавке стали используют как стальной скрап и железную руду, так и жидкие стали, поступающие из мартеновской печи или конвертера. В состав шихты вводят флюсы и легирующие добавки. Источником теплоты является электродуга, образующаяся между вертикально установленными угольными электродами и расплавленным металлом. Особенности производства стали в электропечах: восстановительная атмосфера, что способствует значительному сокращению угара стали и уменьшению расхода легирующих добавок; возможность достижения более высокой температуры, позволяющей получать специальные легированные стали; точное регулирование химического состава стали; более полно удаляются вредные примеси фосфора и серы. Применение электропечей пока ограничено достаточно высокой стоимостью электроэнергии.
Разливка стали
Выплавленную в печи сталь выпускают в ковши. Из ковшей сталь разливают в изложницы, где она кристаллизуется. Образовавшиеся слитки извлекают из изложниц, нагревают и прокатывают на обжимных станках (блюмингах, слябингах). Таким образом, переработка жидкой стали в заготовки складывается из многих операций, каждая из которых выполняется периодически и связана с большими затратами труда. При этом расходуется много топлива и теряется немало стали.
Разработан и широко применяется непрерывный способ получения заготовок. Жидкую сталь заливают из ковша в охлаждаемый водой кристаллизатор. Из нижней части его вытягивают заготовку. После затвердевания ее разрезают на куски желательной длины. Способ непрерывной разливки стали требует значительно меньших капиталовложений, чем периодический. Весь процесс ускоряется, качество стали повышается.
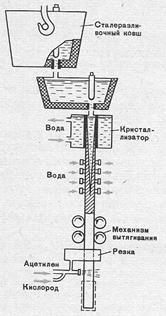
Рис.9-непревывная разливка стали.
5 МЕХАНИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
Механические свойства устанавливают по результатам статистических, динамических и усталостных (на выносливость) испытаний.
5.1 Статистические испытания
Статистические испытания характеризуются медленным и плавным приложением нагрузки. Основными из них являются: испытания на растяжение, твердость и вязкость разрушения.
Для испытания на растяжение используют стандартные образцы с расчетной длиной lp
=10d и площадью 11,3 Ао,
где d и Ао
– соответственно диаметр и площадь поперечног7о сечения образца сортового проката круглого, квадратного или прямоугольного сечения.
Испытания проводят на разрывных машинах с автоматической записью диаграммы растяжения. На рис. 10 представлена такая диаграмма для средне углеродистой стали.
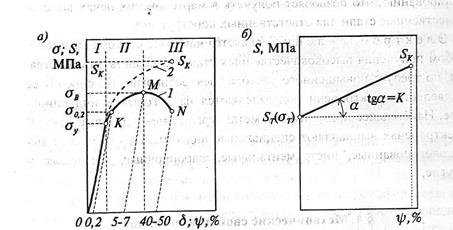
Диаграмма растяжения металла: а) для условных (сплошные линии) и истинных (штриховые линии) напряжений; I-область упругой деформации; II- то же пластической; III- область развития трещин; б) условно истинных напряжений. Рис.10
Кривая l характеризует поведение металла под действием условных напряжений,σ = Р/Ао
, а кривая 2 – под действием истинных напряжений, s = Р/Ах
, ( где Ао
и АХ
– соответственно площади поперечного сечения образца до испытания и на каждой ступени нагружения вплоть до разрушения). Обычно пользуются диаграммой условных напряжений. Хотя более объективной является кривая 2. Напряжение σу
( точка К на диграмме) характеризует предел пропорциональности. Его оценивают по отношению (tgαо
– tgα1
)/ tgαо
, которое не должно превышать 0,5 ( здесь αо
и α1
– соответственно углы наклона касательных к начальному участку диаграммы при линейной и нелинейной зависимости между напряжениями и деформациями).
Предел упругости определяют напряжением, при котором остаточная деформация удлинения не превышает 0,05%. Предел текучести характеризуется условным пределом текучести, σо,2
, при котором остаточная деформация не превышает 0,2%. Физический предел текучести, σт
соответствует напряжению, при котором образец деформируется без дальнейшего увеличения нагрузки. Напряжение σв
( точка М на диаграмме), отвечающее наибольшей нагрузке, предшествующей разрушению образца, называется временным сопротивлением (пределом прочности). Начиная с этого момента деформация локализуется на одном участке образца, напряжение падает и происходит разрушение ( точка N на диаграмме). Истинное сопротивление разрушению Sк
, как видно из диаграммы, больше σв
, что свидетельствует об упрочнении (наклепе) металла при испытании. Различие больше для пластичных и незначительно для хрупких металлов.Для высокоуглеродистых сталей Sт
=σт
и Sт
≈Sк
, так как хрупкие металлы почти не испытывают пластических деформаций. Sk
(Sт
) при хрупком разрушении характеризует сопротивление металлов отрыву. Для материалов хрупких при испытании на растяжение, применяют статистические испытания на сжатие (для чугуна), на кручение (для закаленных и конструкционных сталей) и изгиб (для отливок из серого и ковкого чугуна).
Пластические свойства металлов характеризуются относительным удлинением, δ=[(lk
-lo)/lo
] 100% и сужением, ψ=[(Ао
-АК
)/Ао
] 100%, где lo
,lK
и Ао,
Ак
– соответственно длина и площадь поперечного сечения образца до и после разрушения.
Твердость металлов испытывают путем вдавливания в него под определенной нагрузкой стального шарика, алмазного конуса или пирамиды (рис.11) и оценивают по величине произведенной пластической деформации (отпечатку). В зависимости от вида используемого наконечника и критерия оценки различают твердость по Бринеллю, Роквеллу и Виккерсу.
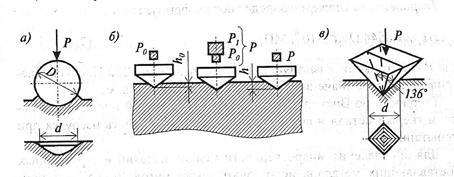
а) по Бринеллю; б)по Роквеллу; в) по Виккерсу.
Рис.11- схема определения твердости.
Твердость металлов по Бринеллю
рассчитывают по формуле:
НВ=2Р/πD (D-√ D2
-d2
)10-6
,МПа, (1)
Где Р- нагрузка, (Н); D- диаметр стального шарика, (м). В приборе принят D=1∙10-2
м; d диаметр отпечатка (лунки), (м).
При испытании значение Р принимают: для стали и чугуна - 3∙104
Н, меди и сплавов - 1∙104
Н, а очень мягких металлов (алюминия, баббита) – 2,5∙103
Н. Метод применим для металлов и сплавов с твердостью не более 4500 МПа, так как при большей твердости стальной шарик может деформироваться.
Твердость по Роквеллу
измеряют в условных единицах по формулам:
HR=100-e (при вдавливании алмазного конуса с углом при вышине 120о
), (2)
HR=130-e ( при вдавливании стального шарика, D=1,588∙10-3
м), (3)
где е = (h - ho
) /2∙10-6
, h – глубина внедрения наконечника (м), под действием общей нагрузки Р после снятия основной нагрузки Р1
, ho
– глубина внедрения наконечника под действием предварительной нагрузки Ро
, (м).
Предварительная нагрузка Ро
при испытаниях независимо от вида наконечника принята 100 Н; основная Р1
для стального шарика – 900 Н (шкала В), алмазного конуса – 1400 Н (шкала С) и 500 Н (шкала А). В соответствии с этим твердость по Роквеллу обозначается HRA, HRB, HRC. Метод широко применяется в промышленности, особенно для твердых и тонколистовых металлов и сплавов.
Твердость по Виккерсу
определяют по формуле:
HV=1, 8544 (P/d2
) ∙10-6
, МПа, (4)
где Р – нагрузка на алмазную пирамиду от 500 до 1200 Н; d – среднеарифметическое значение двух диагоналей отпечатка, м.
Твердость по Виккерсу обозначается HV5, HV10 и т.д. Чем тоньше и тверже металл и сплав, тем меньше должна быть нагрузка пи испытании.
Для определения микротвердости мелких изделий и структурных составляющих металлов используют также метод Виккерса в приборном сочетании с металлографическим микроскопом.
Испытание металлов на вязкость разрушения проводят на стандартных образцах с надрезом при трехточечном изгибе. Метод позволяет оценить сопротивление металла распространению, а не зарождению тещины или трещиноподобного дефекта любого происхождения, всегда имеющегося в металле. Вязкость разрушения оценивается параметром К, предоставляющим собой коэффициент интенсивности напряжений или локальное повышение растягивающих напряжений (МПа) в вершине трещины:
К=YσH
Πc (5)
Условие стабильного существования трещины без ее роста и развития будет К<К1С
, где К1С
– критический коэффициент интенсивности напряжений, определяемой при испытании образцов – балочек с надрезом на изгиб. Он характеризует трещиностойкость металла и является структурно-чувствительной характеристикой; уменьшается при понижении температуры, увеличении скорости приложения нагрузки и коррозии металла.
5.2 Динамические испытания
Динамические испытания металлов проводят на ударный изгиб и знакопеременное циклическое нагружение. На ударный изгиб испытывают образцы металла размерами (1х1х5,5)10-2
м с концентратом напряжения (надрезом) посередине. Испытание проводят на маятниковом копре. Сопротивление металла ударному изгибу называют ударной вязкостью и обозначают KCU, KCV и KCT (где KC – символ ударной вязкости, а U,V и T – вид и размер концентратора напряжения). Она представляет работу Q удара, отнесенную к начальной площади Ао
сечения образца в месте концентратора, т.е. KC=Q/Ao
, МДж/м2
. Ударная вязкость характеризует сопротивление металла хрупкому разрушению и используется для определения порога хладноломкости.
5.3 Усталостные (на выносливость) испытания
Сопротивление металла циклическому нагружению характеризуется максимальным напряжением, которое может выдержать металл без разрушения за заданное число циклов и называется пределом выносливости. Применяют симметричные и нессиметричные циклы нагружения. Предел выносливости резко снижается при наличии концентратов напряжений. Чувствительность к ним при симметричном цикле нагружения определяется эффективным коэффициентом напряжений Кэф
=σ-1
/σ-1
H
(где σ-1
и σ-1Н
– пределы выносливости образцов гладкого и снадрезом).
6 ВЛИЯНИЕ УГЛЕРОДА И ПОСТОЯННЫХ ПРИМЕСЕЙ НА СВОЙСТВА СТАЛЕЙ
Сталь является многокомпонентным сплавом, содержащим углерод и ряд постоянных примесей Mn, Si, S, P, O, H., N. После охлаждения сталь состоит из феррита и цеменита. От их соотношения зависят многие свойства стали. При содержании углерода в стали более 1…2% твердость ее возрастает, а временное сопротивление уменьшается, что объясняется выделением по границам бывшего зерна вторичного цеменита. Кремний и марганец присутствуют в стали в количестве соответственно 0,35…0,4%и 0,5…0,8%. Кремний повышает предел текучести и снижает способность стали к холодной деформации – высадке, штамповке. Марганец повышает прочность, не снижая пластичности, но уменьшает красноломкость, т.е. хрупкость при высоких температурах, вызванную серой. Последняя образует с железом эвтектику при 988о
С, по границам его зерен. При прокатке или ковке такой стали при 1000…1200о
С эвтектика между зернами расплавляется, связь между ними нарушается, вследствие чего в направлении деформирования появляются надрывы и трещины. Это явление называется красноломкостью. Сера, кроме того, снижает ударную вязкость и предел выносливости, ухудшает сваримость и коррозионную стойкость. Поэтому содержание серы ограничивается до 0,035…0,06%. Марганец обладает большим сродством к сере и образует с ней тугоплавкое соединение MnS, практически исключающее красноломкость.
Фосфор является вредной примесью в стали. Растворяясь в феррите, он сильно искажает кристаллическую решетку, повышает σВ
, σ0,2
и порог хладноломкости; уменьшает δ, ψ и KCT. Каждая 0,01% Р повышает порог хладноломкости стали на 20…25о
С. Содержание его в стали ограничивается до 0,025…0,08%.
Азот и кислород присутствуют в стали в виде хрупких включений FeO, SiO2
, Al2
O3
, Fe4
N, твердых растворов или в свободном состоянии в раковинах, трещинах и других дефектных участках металла. Концентрируясь по границам зерен в виде оксидов и нитридов, они повышают порог хладноломкости, уменьшают ударную вязкость и предел выносливости стали.
Особенно вреден растворенный в стали водород. Он не только охрупчивает ее, но и приводит к образованию в катаных заготовках и поковках тонких трещин – флокенов. В изломе они имеют вид хлопьев серебристого цвета. Флокены резко ухудшают свойства стали.
7 ЗАКЛЮЧЕНИЕ
Таким образом, важнейшая стадия металлургического производства – получение металла или сплава из его соединения разными методами. Для проведения этой стадии руду предварительно подготавливают, например крупнокусковые руды измельчают. Заключительная стадия ряда металлургических производств – обработка полученного металлов давлением или литьем, термическая обработка и т.д.
Металлургическая наука исследует все эти стадии производственного процесса. При этом она опирается на химию, физику, минералогию, геологию и другие естественные науки.
В настоящее время используют в машиностроении главным образом сплавы железа – стали. На их долю приходится более 90% общей массы применяемых металлов.
8 СПИСОК ЛИТЕРАТУРЫ
1. Технология металлов и сварка. Под ред. П.И. Полухина. М. Высшая школа. 1977.
2. Строительные материалы. А.Г. Домокеев. М. Высшая школа. 1989
3. Большая советская энциклопедия. Под ред. А.М. Прохорова. М. изд. «Советская энциклопедия». 1974.
4. Строительные материалы: Учеб/Под общ. Ред. В.Г.Микульского. – М.:Изд-во АСВ, 2000-536с.
|