| Зубная гранулема
Гранулема зубная (корневая) - ограниченный участок грануляционной ткани, расположенный, как правило, у верхушки корня зуба с омертвевшей пульпой. Зубная гранулема представляет собой проявление хронического воспаления, возникающего в тканях, окружающих верхушку корня, под влиянием проникания в них из корневого канала микроорганизмов и их токсинов, продуктов распада ткани пульпы и остатков пищи, а также пломбировочных материалов и медикаментов.
Зубная гранулема возникает в ткани перицемента—в области верхушечного отверстия—в виде круглоклеточного очага; зона клеточной пролиферации постепенно расширяется, захватывая новые участки перицемента и распространяясь также на костный мозг в области дна ячейки. Вследствие рассасывания костных балок, в области дна ячейки сначала образуется участок разрежения кости, а позже—лишенный костных перекладин очаг грануляционной ткани; другими словами, имеет место ограниченный рарифицирующий остит. Гранулема характеризуется неоднородностью гистологического строения и состоит из:
- грануляционной ткани, инфильтрированной клетками воспаления с различным соотношением лимфоцитов, макрофагов, сегментоядерных лейкоцитов, плазматических и эпителиоидных клеток. В грануляционной ткани присутствуют отдельные группы (тяжи) эпителиальных клеток, а также наблюдается пролиферация эндотелиальных клеток и ремоделирование сосудов. Характерным для гранулемы является наличие телец Русселя. Иногда встречаются ксантомные клетки, лежащие по отдельности либо небольшими группами, а также гигантские многоядерные клетки инородных тел.
- периферической волокнистой капсулы, чьи волокна непосредственно переходят в ткань перицемента, вследствие чего при экстракции корня нередко удаляется и гранулема. В составе капсулы содержится большое количество коллагеновых волокон, гистиоцитарных элементов и фибробластов. Сосудов в капсуле меньше, чем в грануляционной ткани.
Ткань собственно зубной гранулемы характеризуется обилием плазматических клеток, а также присутствием крупных макрофагов. Среди этих элементов расположены разнообразные клетки гистиогенного и гематогенного происхождения: в долго существующих гранулемах, в условиях затухшего воспалительного процесса, — преимущественно фиксированные элементы фибробластического ряда, а в случаях обострений воспаления—с преобладанием лейкоцитарной инфильтрации, нередко превращающей гранулему в абсцесс.
Кроме простых зубных гранулем, состоящих только из соединительнотканных элементов, различают эпителиальные гранулемы. Ткань, которых больше или меньше пронизана тяжами эпителия. И кистовидные гранулемы, характеризующиеся присутствием выстланных эпителием полостей.
В составе гранулем присутствуют тяжи эпителиальных клеток (в кистовидной гранулеме они более выражены). Их источником являются эпителиальные тельца (островки) Малассе — персистирующие остатки гертвиговского эпителиального влагалища, которые постоянно локализуются в интактной периодонтальной связке. Медиаторы, продуцируемые клетками очага хронического воспаления (например, интерлейкин-6 и эпидермальный фактор роста), стимулируют пролиферацию эпителиальных клеток. В последующем центрально расположенные клетки островков из-за резкого ухудшения условий обеспечения кислородом и питательными веществами погибают, в результате чего образуется полость, и кистовидная гранулема превращается в кисту.
Реклама

В результате регрессивных процессов в ткани гранулемы появляется белковый и жировой детрит. При распаде детрита выпадают кристаллы холестерина, являющиеся характерной составной частью содержимого полостей кистевидных гранулем и корневых кист. Эпителий в гранулемах построен по типу Мальпигиева слоя покровного эпителия полости рта; исключением является изредка находимый в гранулемах на верхней челюсти цилиндрический эпителий, появляющийся в результате воспалительного разрастания слизистой Гайморовой полости.
По вопросу о происхождении эпителия гранулем существуют две теории:
1) теория разрастания островков эмбрионального эпителия, залегающих в перицементе всех зубов;
2) теория разрастания покровного эпителия полости рта.
Наиболее обоснованной считается первая теория. При благоприятных условиях, создающихся в результате лечения корней, а иногда самопроизвольно, зубные гранулемы подвергаются обратному развитию. В порядке организации ткани зубной гранулемы происходит новообразование костных перекладин, и может иметь место восстановление нормальной архитектуры в области дна ячейки.
Эпителиальные и кистевидные гранулемы являются предварительными стадиями развития зубных кист.
Влияние зубной гранулемы на ткани зуба и пародонта
При обследовании выявляется обширный дефект стенки коронковой части пульпарной полости, что обеспечивает сообщение корневого канала с содержимым ротовой полости. В полости коронки зуба нередко определяются фрагменты клетчатки и значительное количество колоний микроорганизмов. Присутствие микроорганизмов отмечается также в расширенных дентинных канальцах.
Пульпа корневого канала в большей или меньшей степени некротизирована, подвержена резорбции и представляет собой мелкозернистый детрит с отдельными пучками соединительнотканных волокон. На всем протяжении канала выявляются колонии грамположительных микроорганизмов (кокков и палочек), иногда окруженные клетками воспаления. По мере приближения к отверстию верхушки корня зуба контаминация корневого канала микроорганизмами уменьшалась, а количество клеток воспалительной реакции (сегментоядерных лейкоцитов, макрофагов, лимфоцитов и плазмоцитов) увеличивалось. В частично сохранившейся пульпе наряду с фиброзом и воспалительной инфильтрацией отмечаются отек и локальное расширение кровеносных сосудов, характерное для хронического пульпита.
Реклама

В большинстве зубов в нижней трети корня обнаруживаются добавочные корневые каналы, количество и диаметр которых существенно варьировали. В отдельных добавочных каналах выявляются колонии микроорганизмов, расширенные тонкостенные сосуды и клетки воспаления.
Внутренние края стенки корневых каналов имеют признаки резорбции. Чаще вceго дефекты заполнены заместительным дентином, местами наблюдается образование дентиклей (рис. 2, а).
Нередко грануляционная ткань вместе с тяжами эпителиальных клеток врастает через верхушечное отверстие в корневой канал и вступает во взаимодействие с его содержимым (см. рис. 3, в). В одних случаях здесь выявляются продукты распада пульпы, колонии микроорганизмов, значительное количество полиморфно-ядерных лейкоцитов, в других преобладает созревающая грануляционная и фиброзная ткань, что может свидетельствовать о доминировании репаративных процессов.
В области хронического очага воспаления наблюдается резорбция твердых тканей зуба (цемента и дентина) различной степени выраженности. Резорбционные дефекты часто имеют вид лакун Хаушипа, вследствие чего поверхность корня зуба становится неровной. Иногда участки разрушенного цемента корня зуба полностью восстанавливаются новообразованной тканью (репаративным цементом). Выраженная резорбция характеризуется значительной убылью цемента и дентина, что приводит к укорочению корня и расширению апикального отверстия.
Персистирование очага хронического воспаления у корня зуба сопровождается признаками гиперпродукции цемента. Избыточные массы новообразованного цемента локализуются чаще всего в области верхушки корня зуба либо равномерно покрывают всю его поверхность. В многокорневых зубах в результате гиперцементоза между корнями формируются перемычки. В толще периодонтальной связки и на поверхности цемента выявляются цементикли.
Микроорганизмы хорошо выявляются на гистологических срезах на всем протяжении корневого канала в виде довольно крупных колоний. Вместе с тем морфологические признаки взаимодействия микроорганизмов с иммунной системой (отек, расширение кровеносных сосудов, воспалительная инфильтрация) наблюдаются преимущественно вблизи апикального отверстия. Этот факт свидетельствует о сохранении жизнеспособности пульпы даже при наличии значительных по размеру очагов хронического периапикального воспаления и подтверждается рядом исследователей.
Но в составе периапикальной гранулемы колонии микроорганизмов удается выявить очень редко. Подобные находки не часто описываются в литературе. Это можно объяснить тем, что за пределами апикального отверстия микроорганизмы доступны воздействию со стороны иммунной системы и быстро элиминируются. В корневом канале изначально практически изолированном от воздействия иммунной системы из-за разрушения нейрососудистых элементов пульпы, возможность подобного контакта становится весьма ограниченной. Кроме того, сама некротизированная пульпа служит благоприятной средой для роста колоний микроорганизмов. Следовательно, основной мишенью при лечении хронического апикального периодонтита должны стать микроорганизмы, локализующиеся внутри корневого канала
Чтобы инициировать выраженную воспалительную реакцию, микроорганизмы не обязательно должны выходить за пределы корневого канала. Липополисахариды и другие компоненты бактериальной стенки могут легко проникать из пульпарной полости в периапикальные ткани и вызывать иммунный ответ как непосредственно, так и через стимуляцию продукции цитокинов и молекул клеточной адгезии. Морфологически в составе периапикальной гранулемы принято выделять несколько концентрических зон: экссудативную, гранулематозную и фиброзную. В зависимости от преобладания той или иной зоны, выделяют: экссудативную, гранулематозную, гранулематозно-фиброзную и фиброзную гранулемы. Эти зоны в виде четко различимых концентрических колец в составе гранулемы выявляются редко. Чаще всего в толще грануляционной ткани участки с преобладанием лейкоцитарной или мононуклеарной инфильтрации располагаются беспорядочно.
Клиническая картина.
Течение гранулематозного периодонтита бывает различным. Нередко гранулема долго не увеличивается или растет крайне медленно. При этом больные часто не предъявляют жалоб. Лишь случайно при рентгенологическом исследовании обнаруживают гранулематозный очаг. Гранулемы, так же как и очаги хронического гранулирующего периодонтита, нередко располагаются не у самой верхушки корня зуба, а несколько сбоку. При этом на поверхности альвеолярного отростка соответственно проекции верхушки корня в результате происходящей перестройки костной ткани и явлений оссифицируюшего периостита можно выявить небольшое безболезненное выбухание без четких границ.
У некоторых больных гранулема постепенно увеличивается. Обычно это связано с обострениями воспалительного процесса и соответствующими изменениями в ткани гранулемы (гиперемия, отек, увеличение количества нейтрофильных лейкоцитов, абсцедирование). При обострении хронического процесса нарушается целость капсулы гранулемы, а в окружающих тканях возникают реактивные воспалительные и дистрофические процессы с преобладанием резорбции прилежащих участков стенок зубной альвеолы. Клинически эти обострения проявляются различно. В одних случаях появляется некоторая чувствительность, а иногда и болезненность при перкуссии и надавливании на зуб, а в других - явления острого периодонтита. В дальнейшем по мере стихания воспаления в окружности, увеличившегося околоверхушечного воспалительного очага вновь образуется капсула.
Лечение и диагностика заболевания
Диагностика основывается на клинической картине, но обычно диагноз зубной гранулемы ставится на основании рентгенограммы, дающей картину упомянутого выше ограниченного периапикального (у верхушки корня) рарифицирующего остита. На рентгенограмме при гранулематозном периодонтите в околоверхушечной области виден округлый очаг разрежения костной ткани с четкими ровными границами.
Присутствие микроорганизмов в корневом канале является ведущим фактором развития воспалительного процесса и его персистирования в периапикальных тканях. В связи с этим основополагающими принципами консервативного лечения хронического апикального периодонтита (первичной эндодонтической инфекции) являются:
— обязательное максимальное обеспечение асептики в пределах операционного поля (за счет наложения коффердама, использования стерильного инструмента и т.д.);
— исключение искусственного выведения микроорганизмов за пределы апикального отверстия на этапе химико-механической обработки корневого канала; при этом следует отдавать предпочтение методикам обработки канала вращающимся инструментом по принципу «от коронки к апексу» с обильным орошением антисептиком под контролем апекслокатора;
— предотвращение повторного поступления микроорганизмов в корневой канал из ротовой полости, чему способствуют: удаление всех измененных тканей из коронковой части полости зуба до начала обработки корневого канала; контроль герметичности изоляции коффердамом; закрытие доступа в полость зуба на этапах лечения цементами.
Но консервативный метод лечения принято считать не надежным, поэтому в клинике чаще используют хирургический метод лечения - операция резекции верхушки корня, удаляемой вместе с зубной гранулемой.
Литература:
- Абрикосов А., Патологическая анатомия полости рта и зубов1914;
- Рывкинд А. Патологическая гистология зубных гранулем;
- Журнал одонтологии и стоматологии, 1924, № 1—2;
- Рывкинд А. и Данилевский А., Патология и клиника хронического апикального парадонтита 1928;
- Лукомский И. Одонтогенные опухоли, М., 1927;
- Быков В.Л. Эпителиальные остатки Малассе: тканевая, клеточная и молекулярная биология. Морфология 2003;124:4:95—103.
- Лукиных Л.М., Лившиц Ю.Н. Верхушечный периодонтит. Учебное пособие. Н. Новгород: Изд-во НГМА 1999;92.
- Международная статистическая классификация болезней и проблем, связанным со здоровьем: МКБ-10. В 3 т. Минск: ИнтерДайджест 2000;1:1:704.
- Abbott P.V. Assessing restored teeth with pulp and periapical diseases for the presence of cracks, caries and marginal breakdown. Aust Dental J 2004;49:3:33—39.
- Laux M. et al. Apical inflammatory root resorption: a correlative radiographic and histological assessment. Int Endod J 2000;33:6:483—493.
- Bergenholtz G., Spдngberg L. Controversies in endodontics. Crit Rev Oral Biol Med 2004;15:2:99—114.
- Ricucci D. et al. Epithelium and bacteria in periapical lesions. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2006;101:2:239—249.
- Nickolaychuck B. et al. Evidence for a role of mitogen-activated kinases in proliferating and differentiating odontogenic epithelia of inflammatory and developmental cysts. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2002;93:6:720—729.
- Fouad A.F., Walton R.E., Rittman B.R. Induced periapical lesions in ferret canines: histologic and radiographic evaluation. Endod Dent Traumatol 1992;8:2:56—62.

Рисунок 1. Эпителиальная гранулема: 1 расщепление эпителиального тяжа и образование щелевидной полости: 2 тяжи эпителиальной ткани; 3 островки грануляционной ткани.
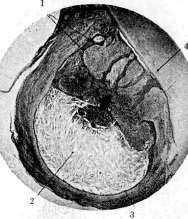
Рисунок 2. Кистовидная гранулема: 1 тяжи эпителия; 2 полость гранулемы, в содержимом которой находится большое количество кристаллов холестерина; 3 эпителиальная выстилка полости; 4 корень зуба.

Рисунок 3. Зубная гранулема in situ (трупный материал): 1 перицемент; 2 костные стенки альвеолы; 3 -фиброзная капсула гранулемы, переходящая в перицемент (вследствие наличия гранулемы и рассасывания костной ткани в области дна альвеолы в периапикальном губчатом костном веществе образовалось лишенное костных балок пространство, выполненное тканью гранулемы); 4 -гранулема; 5- корень зуба.
|