Качественный анализ и экспериментальные задачи на распознавание основных классов неорганических веществ
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
Глава I. ХИМИЧЕСКИЙ ЭКСПЕРИМЕНТ КАК ИСТОЧНИК ПОЗНАНИЯ И СРЕДСТВО ВОСПИТАНИЯ
ГЛАВА II. МЕТОДИКА ПРЕПОДАВАНИЯ ТЕМЫ “ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ” В СОВРЕМЕННОЙ ШКОЛЕ
2.1.1 Оксиды
2.1.2 Основания
2.1.3 Кислоты
2.1.4 Соли
ГЛАВА III. МОИ УРОКИ
ГЛАВА IV. ТЕСТЫ И ЗАДАЧИ ПО ТЕМЕ «КАЧЕСТВЕННЫЙ АНАЛИЗ»
ЛИТЕРАТУРА
Введение
Химия изучает состав, свойства и превращения веществ, а также явления, сопровождающие эти превращения. Объектом изучения химии являются вещества, которые подразделяются на простые и сложные. Простых веществ известно более 400, а сложных веществ - намного больше: несколько сот тысяч, относящихся к неорганическим. Из всего многообразия неорганических веществ выделяют оксиды, кислоты, основания и соли, которые характеризуются своими особенностями. Важная задача - уметь распознавать эти вещества, что является предметом качественного анализа. Поэтому цель моей работы - рассмотреть качественные реакции основных классов неорганических веществ и экспериментальное решение задач по данной теме.
Глава I. Химический эксперимент как источник познания и средство воспитания
При изучении химии важную роль играет химический эксперимент – составная часть учебного процесса [1].
Экспериментальный характер химии проявляется прежде всего в том, что каждое научное понятие должно логически вытекать из поставленной задачи и обосновываться практически. Познание начинается с ощущения и восприятия конкретных предметов, явлений, процессов, фактов и переходит затем к обобщению и абстрагированию. Химическое понятие – это обобщенные знания о существенных признаках химических явлений и процессов, которые формируются на основе их восприятия. Их анализ дает возможность найти существенные, присущие им всем черты и на этой основе установить химические закономерности. Используя различные виды химического эксперимента, преподаватель учит конкретизировать теоретические знания, находить общее в единичном, конкретном. Химический эксперимент помогает учащимся наполнить усваиваемые ими химические понятия живым, конкретным содержанием, увидеть в отдельных фактах общие закономерности.
Реклама

Химический эксперимент проводится в несколько этапов:
первый
– обоснование постановки опыта,
второй – планирование и проведение,
третий – оценка полученных результатов.
Выполнять эксперимент возможно лишь с опорой на полученные ранее знания. Теоретическое обоснование опыта способствует его восприятию, которое становится более целенаправленным и активным, и осмыслению его сущности. Проведение эксперимента обычно связано с выдвижением гипотезы. Привлечение к этой работе учащихся развивает их мышление, заставляет применять имеющиеся знания для формулировки гипотезы, а в результате ее проверки ребята получают новые знания.
Химический эксперимент может выполнять различные дидактические функции, использоваться в различных формах и сочетаться с разными методами и средствами обучения. Он представляет собой систему, в которой используется принцип постепенного повышения самостоятельности учащихся: от демонстрации явлений через проведение фронтальных лабораторных опытов под руководством преподавателя к самостоятельной работе при выполнении практических занятий и решении экспериментальных задач.
Проведение демонстраций позволяет познакомить учеников с различными химическими явлениями и связями между ними, обобщение которых может быть положено в основу закона, теоретического вывода; с устройством и принципом действия приборов и установок; с сущностью протекающих в них процессов, которые могут выступать в качестве критериев правильности выводов. У школьников формируются экспериментальные умения и навыки в обращении с реактивами и оборудованием. Все это способствует улучшению теоретических знаний и политехнической подготовке учащихся.
Решая экспериментальные задачи, ученики совершенствуют свои умения и навыки, учатся применять полученные теоретические знания для решения конкретных заданий. Наблюдение как метод познания широко используется при проведении химического эксперимента. Деятельность учащихся становится целенаправленной и приобретает активную форму при условии четкой постановки задачи и разработки методики ее решения. Например, если ребята наблюдают электролиз сульфата меди(II), то главное – следить за изменением окраски раствора соли и появлением красного налета на одном угольном электроде и пузырьков газа возле другого. Результаты наблюдений школьники интерпретируют с учетом имеющихся теоретических знаний.
Эксперимент должен стать необходимой частью урока при изучении конкретных вопросов. Ученики должны знать, для чего проводить эксперимент, какое теоретическое положение он подтверждает, на какой вопрос поможет ответить. Например, при объяснении химических свойств металлов преподаватель выносит на обсуждение вопрос: «Все ли металлы взаимодействуют с водой?» После демонстрации преподавателем опытов дети самостоятельно делают вывод: металлы, стоящие в ряду напряжений правее водорода, с водой не взаимодействуют [2].
Реклама

Предварительная подготовка теоретического материала к предстоящей практической работе повышает интерес к последней, а это значит, что ребята будут активными и дисциплинированными во время занятия. Осмысленное понимание сущности опытов, а также аккуратное оформление выполненных работ положительно влияют на поведение учащихся во время выполнения опытов. Необходимо добиваться выполнения практических работ и получения нужных результатов всеми учениками, чтобы они почувствовали уверенность в своих силах и стремились преодолеть трудности. Систематическое использование на уроках химии эксперимента помогает бороться с формализмом в знаниях, развивает умения наблюдать факты и явления и объяснять их сущность в свете изученных теорий и законов; формирует и совершенствует экспериментальные умения и навыки; прививает навыки планировать свою работу и осуществлять самоконтроль; воспитывает уважение и любовь к труду. Эта работа способствует общему воспитанию, всестороннему развитию личности, готовит к деятельности на современном производстве [2,3].
Глава II. МЕТОДИКА ПРЕПОДАВАНИЯ ТЕМЫ “ОСНОВНЫЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ” В СОВРЕМЕННОЙ ШКОЛЕ
Тема: «Основные классы неорганических соединений» в школьных программах по химии
Вещества классифицируются на простые и сложные, которые в свою очередь классифицируются на чистые вещества и соединения. К основным классам неорганических соединений относятся оксиды, кислоты, основания, соли. В школьном курсе химии данная тема рассматривается следующим образом:
Основные классы неорганических соединений. (14 часов)
Оксиды, классификация, взаимодействие с водой, кислотами и щелочами. Взаимодействие между кислотными и основными оксидами.
Кислоты – классификация, взаимодействие с металлами, основными оксидами, основаниями и солями. Понятие о ряде напряжений металлов.
Основания – классификация, взаимодействие щелочей с кислотными оксидами, кислотами и солями. Разложение нерастворимых в воде оснований при нагревании.
Амфотерные оксиды и гидроксиды.
Реакция нейтрализации. Кислотно-основные индикаторы.
Соли – реакции с кислотами, щелочами и другими солями. Понятие о кислых и основных солях.
Условия, при которых реакция обмена протекает до конца.
Генетическая связь между основными классами неорганических соединений.
Лабораторные опыты
1. Химические свойства основных и кислотных оксидов.
2. Условия необратимого протекания реакций обмена.
3. Химические свойства кислот и оснований.
4. Получение осадков нерастворимых гидроксидов и изучение их свойств.
5. Получение амфотерного гидроксида и изучение его свойств.
6. Нейтрализация щелочи кислотой в присутствии фенолфталеина.
Практические работы
1. Генетическая связь между основными классами неорганических соединений (выполнение цепочки химических превращений).
Демонстрационные опыты
1. Знакомство с образцами оксидов.
2. Химические свойства растворов кислот, солей и щелочей. Реакция нейтрализации.
Осаждение и растворение осадков солей и нерастворимых гидрооксидов [4].
2.1.1 Оксиды
Оксиды
_ - это соединения элементов с кислородом. По химическим свойствам они подразделяются на солеобразующие и несолеобразующие. Солеобразующие оксиды в свою очередь подразделяются на основные, кислотные и амфотерные. Основным оксидам отвечают основания, кислотным - кислоты. Амфотерным оксидам отвечают гидраты, проявляющие и кислотные, и основные свойства.


+2 +2 +4 +4
CаО Са(ОН)2
SO2
H2
SO3
Примерами основных оксидов могут служить оксид кальция СаО и оксид магния MgO. Оксид кальция взаимодействует с водой, образуя гидро-ксид кальция Са(ОН)2:
СаО + Н2О = Са(ОН)2.
Оксид магния малорастворим в воде; однако ему соответствует основание - гидроксид магния Mg(OH)2, который можно получить из оксида магния косвенным путем.
Примерами кислотных оксидов могут служить триоксид серы SO3 и диоксид кремния SiO2. Первый из них взаимодействует с водой, образуя серную кислоту H2SO4:
SO3 + Н2О = H2SO4.
Диоксид кремния с водой не взаимодействует, но ему соответствует кремниевая кислота H2SiО3, которую можно получить из SiO2 косвенным путем. Кислотные оксиды можно получить из кислот, отнимая от них воду. Поэтому их называют также ангидридами кислот или просто ангидридами.
К несолеобразующим оксидам относится, например, оксид азота (I) N2О. Нет такой кислоты или основания, которые отвечали бы этому оксиду.
Существуют различные номенклатуры оксидов. До сих пор в промышленности могут использоваться устаревшие термины русской номенклатуры. Согласно международной номенклатуре (которой пользуются в настоящее время и отечественные химики) все соединения элементов с кислородом (за исключением пероксидов) называются оксидами. При этом для элементов переменной валентности в скобках римскими цифрами указывается валентность, которую элемент проявляет в данном оксиде. Так, СаО называется оксид кальция, а Сu2О и СuО - оксид меди (I), оксид меди (II). По отечественной номенклатуре оксиды состава ЭО2 или ЭО3 называют также, соответственно, диоксидами и триоксидами. Согласно устаревшей отечественной номенклатуре, если элемент образует только один оксид, то последний назывался окисью. Так, СаО назывался окисью кальция. Если существует два или несколько оксидов данного элемента, то их названия образовывались в соответствии с числом атомов кислорода, приходящихся на один атом элемента, например: Э2О - полуокись, ЭО - одноокись, Э2О3 - полутораокись, ЭО2 - двуокись, Э2О5 - полупятиокись, ЭО3 - трехокись (символом Э здесь обозначен атом соответствующего элемента). Так, FeO -одноокись железа, Fe2O3 - полутораокись железа, Сu2О - полуокись меди, СuО - одноокись меди. Иногда оксиды, в которых элемент проявляет низшую валентность, назывались закисями (Сu2О - закись меди, N2O - закись азота), а кислотные оксиды - ангидридами соответствующих кислот (N2O5 -азотный ангидрид, Мn2O7 - марганцовый ангидрид). Существуют вещества - соединения элементов с кислородом - лишь формально принадлежащие к классу оксидов. К таким веществам относятся, в частности, пероксиды (перекиси) металлов, например, пероксид (перекись) бария ВаО2. По своей природе подобные вещества представляют собой соли очень слабой кислоты - пероксида (перекиси) водорода Н2О2.
2.1.2 Основания
Основания состоят из металла и одновалентных гидроксогрупп ОН, число которых равно валентности металла. Примерами оснований могут служить гидроксид натрия NaOH, гидроксид меди Сu(ОН)2. Важнейшее химическое свойство оснований - способность образовывать с кислотами соли. Например, при взаимодействии перечисленных оснований с соляной кислотой получаются хлористые соли соответствующих металлов - хлориды натрия или меди:
NaOH + НС1 = NaCl + Н2О; Cu(OH)2 + 2НС1 = CuCl2 + 2Н2О.
Основания классифицируют по их растворимости в воде и по их силе. По растворимости основания делятся на растворимые, или щелочи, и на нерастворимые. Важнейшие щелочи - это гидроксиды натрия, калия и кальция. По силе основания делятся на сильные и слабые. К сильным относятся все щелочи, кроме гидроксида аммония. Согласно международной номенклатуре соединения, содержащие в своем составе гидроксогруппы, называют гидроксидами. В случае металлов переменной валентности в скобках указывают валентность металла в данном соединении. Так, Са(ОН)2 - гидроксид кальция, Fe(OH)2 - гидроксид железа (II), Fe(OH)3 - гидроксид железа (III).
В устаревшей русской номенклатуре названия оснований обычно образовывались, прибавлением к названию соответствующего оксида приставку гидро- или слово гидрат. Так, Са(ОН)2 - гидроокись кальция, Fe(OH)2 - гидрат закиси железа, Fe(OH)3 - гидроокись или гидрат окиси железа.
2.1.3 Кислоты
Кислоты состоят из водорода, способного замещаться металлом, и кислотного остатка, причем число атомов водорода равно валентности кислотного остатка. Примерами кислот могут служить соляная (хлористоводородная) НСl, серная H2SO4, азотная HNO3, уксусная СН3СООН. Важнейшее химическое свойство кислот - их способность образовывать соли с основаниями. Например, при взаимодействии кислот c гидроксидом натрия получаются натриевые соли этих кислот:
2NaOH + H2SO4 = Na2SO4 + 2H2O; NaOH + HNO3 = NaNO3 + H2O.
Кислоты классифицируются по их силе, по основности и по наличию кислорода в составе кислоты. По силе кислоты делятся на сильные и слабые. Важнейшие сильные кислоты - это азотная, серная и соляная.
Основностью кислоты называется число атомов водорода в молекуле кислоты, способных замещаться на металл с образованием соли. Такие кислоты, как соляная и уксусная, могут служить примерами одноосновных кислот, серная кислота - двухосновна, ортофосфорная кислота Н3РО4 - трехосновна.
По наличию кислорода в своем составе кислоты делятся на кислородсодержащие и бескислородные. Азотная и серная кислоты - кислородсодержащие кислоты, соляная кислота и сероводород - бескислородные.
Названия кислот производят от того элемента, от которого образована кислота. При этом названия бескислородных кислот имеют окончание водородная: НСl - хлороводородная (соляная кислота), H2S - сероводородная, HCN - циановодородная (синильная кислота). Названия кислородсодержащих кислот также образуются от названия соответствующего элемента с добавлением слова кислота: HNO3 - азотная, Н2CrO4 - хромовая. Если элемент образует несколько кислот, то различие между ними отражается в окончаниях их названий. Название кислоты, в которой элемент проявляет высшую валентность, оканчивается на ная или овая; если же валентность элемента ниже максимальной, то название кислоты оканчивается на истая или овистая. Например, НNO3 - азотная кислота, HNO2 - азотистая, Н3AsO4 - мышьяковая, H3AsO3- мышьяковистая. Кроме того, одному и тому же оксиду могут отвечать несколько кислот, различающихся между собой числом молекул воды. При этом наиболее богатая водой форма имеет приставку орто, а наименее богатая - мета. Так, кислота Н3РО4, в которой на одну молекулу фосфорного ангидрида Р2О5 приходится три молекулы воды, называется ортофосфорная, а кислота НРО3 - метафосфорная, так как в ней на одну молекулу Р2О5 приходится одна молекула воды. Указанная номенклатура кислот не строга. Наряду с приведенными окончаниями и приставками употребляются и другие. Кроме того, ряд кислот имеют исторически сложившиеся названия.
2.1.4 Соли
Со́ли
— класс химических соединений, кристаллические вещества, имеющие ионную структуру. При диссоциации в водных растворах соли дают положительно заряженные ионыметаллов и отрицательно заряженные ионы кислотных остатков (иногда также ионы водорода или гидроксогруппы). В зависимости от соотношения количеств кислоты и основания в реакциях нейтрализации могут образоваться различные по составу соли.
Типы солей
Средние (нормальные) соли — все атомы водорода в молекулах кислот замещены на атомы металла. Пример: Na2
CO3
, K3
PO4
.
Кислые соли — атомы водорода в молекулах кислоты замещены атомами металла частично. Получаются они при нейтрализации основания избытком кислоты. Пример: NaHCO3
, K2
HPO4
.
Основные соли — гидроксогруппы основания (OH-
) частично заменены кислотными остатками. Получаются при избытке основания. Пример: Mg(OH)Cl.
Двойные соли — образуются при замещении атомов водорода в кислоте атомами двух разных металлов. Пример:
CaCO3
·MgCO3
, Na2
KPO4
.
Смешанные соли — в их составе один катион и два аниона. Пример: Ca(OCl)Cl.
Гидратные соли (кристаллогидраты) — в их состав входят молекулы кристаллизационной воды. Пример:
CuSO4
·5H2
O.
Комплексные соли — особый класс солей. Это сложные вещества, в структуре которых выделяют координационную сферу, состоящую их комплексообразователя (центральной частицы) и окружающих его лигандов. Пример:
K2
[Zn(OH)4
], [Cr(H2
O)6
]Cl3
, [Ni(NH3
)6
](NO3
)2
.
Особую группу составляют соли органических кислот, свойства которых значительно отличаются от свойств минеральных солей.
Нахождение в природе
Многие минералы — соли, образующие залежи (например, галит NaCl, сильвин KCl, флюорит CaF2
).
Номенклатура
Названия солей образуются из двух слов: название аниона в именительном падеже и название катиона в родительном падеже: Na2
SO4
— сульфат натрия. Для металлов с переменной степенью окисления её указывают в скобках: FeSO4
— сульфат железа (II), Fe2
(SO4
)3
— сульфат железа (III).
Названия кислых солей начинаются с приставки «гидро-» (если замещён один атом водорода) или «дигидро-» (если замещены два атома водорода). Например, NaHCO3
— гидрокарбонат натрия, NaH2
PO4
— дигидрофосфат натрия.
Названия основных солей начинаются с приставки «гидроксо-» или «дигидроксо-». Например, Mg(OH)Cl — гидроксохлорид магния, Al(OH)2
Cl — дигидроксохлорид алюминия.
В гидратных солях на наличие кристаллической воды указывает приставка «гидрат-». Степень гидратации отражают численной приставкой. Например, CaCl2
·2H2
O — дигидрат хлорида кальция.
На низшую степень окисления кислотообразующего элемента (если их больше двух) указывает приставка «гипо-». Приставка «пер-» указывает на высшую степень окисления (для солей кислот с окончаниями «-овая», «-евая», «-ная»). Например: NaOCl — гипохлорит натрия, NaClO2
— хлорит натрия, NaClO3
— хлорат натрия, NaClO4
— перхлорат натрия.
Названия комплексных солей составляются аналогично названиям обычных солей, только с указанием лигандов и степени окисления центрального иона. Пример: [Cr(H2
O)6
]Cl3
— хлорид гексааквахрома (III), K2
[Zn(OH)4
] — тетрагидроксоцинкат (II) калия.
Методы получения
Существуют различные методы получения солей:
Взаимодействие кислот с металлами, основными и амфотерными оксидами и гидроксидами.
H2
SO4
+ Mg → MgSO4
+ H2
↑;
H2
SO4
+ CuO → CuSO4
+ H2
O;
HCl + Mg(OH)2(
изб
.)
→ Mg(OH)Cl + H2
O;
NaOH + 2KOH + H3
PO4
→ K2
NaPO4
+ 3H2
O.
Взаимодействие кислотных оксидов со щелочами, основными и амфотерными оксидами.
SiO2
+ CaO → CaSiO3
;
Ca(OH)2
+ CO2
→ CaCO3
↓ + H2
O.
Взаимодействие солей с кислотами, щелочами, металлами, другими солями и нелетучими кислотными оксидами (если образуется выходящий из сферы реакции продукт).
CaCO3
+ 2HCl → CaCl2
+ H2
O + CO2
↑;
CuSO4
+ Fe → FeSO4
+ Cu↓;
CuCl2
+ Na2
S → 2NaCl + CuS↓;
2Na2
CO3
+ 2MgCl2
+ H2
O → [Mg(OH)]2
CO3
+ CO2
↑ + 4NaCl.
Взаимодействие металлов с неметаллами.
Fe + S → FeS.
Взаимодействие оснований с неметаллами.
Ca(OH)2
+ Cl2
→ Ca(OCl)Cl + H2
O.
Химические свойства
Химические свойства определяются свойствами катионов и анионов, входящих в их состав.
Соли взаимодействуют с кислотами, оксидами и основаниями, если в результате реакции получается продукт, который выходит из сферы реакции (осадок, газ, мало диссоциирующие вещества, например, вода):
BaCl2
+ H2
SO4
→ BaSO4
↓ + 2HCl;
NaHCO3
+ HCl → NaCl + H2
O + CO2
↑;
Na2
SiO3
+ 2HCl → 2NaCl + H2
SiO3
↓.
Соли взаимодействуют с металлами, если свободный металл находится левее металла в составе соли в ряду напряжений:
Cu + HgCl2
→ CuCl2
+ Hg.
Соли взаимодействуют между собой, если продукт реакции выходит из сферы реакции; в том числе эти реакции могут проходить с изменением степеней окисления атомов реагентов:
CaCl2
+ Na2
CO3
→ CaCO3
↓ + 2NaCl;
AgNO3
+ NaCl → AgCl↓ + NaNO3
;
K2
Cr2
O7
+ 3Na2
SO3
+ 4H2
SO4
→ Cr2
(SO4
)3
+ 3Na2
SO4
+ K2
SO4
+ 4H2
O.
Некоторые соли разлагаются при нагревании:
CuCO3
→ CuO + CO2
↑;
NH4
NO3
→ N2
O↑ + 2H2
O;
NH4
NO2
→ N2
↑ + 2H2
O.
Практическое занятие № 1
Тема.
Определение качественного состава неорганических веществ.
Цель:
сформировать у учащихся методический подход к качественному анализу неорганических веществ.
Ход работы
Задания для самостоятельной работы
В четырех пробирках находятся растворы следующих солей: сульфат меди (II), хлорид меди (II), иодид калия, хлорид бария. Как определить, в какой пробирке находится каждый из растворов, не используя дополнительные реактивы? Составьте схему исследования, напишите уравнения всех возможных реакций.
| CuSO4
|
CuCl2
|
KI |
BaCl2
|
| CuSO4
|
Белый осадок |
| CuCl2
|
| KI |
| BaCl2
|
Напишите уравнения всех возможных реакций, которые будут протекать при смешивании реактивов.
Сделайте выводы по проделанной работе.
Лабораторный опыт «Распознование сульфат-ионов в растворе»
Учащимся предлагают с помощью раствора хлорида бария провести анализ пробы воды, взятой из сточных вод местного предприятия, или заранее приготовленного раствора соответствующего состава на присутствие сульфат-ионов. Для этого исследуемый раствор подкисляют разбавленной соляной кислотой и добавляют к нему по каплям реактив. При наличии сульфат-ионов выпадает белый осадок сульфата бария. По окончании исследования учащимся предлагают с помощью таблицы растворимости найти еще несколько реактивов на сульфат-ионы и самостоятельно провести исследования
Урок – практикум «Качественное определение карбонатов».
Цель:
формирование умения у учащихся распознавать соли угольной кислоты –
карбонаты.
Задачи:
1) совершенствовать практические навыки при выполнении
лабораторного опыта, умение наблюдать, анализировать, делать выводы;
2) формировать положительное отношение к учебе, повышая самооценку
учащихся через индивидуализацию учебного процесса;
3) развитие творческих способностей учащихся через увеличение доли
самостоятельной работы при работе с модулем и проведении исследования.
Методы:
стимулирования и мотивации учения; организации и осуществления учебно-познавательной деятельности (самостоятельная работа с модульной программой, практическая работа - исследование).
Оборудование и реактивы:
модули для учащихся, растворы: карбоната натрия, соляной кислоты; порошок мела, мрамор, ракушки, яичная скорлупа, жемчуг, шприц, пробирки.
Ход урока:
I. Организация начала урока, подготовка учащихся к уроку.
II. Активизация, подготовка к учебно-познавательной деятельности:
Учитель:
Что такое карбонаты? Как человек использует карбонаты в своей жизни?
Как видим, эти соединения играют важную роль в нашей жизни.
Тема нашего урока «Качественное определение карбонатов». Как вы считаете, ребята, чем мы будем заниматься сегодня на уроке?
Сегодня на уроке узнаем, какой реактив используется для распознавания карбонатов, каковы признаки данной реакции, исследуем ряд природных материалов и определим их состав.
Учитель:
дает учащимся инструктаж по работе с модулем.
Учащиеся работают по модулю. Учитель оказывает помощь.
«Качественное определение карбонатов»
Изучив материал вы:
· научитесь качественно определять карбонаты;
· закрепите знания о химических свойствах карбонатов;
· узнаете о природных соединениях, содержащих карбонаты.
. Входной контроль. Цель:
повторить учебный материал.
Задание: Выполните проверочную работу письменно в тетради:
1. Установите соответствие:
Формулы Вещества
А. СаСО3
1. углекислый газ
Б. Н 2
СО3
2. угарный газ
В. СО 3. карбонат кальция
Г. СН4
4. угольная кислота
Д. СО2
2. Назовите два типа солей, образуемых угольной кислотой. Приведите по одному
примеру на каждый случай и назовите соли.
Качественное определение карбонатов.
Цели:
Изучив данный материал, вы познакомитесь с качественной реакцией на карбонаты.
Задание:
1.Изучите текст.
2. Запишите в тетрадь:
- Реактив, который используют для определения карбонатов.
- Признаки качественной реакции.
Угольная кислота образует два ряда солей: карбонаты и гидрокарбонаты. В отличие от самой угольной кислоты, ее соли довольно устойчивы. Качественной реакцией для определения ионов СО3
2-
является взаимодействие карбонатов и гидрокарбонатов с растворами сильных кислот
Na2
CO3
+ 2НСI = 2NaCI + Н2
О + СО2
↑
2Н+
+ СО3
2-
→ Н2
О + СО2
↑
При определении карбоната кальция лучше использовать соляную кислоту.
Чтобы убедиться в том, что выделяющийся газ - СО2
, его пропускают через известковую воду, которая мутнеет вследствие образования осадка СаСО3
:
СО2
+ Са(ОН)2
= СаСО3
+ Н2
О
Задание: Выполните
лабораторный опыт «Качественная реакция на карбонаты»:
1. Внимательно прочитайте правила техники безопасности:
- Помните об осторожном обращении со стеклом!
- При работе с кислотами надо соблюдать осторожность! При попадании кислоты на кожу или слизистые ткани надо промыть пораженное место большим количеством воды, затем обработать раствором питьевой соды.
2. Изучите порядок работы:
Опыт.
1)В чистую пробирку налейте немного раствора карбоната натрия, добавьте к нему раствор соляной кислоты. Наблюдения запишите в тетрадь.
2) В пробирку с мелом добавьте раствор соляной кислоты. Наблюдения запишите.
Задание.
Запишите уравнение одной реакции (по выбору) в молекулярном и ионном виде. Сделайте вывод и запишите в тетрадь: какой реактив используется для определения карбонатов, назовите признак реакции.
Природные процессы и применение качественного определения карбонатов.
Цели:
Изучив данныйматериал, вы узнаете о роли изучаемой реакции в природных процессах, о применении в быту, производстве.
Огромную роль в формировании облика нашей планеты играют процессы, которые можно описать следующими уравнениями:
СО2
+ Са(ОН)2
= СаСО3
+ Н2
О
СаСО3
+ Н2
О+ СО2
↑= Са(НСО3
)2
Одним из результатов данных процессов является образование карстовых пещер, в которых образуются сталактиты и сталагмиты.
В повседневной жизни нам часто приходится сталкиваться с солями угольной кислоты. Питьевая сода применяется в пищевой промышленности как разрыхлитель, в медицинских целях - для устранения изжоги. Для нейтрализации промышленных кислых сточных вод используют кристаллическую соду. В строительстве широко применяется известняк, мрамор, для отделочных работ и украшений – малахит. Известняки широко распространены по всей территории Якутии, их значительное количество наблюдается в Хангаласском улусе. Геологи в полевых условиях определяют карбонатные минералы, действуя на них кислотой.
Задание: Выполните
лабораторный опыт «Исследование состава природных образцов»:
1. Помните о технике безопасности!
2. Изучите порядок работы:
В чистые пробирки поместите:
1) небольшой кусочек яичной скорлупы,
2) 1 жемчужину (арагонит),
3) небольшой кусочек мрамора (кальцит),
4) добавьте в каждую пробирку раствор соляной кислоты.
5) в углубление ракушки внесите 1-2 капли соляной кислоты с помощью шприца.
6) Свои наблюдения оформите в виде таблицы в тетради:
7)
| Природные вещества
|
Наблюдения
|
| Яичная скорлупа |
| Жемчуг
|
| Мрамор
|
| Ракушка
|
Задание:
Какое соединение кальция содержат природные вещества: яичная скорлупа, жемчуг, мрамор, ракушка?
Запишите в тетрадь:
1) формулу вещества;
2) химическое название вещества;
3) вывод.
Выходной контроль.
Цели:
При выполнении данного вы определите уровень усвоения изученного материала.
Задание:
1.Выполните задание программы А.
2. Если вы испытаете затруднения при выполнении задания, обратитесь к записям в рабочей тетради, материалу учебника п.19, воспользуйтесь консультацией учителя.
3. Если вы не успеваете выполнить задания выходного контроля, можно доработать его после уроков или при выполнении домашнего задания.
Программа А
Раствор карбоната калия добавили к растворам: а) серной кислоты, б) нитрата калия. В каких случаях будет протекать химическая реакция? Запишите уравнения возможных реакций в молекулярном и ионном виде.
Задание:
1. После выполнения программы А вы можете приступить к выполнению заданий программы В.
Программа В
Составьте два молекулярных уравнения реакций, соответствующих сокращенному ионному: 2Н+
+ СО3
2-
→ Н2
О + СО2
↑ . Для чего используются эти реакции?
Домашнее задание
:
1. Проведите опыт «Взаимодействие питьевой соды с уксусной кислотой».
2. Запишите уравнение реакции в молекулярном и ионном виде, учитывая, что формула уксусной кислоты СН3
СООН.
ГЛАВА III. МОИ УРОКИ
Урок-турнир
Что мы знаем, что мы умеем
Основные классы неорганических соединений
Оборудование и реактивы. магнитофон, кубики, ребусы, волшебные ящики, магнитная доска, необходимые реактивы для экспериментальных работ.
Введение в игру. В игре участвуют две команды. Из наиболее подготовленных учащихся 9-х классов создают творческую группу, которая вместе с учителем разрабатывает форму и правила проведения урока, выбирает систему оценок, изготавливает призы, помогает учителю в проведении игры. Один из учеников исполняет роль старика Хоттабыча.
А. Оживление схемы.
Б. Волшебные ящики.
В. Угадайте правильный ответ.
ХОД УРОКА
Хоттабыч. Здравствуйте! Мы открываем турнир, девиз которого: «Что мы знаем, что мы умеем». Как и всякая наука, химия требует к себе самого серьезного и ответственного отношения. Вы успели познакомиться с химией, мои юные друзья. Сегодня мы узнаем самого находчивого, сообразительного, внимательного ученика. В гостях у нас ваши родители. Каждое выполненное задание и правильный ответ оцениваются одним баллом. В честь начала нашего турнира зажигаю священный огонь (заранее готовят смесь веществ
KMnO4
, H2
SO4
, C2
H5
OH).
Турнир открыт. У меня пожелание всем участникам: будьте честными, активными, не забывайте, что дружба помогает преодолевать испытания. Уважаемые родители, участвуйте в наших играх, радуйтесь вместе с детьми. Может быть, урок поможет вам вспомнить школьные годы.
Дальше, дальше, дальше...
За короткое время команды должны ответить на максимальное количество вопросов.
1) Кто открыл закон сохранения веществ? 2) Назовите формулу поваренной соли. 3) Что общего у всех кислот? 4) Назовите самый распространенный элемент в космосе. 5) Сколько кислорода (%) содержится в воздухе? 6) Как проверить водород на чистоту? 7) Как называется реакция между кислотой и основанием? 8) Назовите растворимые в воде основания. 9) Напишите формулу карбоната магния. 10) Назовите съедобные кислоты. 11) В какой цвет окрашивается фенолфталеин в кислотах? 12) В какой цвет окрашивается лакмус в щелочах?
Выполнение заданий
Конкурсы проходят одновременно.
А. Оживление схемы. У доски работают по два представителя от каждой команды:
Рb – PbO – PbCl2
– Pb(OH)2
– PbO; Р – P2
O5
– H3
PO4
– Ca3
(PO4
)2
– CaSO4
.
Б. Волшебные ящики. В ящиках находятся пробирки с реактивами без этикеток. По два участника выполняют опыты и объясняют происходящие явления.
1) Определите, в какой из двух пробирок находится раствор щелочи. 2) Получите реакцией обмена Fe(ОН)3
, из него – Fe2
(SO4
)3
. (Даны: FeCl3
, КОН, H2
SO4
.)
В. Угадайте правильный ответ. Остальные участники выполняют это задание в письменном виде.
1) Определите формулу оксида Мn(VII): а) МnО2
; б) Мn2
О7
; в) Мn2
О3
; г) МnО3
2) Если железный гвоздь погрузить в раствор хлорида меди, то он покрывается красным налетом меди. Какая происходит реакция?
а) Обмена;
б) замещения;
в) разложения;
г) соединения.
3) В три пробирки с разбавленной серной кислотой помещают по 1 г: в № 1 – магний, № 2 – алюминий, № 3 – серебро. В какой пробирке реакция не происходит?
а) № 1; б) № 2; в) № 3.
4) В трех пробирках находятся вещества:
№ 1 – вода, № 2 – бензин, № 3 – соляная кислота. В каждую из них добавили лакмус.
В какой пробирке раствор не изменит своего цвета?
а) № 1; б) № 2; в) № 3; г) не изменит ни в одной.
5) К какому типу реакции относится взаимодействие CuO c H2
SO4
?
а) Обмена; б) соединения; в) замещения.
6) Укажите реакцию нейтрализации:
а) KOH + HCl; б) Mn + HCl; в) СаО + HCl; г) Na + H2
O.
7) Силикаты – это соли какой кислоты?
8) Какое основание нерастворимо в воде?
а) KOH; б) Ca(OH)2
; в) Fe(OH)3
; г) NaOH.
9) Какое из перечисленных веществ является солью?
а) НNО3
; б) H2
SO4
; в) NH4
NO3
.
10) Общим свойством для растворимых и нерастворимых в воде оснований является взаимодействие с:
а) водой; б) кислотами; в) солями; г) основными оксидами.
После написания работы ассистенты собирают листки, проверяют их и комментируют.
Расшифруйте сказку
Запишите содержание сказки с помощью формул и уравнений химических реакций, назовите тип реакции.
«Дружили Соляная Кислота и Щелочь – Гидроксид Натрия. Однажды Соляная Кислота пригласила в гости подругу. Щелочь надела свое фенолфталеиновое платье и стала вся малиновая. День был солнечный. Кислота решила показать подружке свой красивый сад. Вышли в сад, но что это? Все цветы, кусты, деревья засохли, хотят пить и просят помощи. – Давай поможем им, – сказала Кислота и задумалась. – А как? – Я знаю, как им помочь! – воскликнула Щелочь. – Объединим мою ОН-группу и твой водород.
– С удовольствием, – согласилась Кислота.
Вода – эликсир жизни на Земле. Именно вода доставляет питательные вещества растениям. Щелочь обняла подругу. Исчезли Кислота и Щелочь. Потекла вода по корням растений. Все ожило вокруг, зазеленело, зацвело. Все благодарили двух подружек».
Пока члены жюри подводят итоги и подсчитывают баллы, коллективу предлагают разгадать ребусы. Звучит тихая музыка.
Решение экспериментальных задач
Практическая работа № 3
Тема:
«Решение экспериментальных задач на распознавание катионов и анионов»
Вариант 1
Оборудование и реактивы
: штатив для пробирок, пронумерованные пробирки с растворами, в которых находятся растворы карбоната калия, гидроксида натрия, хлорида бария, пробирки (6шт.), пипетки (2шт.); растворы серной кислоты, фенолфталеина, лакмуса, нитрата серебра.
Содержание и порядок выполнения опыта
1. теоретически решите задачу на распознавание веществ, используя минимальное число реактивов.
В трех пробирках находятся растворы карбоната калия, гидроксида натрия и хлорида бария. Определите, в какой пробирке находится каждое из веществ.
1. Впишите в таблицу 1 формулы исследуемых веществ, реактивы на ионы, содержащихся в исследуемых веществах, и признаки реакций, наблюдаемые при сливании растворов веществ.
| Название вещества, его формула |
Формулы реактивов |
| Карбонат калия…… |
| Гидроксид натрия…... |
| Хлорид бария……. |
2. Запишите молекулярные и ионные уравнения возможных реакций для тех случаев, когда наблюдается изменение в реакционной системе (образование газа, осадка, изменение цвета и т.д.).
2. Решите задачу экспериментально, соблюдая правила техники безопасности
Из пронумерованных пробирок с исследуемыми веществами возьмите пробы (по 1-2мл) растворов. Добавьте в каждую из них по несколько капель одного из реактивов. Отметьте наблюдения в таблице 2. Повторяйте эти действия до тех пор. Пока не определите содержимое всех пробирок с растворами исследуемых веществ.
| Номер пробирки |
Формулы реактивов |
| …….. |
…….. |
…….. |
| 1 |
| 2 |
| 3 |
3. Сделайте вывод о том, в какой из пробирок находилось каждое из исследуемых веществ.
Глава IV Тесты и задачи
Тесты
1.Фенолфталеин изменяет окраску при добавлении к:
а) к раствору серной кислоты
б) раствору гидроксида натрия +
в) воде
г) гидроксиду меди (II)
2.Метилоранжем можно распознать
а) соляную кислоту +
б) гидроксид железа (III)
в) воду
г) гидроксид меди (II)
3.В растворе кислот
а) фенолфталеин становится малиновым
б) лакмус краснеет +
в) лакмус синеет
г) метилоранж желтеет
4.Цвет индикатора изменяется под действием соляной кислоты следующим образом:
а) лакмус краснеет +
б) лакмус синеет
в) метилоранж желтеет
г) фенолфталеин становится малиновым
5.В растворе гидроксида натрия
а) фенолфталеин становится малиновым +
б) лакмус краснеет
в) метилоранж краснеет
г) фенолфталеин не изменяет цвета
6.В растворе щелочей:
а) фенолфталеин приобретает малиновый цвет +
б) метилоранж краснеет
в) лакмус краснеет
г) фенолфталеин не изменяет цвета
7.Лакмусом можно распознать два вещества пары
а) 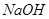 и и 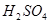 + +
б) 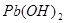 и и 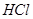
в) 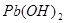 и и  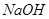
г) 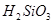 и и 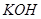
8.Углекислый газ можно распознать раствором
а) гидроксида калия
б) азотной кислоты
в) нитрата серебра
9. г) гидроксида кальция +
Кислород можно распознать
а) лакмусом
б) тлеющей лучинкой +
в) известковой водой
г) по запаху
10. Лакмусом можно распознать
а) соляную кислоту +
б) гидроксид железа (III)
в) воду
г) оксид кремния (IV)
11. Оксиды фосфора (V) и цинка являются соответственно
а) кислотными и основными
б) основным и кислотным
в) кислотным и амфотерным +
г) основным и амфотерным
12. Карбонат – ионы можно обнаружить водным раствором:
а) хловодорода +
б) хлорида натрия
в) гидроксида натрия
г) сульфата аммония
13. Состав соли (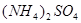 ) можно установить используя два раствора, содержащие ионы ) можно установить используя два раствора, содержащие ионы
а) 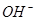 и и 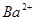 + +
б) 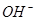 и и 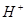
в) 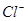 и и 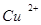
г) 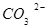 и и 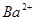
14. Качественный состав хлорида бария можно установить, используя два раствора, содержащие ионы
а) 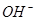 и и 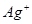 + +
б) 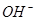 и и 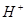
в) 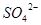 и и 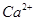
г) 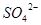 и и 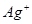
15. Присутствие гидроксида кальция в водном растворе можно доказать с помощью
а) лакмуса и азотной кислоты
б) лакмуса и углекислого газа
в) фенолфталеина и хлороводорода
г) фенолфталеина и аммиака +
16. Присутствие в водном растворе серной кислоты можно доказать с помощью
а) лакмуса и карбоната кальция
б) лакмуса и хлорида бария +
в) фенолфталеина и хлорида бария
г) фенолфталеина и гидроксида натрия
17. Реактивом на ионы бария может быть
а) гидроксид натрия
б) сульфат натрия +
в) лакмус
г) нитрат серебра
18. Реактивом на сульфат-ионы является
а) гидроксид натрия
б) лакмус
в) хлорида бария (р-р) +
г) нитрат серебра
19. Качественной реакцией на соли аммония является действие
а) щелочи +
б) другой соли
в) кислоты
г) лакмуса
20. Реактивом на хлорид-ионы является
а) гидроксид бария
б) сульфат аммония
в) карбонат натрия
г) нитрат серебра +
Задачи по теме: «Качественный анализ»
1.
В два одинаковых химических стакана налиты равные объемы: в один воды, в другой — разбавленного раствора серной кислоты. Как, не имея под рукой никаких химических реактивов, различить эти жидкости (пробовать растворы на вкус нельзя)?
2.
В четырех пробирках находятся порошки оксида меди(II), оксида железа (III), серебра, железа. Как распознать эти вещества, используя только один химический реактив? Распознавание по внешнему виду исключается.
3.
В четырех пронумерованных пробирках находятся сухие оксид меди (II), сажа, хлорид натрия и хлорид бария. Как, пользуясь минимальным количеством реактивов, определить, в какой из пробирок находится какое вещество? Ответ обоснуйте и подтвердите уравнениями соответствующих химических реакций.
4.
В шести пробирках без надписей находятся безводные соединения: оксид фосфора(V), хлорид натрия, сульфат меди, хлорид алюминия, сульфид алюминия, хлорид аммония. Как можно определить содержимое каждой пробирки, если имеется только набор пустых пробирок, вода и горелка? Предложите план анализа.
5
. В четырех пробирках без надписей находятся водные растворы гидроксида натрия, соляной кислоты, поташа и сульфата алюминия. Предложите способ определения содержимого каждой пробирки, не применяя дополнительных реактивов.
6
. В пронумерованных пробирках находятся растворы гидроксида натрия, серной кислоты, сульфата натрия и фенолфталеин. Как различить эти растворы, не пользуясь дополнительными реактивами?
7.
В банках без этикеток находятся следующие индивидуальные вещества: порошки железа, цинка, карбоната кальция, карбоната калия, сульфата натрия, хлорида натрия, нитрата натрия, а также растворы гидроксида натрия и гидроксида бария. В Вашем распоряжении нет никаких других химических реактивов, в том числе и воды. Составьте план определения содержимого каждой банки.
8
. В четырех пронумерованных банках без этикеток находятся твердые оксид фосфора (V) (1), оксид кальция (2), нитрат свинца (3), хлорид кальция (4). Определить, в какой из банок находится каждое из
указанных соединений, если известно, что вещества (1) и (2) бурно реагируют с водой, а вещества (3) и (4) растворяются в воде, причем полученные растворы (1) и (3) могут реагировать со всеми остальными растворами с образованием осадков.
9
. В пяти пробирках без этикеток находятся растворы гидроксида, сульфида, хлорида, йодида натрия и аммиака. Как определить эти вещества при помощи одного дополнительного реактива? Приведите уравнения химических реакций.
10.
Как распознать растворы хлорида натрия, хлорида аммония, гидроксида бария, гидроксида натрия, находящиеся в сосудах без этикеток, используя лишь эти растворы?
11.
. В восьми пронумерованных пробирках находятся водные растворы соляной кислоты, гидроксида натрия, сульфата натрия, карбоната натрия, хлорида аммония, нитрата свинца, хлорида бария, нитрата серебра. Используя индикаторную бумагу и проводя любые реакции между растворами в пробирках, установить, какое вещество содержится в каждой из них.
12.
В двух пробирках имеются растворы гидроксида натрия и сульфата алюминия. Как их различить, по возможности, без использования дополнительных веществ, имея только одну пустую пробирку или даже без нее?
13.
В пяти пронумерованных пробирках находятся растворы перманганата калия, сульфида натрия, бромная вода, толуол и бензол. Как, используя только названные реактивы, различить их? Используйте для обнаружения каждого из пяти веществ их характерные признаки (укажите их); дайте план проведения анализа. Напишите схемы необходимых реакций.
14.
В шести склянках без наименований находятся глицерин, водный раствор глюкозы, масляный альдегид (бутаналь), гексен-1, водный раствор ацетата натрия и 1,2-дихлорэтан. Имея в качестве дополнительных химических реактивов только безводные гидроксид натрия и сульфат меди, определите, что находится в каждой склянке.
Решения
1.
Для определения воды и серной кислоты можно использовать различие в физических свойствах: температурах кипения и замерзания, плотности, электропроводности, показателе преломления и т. п. Самое сильное различие будет в электропроводности.
2.
Прильем к порошкам в пробирках соляную кислоту. Серебро не прореагирует. При растворении железа будет выделяться газ: Fe + 2HCl = FeCl2
+ H2

Оксид железа (III) и оксид меди (II) растворяются без выделения газа, образуя желто-коричневый и сине-зеленый растворы:
Fe2
O3
+ 6HCl = 2FeCl3
+ 3H2
O; CuO + 2HCl = CuCl2
+ H2
O.
3.
CuO и С — черного цвета, NaCl и ВаВr2
- белые. Единственным реактивом может быть, например, разбавленная серная кислота H2
SO4
:
CuO + H2
SO4
= CuSO4
+ H2
O (голубой раствор); BaCl2
+ H2
SO4
= BaSO4
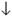 + 2HCl (белый осадок). + 2HCl (белый осадок).
С сажей и NaCl разбавленная серная кислота не взаимодействует.
3. Небольшое количество каждого из веществ помещаем в воду:
CuSO4
+5H2
O = CuSO4
 5H2
O 5H2
O |
(образуется голубой раствор и кристаллы); |
Al2
S3
+ 6H2
O = 2Al(OH)3
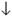 + 3H2
S + 3H2
S |
(выпадает осадок и выделяется газ с неприятным запахом); |
AlCl3
+ 6H2
O = A1C13
 6H2
O + Q AlCl3
+ H2
O 6H2
O + Q AlCl3
+ H2
O  AlOHCl2
+ HCl AlOHC12
+ H2
0 = Al (OH) 2
Cl + HCl А1(ОН)2
С1 + Н2
О = А1(ОН)2
+ НСl AlOHCl2
+ HCl AlOHC12
+ H2
0 = Al (OH) 2
Cl + HCl А1(ОН)2
С1 + Н2
О = А1(ОН)2
+ НСl |
(протекает бурная реакция, образуются осадки основных солей и гидроксида алюминия); |
| P2
O5
+ H2
O = 2HPO3
HPO3
+H2
O = H3
PO4
|
(бурная реакция с выделением большого количества тепла, образуется прозрачный раствор). |
Два вещества — хлорид натрия и хлорид аммония— растворяются, не реагируя с водой; их можно различить, нагревая сухие соли (хлорид аммония возгоняется без остатка): NH4
Cl  NH3 NH3
 + HCl + HCl ; или по окраске пламени растворами этих солей (соединения натрия окрашивают пламя в желтый цвет). ; или по окраске пламени растворами этих солей (соединения натрия окрашивают пламя в желтый цвет).
6.
Попарно смешивают все растворы Пара растворов, дающая малиновую окраску, — NaOH и фенолфталеин Малиновый раствор прибавляют в две оставшиеся пробирки. Там, где окраска исчезает, — серная кислота, в другой — сульфат натрия. Остается различить NaOH и фенолфталеин (пробирки 1 и 2). А. Из пробирки 1 прибавляют каплю раствора к большому количеству раствора 2. Б. Из пробирки 2 — каплю раствора прибавляют к большому количеству раствора 1. В обоих случаях— малиновое окрашивание. К растворам А и Б прибавляют по 2 капли раствора серной кислоты. Там, где окраска исчезает, содержалась капля NaOH. (Если окраска исчезает в растворе А, то NaOH — в пробирке 1).
8
. Бурно реагируют с водой: Р2
О5
и СаО с образованием соответственно H3
PO4
и Са(ОН)2
:
Р2
O5
+ 3Н2
О = 2Н3
РO4
, СаО + Н2
О = Са(ОН)2
.
Вещества (3) и (4) -Pb(NO3
)2
и СаСl2
- растворяются в воде. Растворы могут реагировать друг с другом следующим образом:
| Вещества |
1. Н3
РО4
|
2.Са(ОН)2
, |
3.Pb(NO3
)2
|
4. CaCl2
|
| 1. Н3
РО4
|
X |
CaHPO4
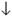 |
PbHPO4
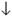 |
CaHPO4
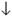 |
| 2.Са(ОН)2
|
СаНРО4
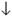 |
X |
Pb(OH)2
|
— |
| 3.Pb(NO3
)2
|
РbНРО4
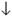 |
Pb(OH)2
 |
X |
РbСl2
 |
| 4. СаС12
|
CaHPO4
 |
PbCl2
 |
X |
Таким образом, раствор 1 (H3
PO4
) образует осадки со всеми другими растворами при взаимодействии. Раствор 3 — Pb(NO3
)2
также образует осадки со всеми другими растворами. Вещества: I —Р2
O5,
II —СаО, III —Pb(NO3
)2
, IV—СаСl2
. В общем случае выпадение большинства осадков будет зависеть от порядка сливания растворов и избытка одного из них (в большом избытке Н3
РО4
фосфаты свинца и кальция растворимы).
9.
Задача имеет несколько решений, два из которых приведены ниже. а.
Во все пробирки добавляем раствор медного купороса: 2NaOH + CuSO4
= Na2
SO4
+ Cu(OH)2
 (голубой осадок); Na2
S + CuSO4
= Na2
SO4
+ CuS (голубой осадок); Na2
S + CuSO4
= Na2
SO4
+ CuS (черный осадок); NaCl + CuSO4
(в разбавленном растворе изменений нет); 4NaI+2CuSO4
= 2Na2
SO4
+ 2CuI (черный осадок); NaCl + CuSO4
(в разбавленном растворе изменений нет); 4NaI+2CuSO4
= 2Na2
SO4
+ 2CuI +I2 +I2
 (коричневый осадок); 4NH3
+ CuSO4
= Cu(NH3
)4
SO4
(синий раствор или голубой осадок, растворимый в избытке раствора аммиака). (коричневый осадок); 4NH3
+ CuSO4
= Cu(NH3
)4
SO4
(синий раствор или голубой осадок, растворимый в избытке раствора аммиака).
б.
Во все пробирки добавляем раствор нитрата серебра: 2NaOH + 2AgNO3
= 2NaNO3
+ Н2
О + Ag2
O (коричневый осадок); Na2
S + 2AgNO3
= 2NaNO3
+ Ag2
S (коричневый осадок); Na2
S + 2AgNO3
= 2NaNO3
+ Ag2
S (черный осадок); NaCl + AgNO3
= NaN03
+ AgCl (черный осадок); NaCl + AgNO3
= NaN03
+ AgCl (белый осадок); NaI + AgNO3
= NaNO3
+ AgI (белый осадок); NaI + AgNO3
= NaNO3
+ AgI (желтый осадок); 2NH3
+ 2AgNO3
+ H2
O = 2NH4
NO3
+ Ag2
O (коричневый осадок). Ag2
O растворяется в избытке раствора аммиака: Ag2
0 + 4NH3
+ H2
O = 2[Ag(NH3
)2
]OH. (желтый осадок); 2NH3
+ 2AgNO3
+ H2
O = 2NH4
NO3
+ Ag2
O (коричневый осадок). Ag2
O растворяется в избытке раствора аммиака: Ag2
0 + 4NH3
+ H2
O = 2[Ag(NH3
)2
]OH.
NaOH и Ва(ОН)2
можно различить по разному окрашиванию пламени (Na+ окрашивают в желтый цвет, а Ва2
+ — в зеленый).
12.
В пустую пробирку наливают один из растворов и приливают каплю другого.
Случайпервый : образовался осадок и сразу растворился, или вовсе не образовался:
6NaOH + Al2
(SO4
)3
 3Na2
SO4
+ 2Al(OH)3 3Na2
SO4
+ 2Al(OH)3
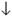 ; ;
Al(OH)3
+ NaOH (избыток) + 2Н2
О Na[Al(OH)4
(H2
O)2
]. Na[Al(OH)4
(H2
O)2
].
Значит, раствор (1)—NaOH, раствор (2) — Al2
(SO4
)3
.
Случайвторой : осадок образовался и не растворился. Тогда, наоборот, раствор (1) — Al2
(SO4
)3
, а раствор (2)—NaOH.
1. Во время практической работы вы пролили случайно на стол кислоты. Ваши действия? Выберите ответ:
- вытереть пролитое тряпкой для мела.
- насухо вытереть стол бумагой
- смыть водой
- засыпать содой, затем смыть водой
- нейтрализовать раствором щелочи или раствором аммиака. +
2. Вы обожглись дном неостывшей пробирки. Ваши действия? Выберите правильный ответ:
- смазать ожог вазелином
- промыть руку под струей холодной воды +
- смазать йодом
- сделать спиртовой компресс
- промыть борной кислотой.
3. На руку попала щелочь. Ваши действия? Выберите правильный ответ:
- смыть большим количеством воды
- нейтрализовать кислотой (уксусной или соляной). +
- смазать вазелином
- тщательно протереть ватой, тряпкой или бумагой.
- промыть раствором аммиака.
ЛИТЕРАТУРА
1. Т. Н. Кровельщикова, А. В. Коршунов. Из опыта реализации экологического подхода к обучению химии / Химия в школе. 2002, № 8, с. 40-42.
2. Чернобельская Г. М. Методика обучения химии в средней школе: Учеб. для студ. высш. учеб. заведений. — М.: Владос, 2000. — 336 с.
3. О. С. Зайцев. Методика обучения химии: Теоретический и прикладной аспекты. – М.: Гуманит. изд. ВЛАДОС, 1999. – 358 с.
4. Ф. Г. Фельдман, Г. Е. Рудзитис. Химия, 8 кл. М.: Просвещение, 1985.
5. Д. М. Кирюшкин, В. С. Полосин. Методика обучения химии. М.: Просвещение, 1970. C. 297 – 302.
6. Р. И. ТагировКак мы изучаем химические свойства оснований и солей / Химия в школе, 2002, № 9, с. 58 – 59.
7. Пособие по химии для поступающих в вузы. Г. П. Хомченко. 1976 г.
8. www.1september.ru
9. И. И. Супоницкая, Н. И. Гоголевская.Комплект обобщающих схем-конспектов по теме «Электролитическая диссоциация». // Хим. в шк. № 5. 1991. С. 25-30.
10. И. Г. Афонина. Тестовые задания в курсе химии. // Химия в школе. № 7, 2002, с. 43 – 45.
11. Единый государственный экзамен 2002: Контрольные измерительные материалы: Химия / А. А. Каверина, Д. Ю. Добротин, М. Г. Снастина и др.; М-во образования РФ. – М.: Просвещение, 2002. – 142 с.
12. Лидин Р. А. Химия: Руководство к экзаменам / Р. А. Лидин, В. Б. Маргулис. – М.: ООО Издательство «АСТ»: ООО «Издательство Астрель», 2003. 207 с.
13. Химия: Большой справочник для школьников и поступающих в вузы / Е. А. Алферова, Н. С. Ахметов, Н. В. Богомолова и др. М.: Дрофа, 1999. с. 430-438.
14. Химия: Сборник тестовых заданий для подготовки к итоговой аттестации (варианты и ответы, решение расчетных задач). 9 класс (базовый уровень) / Н.В. Ширшина. – Волгоград: Учитель, 2004. – 81 с.
|