Министерство образования и науки Российской Федерации
Федеральное Агентство общего и профессионального образования
Челябинский государственный университет
Кафедра аналитической и физической химии
Курсовая работа
Определение термодинамических активностей компонентов бронзы БрБ2
Челябинск 2006
Содержание
Введение
1. Литературный обзор
1.1 Медь и сплавы на её основе. Бронзы
1.2 Диаграмма состояния Be–Cu
1.3 Диаграмма состояния Be–Ni
1.4 Диаграмма состояния Cu–Ni
1.5 Термодинамическое моделирование свойств твёрдых металлических растворов
2. Расчётная часть
2.1 Расчёт зависимости энергий смешения компонентов системы Cu–Ni от температуры
2.2 Расчёт купола расслаивания твёрдого раствора Cu–Ni
2.3 Вычисление термодинамических активностей меди и никеля в бинарной системе при 25°С
2.4 Вычисление термодинамических активностей компонентов бронзы БрБ2 при 25°С
Выводы
Приложения
Список использованной литературы
медь бронза термодинамическая активность
Введение
Цель данной работы – расчёт термодинамических активностей компонентов бериллиевой бронзы БрБ2. Это является первым шагом на пути к изучению термодинамических свойств этой бронзы, построению диаграмм устойчивости сплава в различных условиях, изучению его физико-механических свойств. В настоящее время сплавы на основе меди, и в частности, бронзы находят широкое применение в различных областях науки и техники. Поэтому изучение свойств подобных сплавов – это интересный вопрос.
В первой части работы – обзоре литературы – будет приведена некоторая информация о меди и её сплавах. Особое внимание будет уделено бронзам, и в частности, бериллиевым бронзам.
Бериллиевая бронза БрБ2 – это трёхкомпонентная система. Для описания свойств её компонентов будут приведены диаграммы состояния бинарных систем, в которых эти компоненты соединены друг с другом попарно, а также краткие их описания.
Также будет рассказано о теории, в рамках которой будет произведён дальнейший расчёты – обобщённой теории «регулярных» растворов.
Вторая часть работы – расчётная. Собственно, в ней и будут приведены схемы расчётов всех необходимых величин и даны конкретные результаты, полученные автором работы.
Все комментарии к полученным результатам будут сделаны в выводах.
Реклама

1. Литературный обзор
1.1 Медь и сплавы на её основе. Бронзы [1, c. 406-417]
Медь — металл красного, в изломе розового цвета. Температура плавления чистой меди равна 1083°С. Кристаллическая решетка - ГЦК с периодом а
= 0,31607 нм. Плотность меди равна 8,94 г/см3
. Медь обладает настолько высокими электропроводимостью и теплопроводностью, что их принято принимать за 100%, а для всех других технических металлов, за исключением серебра, эти свойства сравнивать со свойствами меди и выражать в процентах. Удельное электрическое сопротивление меди равно 0,0175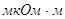 . В зависимости от чистоты медь изготовляют следующих марок: М00 (99,99% Cu), М0 (99,97% Cu), Ml (99,9% Cu), М2 (99,7% Cu), МЗ (99,50% Cu). Присутствующие в меди примеси оказывают большое влияние на ее свойства. . В зависимости от чистоты медь изготовляют следующих марок: М00 (99,99% Cu), М0 (99,97% Cu), Ml (99,9% Cu), М2 (99,7% Cu), МЗ (99,50% Cu). Присутствующие в меди примеси оказывают большое влияние на ее свойства.
По характеру взаимодействия примесей с медью их можно разделить на три группы.
1) Примеси, образующие с медью твердые растворы: Ni, Zn, Sb, Sn, Al, As, Fe, P и др.; эти примеси (особенно Sb и As) резко снижают электропроводимость и теплопроводность меди, поэтому для проводников тока применяют медь М0 и Ml, содержащую <0,002 % Sb и <0,002 % As. Сурьма, кроме того, затрудняет горячую обработку давлением.
2) Примеси Pb, Bi и другие, практически не растворимые в меди, образуют в ней легкоплавкие эвтектики, которые, выделяясь по границам зерен, затрудняют обработку давлением. При содержании 0,005% Bi медь разрушается при горячей обработке давлением; при более высоком содержании висмута медь становится, кроме того, хладноломкой; на электропроводимость эти примеси оказывают небольшое влияние.
3) Примеси кислорода и серы, образующие с медью хрупкие химические соединения Сu2
О и Cu2
S, входящие в состав эвтектики. Кислород, находясь в растворе, уменьшает электропроводимость, а сера не влияет на нее. Сера улучшает обрабатываемость меди резанием, а кислород, если он присутствует в меди, образует закись меди и вызывает «водородную болезнь».
При нагреве меди в атмосфере, содержащей водород, происходит его диффузия вглубь меди. Если в меди присутствуют включения Сu2
О, то они реагируют с водородом, в результате чего образуются пары воды по реакции
Сu2
О + Н2
→ 2Сu + Н2
О,
протекающей с увеличением объема. Это создает в отдельных участках металла высокое давление и вызывает появление микротрещин, которые могут привести к разрушению детали.
Медь хорошо сопротивляется коррозии в обычных атмосферных условиях, в пресной и морской воде и других агрессивных средах, но обладает плохой устойчивостью в сернистых газах и аммиаке.
Реклама

Механические свойства меди в литом состоянии таковы:
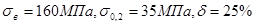 ; ;
в горячедеформированном состоянии:
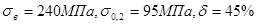 . .
При холодном деформировании предел прочности может быть повышен до 450 МПа (проволока) при снижении относительного удлинения до 3%. Модуль нормальной упругости меди равен 115 000 МПа.
Медь легко обрабатывается давлением, но плохо резанием, и имеет невысокие литейные свойства из-за большой усадки. Медь плохо сваривается, но легко подвергается пайке. Ее применяют в виде листов, прутков, труб и проволоки.
В электротехнической промышленности, электронике и электровакуумной технике применяют бескислородную М0б (0,001% О2
) и раскисленную М1р (0,01% О2
) медь.
Различают две основные группы медных сплавов:
1) Латуни — сплавы меди с цинком;
2) Бронзы — сплавы меди с другими элементами, в числе которых, но только наряду с другими, может быть и цинк. Медные сплавы обладают высокими механическими и техническими свойствами, хорошо сопротивляются износу и коррозии. Принята следующая маркировка медных сплавов. Сплавы обозначают буквами «Л» (латунь) или «Бр» (бронза), после чего следуют буквы основных элементов, образующих сплав. Например, О — олово, Ц — цинк, Мц — марганец, Ж — железо, Ф — фосфор, Б — бериллий, X — хром и т. д. Цифры, следующие за буквами, указывают количество легирующего элемента. ,
Порядок цифр для бронз и латуней различен. В марках деформируемых латуней первые две цифры после буквы «Л» указывают среднее содержание меди в процентах. Например, Л70 — латунь, содержащая 70% Си. В случае легированных деформируемых латуней указывают еще буквы и цифры, обозначающие название и количество легирующего элемента, например ЛАЖ60-1-1 означает латунь с 60% Сu, легированную алюминием (А) в количестве 1% и железом (Ж) в количестве 1%. Содержание цинка определяется по разности от 100% . В деформированных бронзах содержание основного компонента — меди — не указывается, а определяется по разности. Цифры после букв, отделенные друг от друга через тире, указывают среднее содержание легирующих элементов в процентах; цифры расположены в том же порядке, как и буквы, указывающие присутствие в бронзе того или иного элемента, например, бронза БрОЦ4-3 имеет следующий состав: олова (О) — 4%, цинка (Ц) — 3% . Содержание меди определяется по разности от 100%.
В литейных латунях и бронзах среднее содержание компонентов сплава в процентах ставится сразу после буквы, обозначающей его название. Например, латунь ЛЦ40Мц1,5 содержит 40% цинка (Ц) и 1,5% марганца (Мц). Бронза БрА10ЖЗМц2 содержит алюминия (А) 10%, железа (Ж) — 3% и марганца (Мц) — 2% .
Оловянные бронзы
. На рис. 1.1 приведена диаграмма состояния Сu—Sn. Фаза α представляет твердый раствор олова в меди с ГЦК-решегкой. В сплавах этой системы образуются электронные соединения: β-фаза (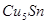 ), δ-фаза ( ), δ-фаза (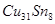 ), ε-фаза ( ), ε-фаза (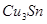 ), а также γ-фаза — твердый раствор на базе химического соединения, природа которого не установлена. Система Сu—Sn имеет ряд перитектических превращений и два превращения эвтектоидного типа. При температуре 588°С кристаллы β-фазы претерпевают эвтектоидный распад с образованием α- и γ-фаз, а при 520°С кристаллы твёрдого раствора γ распадаются на фазы α и δ. При температуре 350°С δ-фаза распадается на α-твердый раствор и ε-фазу. Однако это превращение протекает только при очень медленном охлаждении. В реальных условиях охлаждения бронза состоит из α и δ фаз. В практике применяют только сплавы с содержанием до 10 - 12% Sn. Сплавы, более богатые оловом, очень хрупки. Оловянные бронзы при ускоренном охлаждении имеют резко выраженное дендритное строение. ), а также γ-фаза — твердый раствор на базе химического соединения, природа которого не установлена. Система Сu—Sn имеет ряд перитектических превращений и два превращения эвтектоидного типа. При температуре 588°С кристаллы β-фазы претерпевают эвтектоидный распад с образованием α- и γ-фаз, а при 520°С кристаллы твёрдого раствора γ распадаются на фазы α и δ. При температуре 350°С δ-фаза распадается на α-твердый раствор и ε-фазу. Однако это превращение протекает только при очень медленном охлаждении. В реальных условиях охлаждения бронза состоит из α и δ фаз. В практике применяют только сплавы с содержанием до 10 - 12% Sn. Сплавы, более богатые оловом, очень хрупки. Оловянные бронзы при ускоренном охлаждении имеют резко выраженное дендритное строение.
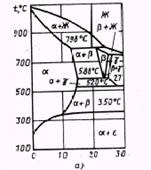
Рис. 1.1 Диаграмма состояния Cu-Sn
Бронзы, содержащие до 4-5% Sn, после деформации и отжига получают полиэдрическое строение и представляют собой в основном α-твердый раствор. После литья даже такие низколегированные бронзы в результате сильной ликвации могут иметь включения эвтектоида (α+δ).
При большем содержании олова в структуре бронз в равновесном состоянии с α-раствором присутствует эвтектоид (α+δ). Зависимость механических свойств литых бронз от содержания олова показана на рис. 1.2. Предел прочности возрастает с увеличением содержания олова. При высокой концентрации олова вследствие присутствия в структуре значительного количества эвтектоида, содержащего хрупкое соединение 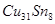 , предел прочности резко снижается. , предел прочности резко снижается.
Относительное удлинение несколько возрастает при содержании в бронзе 4-6% Sn, но при образовании эвтектоида сильно уменьшается. Оловянные бронзы обычно легируют Zn, Fe, P, Pb, Ni и другими элементами. Цинк улучшает технологические свойства бронзы и удешевляет её. Фосфор улучшает литейные свойства. Никель повышает механические свойства, коррозионную стойкость и плотность отливок и уменьшает ликвацию. Железо измельчает зерно, но ухудшает технологические свойства бронз и сопротивляемость коррозии. Легирование свинцом снижает механические свойства бронзы, но повышает плотность отливок, а главное — облегчает обработку резанием и улучшает антифрикционные свойства.
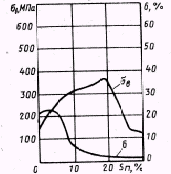
Рис. 1.2 Влияние олова на механические свойства бронз
Табл. 1.1 Механические свойства и назначение деформируемых и литейных оловянных бронз
| Бронза |
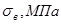 |
δ, % |
Назначение |
| Деформируемые бронзы (ГОСТ 5017-74)
|
| БрОФ6,5-0,4 |
400(750) |
65(10) |
Пружины, барометрические коробки, мембраны, антифрикционные детали |
| БрОЦ4-3 |
330(550) |
40(4) |
Плоские и круглые пружины |
| БрОЦС4-4-2,5 |
350(650) |
35(2) |
Антифрикционные детали |
| Литейные бронзы (ГОСТ 613-79)
|
| БрО3Ц12С5 |
200(170) |
5(8) |
Арматура общего назначения |
| БрО5ЦНС5 |
175(150) |
4(6) |
Антифрикционные детали, вкладыши подшипников, арматура |
| БрО4Ц4С17 |
150(150) |
12(5) |
Втулки, подшипники, вкладыши, червячные шары и т.п. |
Различают деформируемые и литейные оловянные бронзы (табл. 1.1).
В таблице для деформируемых бронз в скобках приведены свойства после холодной прокатки (наклёпа), а без скобок – свойства после отжига. Для литейных же бронз в скобках указаны свойства при литье в песчаную форму, а без скобок – свойства при литье в кокиль. Деформируемые бронзы изготовляют в виде прутков, лент и проволоки в нагартованном (твердом) и отожженном (мягком) состояниях. Эти бронзы чаще предназначаются для изготовления пружин и пружинных деталей, применяемых в различных отраслях промышленности. Структура деформированных оловянных бронз — это α-твердый раствор. Литейные бронзы, содержащие большое количество цинка, фосфора и нередко свинца, имеют двухфазную структуру: α-твердый раствор и твердые хрупкие включения δ-фазы, входящие обычно в структуру эвтектоида.
Оловянные бронзы обладают хорошими литейными свойствами и применяются для литья деталей сложной формы. Недостатком отливок из оловянных бронз является большая микропористость. Бронзы, особенно двухфазные, обладают высокими антифрикционными свойствами. В связи с этим их часто применяют для изготовления антифрикционных деталей.
Для облегчения обработки давлением бронзы подвергают гомогенизации при 700—750 °С с последующим быстрым охлаждением.
В таблице 1.2 указаны свойства и применение безоловянных бронз. Для литейных бронз без скобок указаны свойства при литье в кокиль, в скобках – свойства при литье в песчаную форму. Для бронзы БрБ2 без скобок указаны свойства сразу после закалки, в скобках – свойства после старения.
Табл. 1.2 Механические свойства и назначение деформируемых и литейных безоловянных бронз (ГОСТ 493-79, 18175-78)
| Бронза |
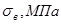 |
δ, % |
Назначение |
| Алюминиевые бронзы
|
| БрАЖ9-14 |
600 |
40 |
Обработка давлением (прутки, трубы, листы) |
| БрАЖН10-4-4 |
650 |
35 |
| БрА9Ж3Л |
490(392) |
12(10) |
Арматура, антифрикционные детали |
| БрА10Ж3Мц2 |
490(392) |
12(10) |
| Кремнистые бронзы
|
| БрКМц3-1 |
380 |
35 |
Прутки, ленты, проволока для пружин |
| Свинцовые бронзы
|
| БрС30 |
600 |
4 |
Антифрикционные детали |
| Бериллиевые бронзы
|
| БрБ2 |
500(950) |
45(1-2) |
Полосы, прутки, ленты, проволока для пружин |
Алюминиевые бронзы
. Наиболее часто применяют алюминиевые бронзы двойные и добавочно легированные Ni, Mn, Fe и др. Сплавы, содержащие до 9% Аl, однофазные и состоят только из α-твердого раствора алюминия в меди. Фаза β, существующая при температуре свыше 565°С, представляет собой твердый раствор на базе электронного соединения Си3
Аl. При содержании алюминия более 9% в структуре появляется эвтектоид α т γ' (γ' – это электронное соединение 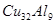 ). Фаза α пластична, по прочность её невелика. Двухфазные сплавы α+γ' имеют повышенную прочность, по пластичность их заметно ниже (рис. 1.3-1.4). Железо измельчает зерно и повышает механические и антифрикционные свойства алюминиевых бронз. Никель улучшает механические свойства и износостойкость, как при низких, так и при высоких температурах (500--600°С). ). Фаза α пластична, по прочность её невелика. Двухфазные сплавы α+γ' имеют повышенную прочность, по пластичность их заметно ниже (рис. 1.3-1.4). Железо измельчает зерно и повышает механические и антифрикционные свойства алюминиевых бронз. Никель улучшает механические свойства и износостойкость, как при низких, так и при высоких температурах (500--600°С).
Алюминиевые бронзы хорошо сопротивляются коррозии в морской воде и тропической атмосфере, имеют высокие механические и технологические свойства. Однофазные бронзы, обладающие высокой пластичностью, применяют для глубокой штамповки. Двухфазные бронзы подвергают горячей деформации или применяют в виде фасонного литья.
Литейные свойства алюминиевых бронз ниже, чем литейные свойства оловянных бронз, но они обеспечивают высокую плотность отливок.
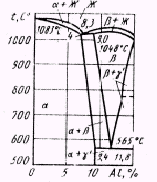
Рис. 1.3Диаграмма состояния Cu-Al
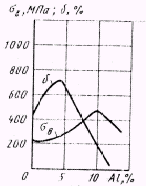
Рис. 1.4 Влияние алюминия на механические свойства бронз
Кремнистые бронзы
. При легировании меди кремнием (до 3,5%) повышается прочность, а также пластичность. Никель и марганец улучшают механические и коррозионные свойства кремнистых бронз. Эти бронзы легко обрабатываются давлением, резанием и свариваются. Благодаря высоким механическим свойствам, упругости и коррозионной стойкости их применяют для изготовления пружин и пружинящих деталей приборов и радиооборудования, работающих при температуре до 250°С. а также в агрессивных средах (пресная, морская вода).
Свинцовые бронзы
. Свинец практически не растворяется в жидкой меди. Поэтому сплавы после затвердевания состоят из кристаллов меди и включений свинца.
Такая структура бронзы обеспечивает высокие антифрикционные свойства. Это предопределяет широкое применение бронзы БрСЗ0 для изготовления вкладышей подшипников скольжения, работающих с большими скоростями и при повышенных давлениях. По сравнению с оловянными подшипниковыми бронзами теплопроводность бронзы БрСЗ0 в 4 раза больше, поэтому она хорошо отводит теплоту, возникающую при трении.
Из-за невысоких механических свойств (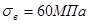 , δ=4%) бронзу БрСЗ0 наплавляют тонким слоем на стальные ленты (трубы). Такие биметаллические подшипники просты в изготовлении и легко заменяются при изнашивании. Вследствие большой разности значений плотности меди (8,94 г/см3
) и свинца (11,34 г/см3
) и широкого интервала кристаллизации бронза БрСЗ0 склонна к ликвации по плотности. Нередко свинцовые бронзы легируют никелем и оловом, которые, растворяясь в меди, повышают механические и коррозионные свойства. , δ=4%) бронзу БрСЗ0 наплавляют тонким слоем на стальные ленты (трубы). Такие биметаллические подшипники просты в изготовлении и легко заменяются при изнашивании. Вследствие большой разности значений плотности меди (8,94 г/см3
) и свинца (11,34 г/см3
) и широкого интервала кристаллизации бронза БрСЗ0 склонна к ликвации по плотности. Нередко свинцовые бронзы легируют никелем и оловом, которые, растворяясь в меди, повышают механические и коррозионные свойства.
Бериллиевые бронзы
. Эти бронзы относятся к сплавам, упрочняемым термической обработкой. Предельная растворимость бериллия в меди при температуре 866°С составляет 2,7%, при температуре 600 °С - 1,5%, а при 300°С всего 0,2%. Это указывает на возможность упрочнения бериллиевой бронзы методом дисперсного твердения. При нагреве бронзы БрБ2 до 760—780°С образуется однородный α-раствор, который сохраняется в результате быстрого охлаждения в воде при нормальной температуре. В составе бериллиевых бронз всегда присутствует никель или кобальт для повышения устойчивости переохлаждённого твёрдого раствора.
После закалки бронза обладает малой прочностью (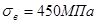 ), высокой пластичностью (δ = 40%) и способностью упрочняться при старении как непосредственно после закалки, так и после пластической деформации в закаленном состоянии. Старение проводят при 300—350°С. При старении из пересыщенного α-раствора выделяются дисперсные частицы γ-фазы (СuВе), что сильно повышает прочность бронзы. Предварительно наклепанная бронза при старении упрочняется сильнее и быстрее. ), высокой пластичностью (δ = 40%) и способностью упрочняться при старении как непосредственно после закалки, так и после пластической деформации в закаленном состоянии. Старение проводят при 300—350°С. При старении из пересыщенного α-раствора выделяются дисперсные частицы γ-фазы (СuВе), что сильно повышает прочность бронзы. Предварительно наклепанная бронза при старении упрочняется сильнее и быстрее.
Так, бронза БрБ2 в состоянии после закалки и старения имеет 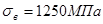 и δ=З÷5 %, а после закалки, холодной пластической деформации с обжатием 30% и старения - и δ=З÷5 %, а после закалки, холодной пластической деформации с обжатием 30% и старения - 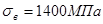 , пластичность после старения невелика (δ = 2%). Бронзу нередко легируют также титаном (0,1—0,25%): БрБНТ1,9 и БрБНТ1,7. Обладая высокими значениями временного сопротивления, пределов текучести и упругости, бериллиевые бронзы хорошо сопротивляются коррозии, свариваются и обрабатываются резанием. Бериллиевые бронзы применяют для мембран, пружин, пружинящих контактов, деталей, работающих на износ (кулачки полуавтоматов), в электронной технике и т. д. , пластичность после старения невелика (δ = 2%). Бронзу нередко легируют также титаном (0,1—0,25%): БрБНТ1,9 и БрБНТ1,7. Обладая высокими значениями временного сопротивления, пределов текучести и упругости, бериллиевые бронзы хорошо сопротивляются коррозии, свариваются и обрабатываются резанием. Бериллиевые бронзы применяют для мембран, пружин, пружинящих контактов, деталей, работающих на износ (кулачки полуавтоматов), в электронной технике и т. д.
Бериллиевая бронза БрБ2 содержит в своём составе (по массе) 97,5% Cu, 0,5% Ni, 2% Be.
Система бериллий – медь была хорошо изучена многими исследователями. На рисунке 1.5 представлена обобщённая диаграмма состояния.
Граница твердого раствора Be в Си определена во многих работах на основании данных микроскопического, рентгеновского, дилатометрического анализов, измерения твердости и электрических свойств. Растворимость Be в Сu при эвтектоидной температуре (600°С) составляет 10%(ат.), а при перитектической температуре (866°С) - 16,5% (ат.).
Растворимость Сu в Be изучена в нескольких работах. Установлено, что со стороны Beв системе имеет место эвтектоидное превращение, соответствующее β↔α-превращению Be. Его температура находится в пределах 1100—1120°С.
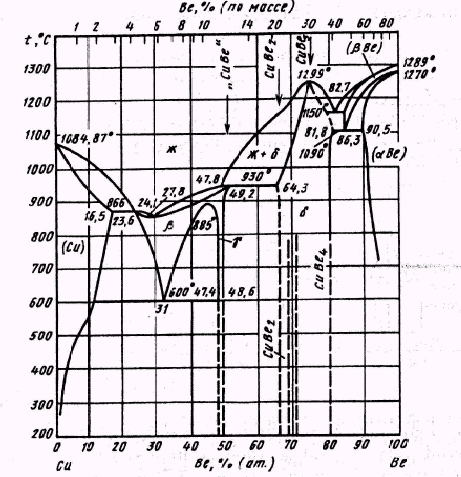
Рис. 1.5 Диаграмма состояния Be-Cu
Концентрация эвтектоиднои точки на представленной диаграмме соответствует значению 13,7-14,2%(ат.) Сu.
Максимальная растворимость Сu в α-Ве равна 9,5%(ат.) при 1090°С и уменьшается с понижением температуры до значений 7,5; 7,0; 6,0 и 4,5% (ат.), соответственно, при 1000, 900, 800 и 700°С. Методом микроскопического анализа ранее были установлены следующие значения растворимости Сu в Be: 7,3; 6,3; 5,2 и 4,6%(ат.), соответственно, при температурах 1100, 1000, 800 и 600°С. Также растворимость Сu в Beизучали, вводя Сu в Be методом ионнойимплантации и отжигом сплавов в интервале температур 320—1290°С. Полученные результаты согласуются с представленными ранее.
Кроме твердых растворов на основе чистых металлов компонентов в системе существуют следующие фазы: β, γ, δ. Фазе β иногда приписывают формулу Cu2
Be, а фазе γ — формулу СuВе, но чаще эти фазы рассматривают как упорядоченные твердые растворы Beв Сu с разной степенью упорядоченности. Фаза β имеет неупорядоченную ОЦК структуру, фаза γ обладает ОЦК структурой типа CsCl. Данные о структуре фазы δ неоднозначны. Структура фазы δ определялась как кубическая, так и гексагональная. Согласно некоторым данным в области существования фазы δ имеются два соединения: СuВе3
и СuВе2
. Соединение СuВе3
имеет гексагональную структуру типа CuZn3
. Соединение СuВе2
обладает кубической решеткой, изотипной MgCu2
. Соединения должны быть разделены гетерогенной областью существования двух фаз (CuBe3
+ CuBe2
), но так как положение соответствующих фазовых границ точно не установлено, на диаграмме состояния эти области показаны штриховыми линиями. То, что соединение СuВе3
имеет гексагональную решетку, вызывает определенные сомнения, так как соединение CuZn3
в системе Сu—Zn обычно рассматривается как фаза δ, существующая только при повышенных температурах и имеющая ОЦК решетку типа CsCl. При температурах, близких к комнатной, составу Cu3
Zn в системе Сu—Zn отвечает двухфазная смесь, состоящая из кубической фазы γ и гексагональной плотноупакованной фазы ε.
Фаза δ плавится конгруэнтно и образует эвтектику с β-Ве при температуре 1150°С и содержании 17,3%(ат.) Сu. Фаза δ имеет широкую область гомогенности, располагающуюся в пределах концентраций Be4
Cu — Be2
Cu, и плавится конгруэнтно при 1219°С. Точка максимума на кривых ликвидуса и солидуса отвечает 22%(ат.) Сu. Предполагается, что фаза на основе Ве3
Сu является метастабильной.
Максимальная растворимость Сu в β-Ве при эвтектической температуре 1199°С составляет 17,3%(ат.), а в α-Ве при эвтектоиднои температуре 1109°С - 9,5% (ат.).
Кристаллическая структура промежуточных фаз указана в табл. 1.3.
Таб. 1.3 Кристаллическая структура соединений системы Be–Cu
| Соединение |
Прототип |
Группа симметрии |
Параметры ячейки, нм |
| a
|
c
|
| β |
W |
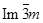
|
0,2798 |
- |
| γ |
CsCl |
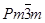 |
0,2689-0,272 |
- |
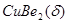 |
MgCu2
|
 |
0,5957-0,5977 |
- |
 |
Mg (?) |
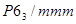 |
0,2555-0,2557 |
0,4178-0,4179 |
1.2Диаграмма состояния Be–Ni [2, c. 592-594].
Обобщённая диаграмма системы бериллий – никель, построенная по результатам работ многих исследователей, приведена на рисунке 1.6.
В сплавах системы образуются две промежуточные фазы переменного состава на основе соединений NiBe и Ni5
Ве21
, указанные фазы плавятся конгруэнтно при 1472 и 1264°С, соответственно. В сплавах кристаллизуются три эвтектики (Ni) + NiBe, NiBe + Ni5
Be21
и Ni5
Be21
+ (β-Ве) при температурах 1157, 1190 и 1240°С, эвтектические точки расположены при содержаниях 23,6; 68,5 и 89% (ат.) Be, соответственно. При температуре 1065°С протекает эвтектоидный распад β-Ве на смесь α-Вс + Ni5
Be21
.
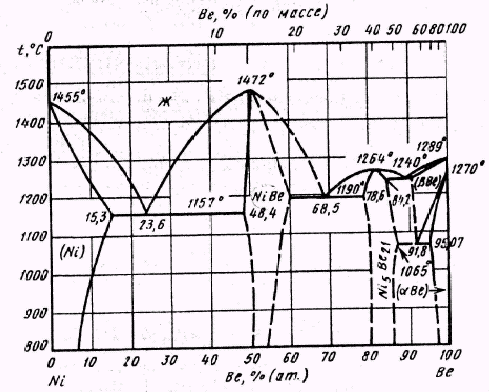
Рис. 1.6 Диаграмма состояния Be-Ni
Эвтектоидная точка расположена при 91,8% (ат.) Be. При температуре 800°С область гомогенности фазы на основе NiBe имеет протяженность около 4% (ат.), а на основе Ni5
Be21
— около 5%(ат.). Ni один из немногих элементов, который значительно снижает температуру полиморфного превращения β-Ве↔α-Ве.
Для растворимости Ni в Be (по данным разных авторов) указаны следующие значения: 5, 4 и 3% (ат.) при температурах 1080, 600 и 500°С, соответственно, а для растворимости Be в Ni: 15,3; 11,7; 7,3; 3,7 и 1,8% (ат.) при температурах 1150, 1000, 800, 600 и 440°С, соответственно. Методом вторичной ионной эмиссии растворимость Ni в Beопределена равной 1,3±0,27%(ат.) при 20°С.
Соединение NiBe(β-фаза) обладает структурой типа CsCl (группа симметрии 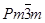 ) с параметром элементарной ячейки (при 49,8% (ат.) Ni) а
=0,2604÷0,2631 нм. Соединение Ni5
Be21
имеет деформированную решетку типа γ-латуни (группа симметрии ) с параметром элементарной ячейки (при 49,8% (ат.) Ni) а
=0,2604÷0,2631 нм. Соединение Ni5
Be21
имеет деформированную решетку типа γ-латуни (группа симметрии 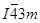 ) с параметром псевдокубической ячейки а
= 0,758 нм при содержании 81,9—82,5% (ат.) Ве. ) с параметром псевдокубической ячейки а
= 0,758 нм при содержании 81,9—82,5% (ат.) Ве.
1.3Диаграмма состояния Cu–Ni [3, c. 283-284].
Диаграмма состояния медь – никель приведена на рисунке 1.7.
В интервале температур 1000—1500°Сисследование проведено с использованием катодной Сu чистотой 99,99%(по массе) и электролитического Ni чистотой 99,95% (по массе) методом микрорентгеноспектрального анализа образцов, закаленных из твердожидкого состояния. Результаты работы хорошо совпадают с данными,
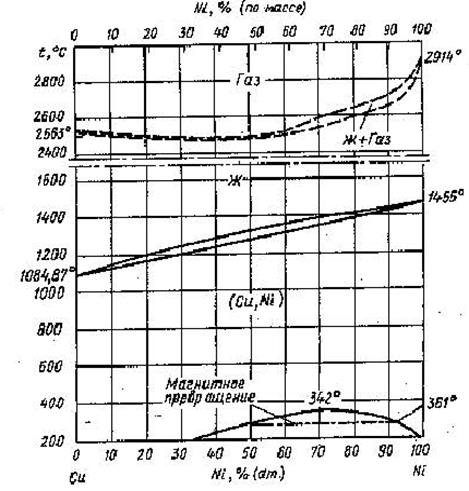
Рис. 1.7 Диаграмма состояния Cu - Ni
полученными методами термического, металлографического и микрорентгеноспектрального анализов в области концентраций 0-100% (ат.) Ni. Система Сu—Ni характеризуется образованием в процессе кристаллизации непрерывного ряда твердых растворов (Си, Ni) с гранецентрированной кубической структурой. По данным спектрального анализа установлено равновесие Ж↔Г с азеотропным минимумом при температуре 2500°С и концентрации 50—60% ;
(ат.) Ni; указывается на наличие области расслоения на две фазы (газообразный и жидкий растворы разного состава) при концентрации 60—100% (ат.) Ni. В интервале концентраций 0—60%(ат.) Ni область расслоения настолько узка, что практически вырождается в прямую линию.
Граница расслаивания твердого раствора и критическая точка несмешиваемости, соответствующая концентрации никеля 69,7% (ат.) и температуре 342°С приведена на основании расчета, проведенного по термодинамическим константам.
1.4Термодинамическое моделирование свойств твёрдых металлических растворов [4, c. 17-20]
Существует 2 способа описания термодинамических свойств растворов – с помощью активностей компонентов и с помощью избыточных термодинамических функций. Эти способы тесно связаны между собой.
Избыточная термодинамическая функция – это положительный или отрицательный избыток какого-либо термодинамического свойства реального раствора над тем же свойством гипотетического идеального раствора при одинаковых значениях параметров. Обозначают их верхними индексами Е.
Если в качестве стандартного состояния выбрать чистый компонент, и концентрации представлять в виде мольных долей, то для компонента s:
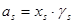 (1.1) (1.1)
Коэффициент активности 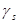 может быть выражен через соответствующий избыточный химический потенциал: может быть выражен через соответствующий избыточный химический потенциал:
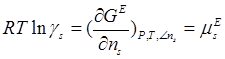 (1.2) (1.2)
Прологарифмировав (1.1) с учётом (1.2) получим:
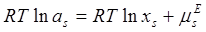 (1.3) (1.3)
Таким образом, для определения активности необходимо знать избыточный химический потенциал (или избыточную энергию Гиббса), а для аналитического представления концентрационной и температурной зависимости термодинамических свойств растворов нужно знать соответствующую зависимость 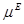 или или 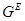 . .
Обычно для описания реальных растворов применяют модель идеального раствора, при этом 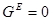 . Однако, в реальном растворе законы Рауля и Генри, а также равенства типа . Однако, в реальном растворе законы Рауля и Генри, а также равенства типа 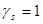 (или (или 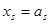 ) выполняются только в чрезвычайно узких диапазонах концентраций при ) выполняются только в чрезвычайно узких диапазонах концентраций при 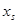 →0, или →0, или 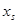 →1 (то есть в бесконечно разбавленных растворах). →1 (то есть в бесконечно разбавленных растворах).
Существует теория, включающая в себя понятия «идеальный» и «предельно разбавленный» растворы, как частные случаи. Это обобщённая теория «регулярных» растворов (далее – ОТРР). С её позиций области, в которых реальный раствор является регулярным (так называемые области «граничной регулярности») располагаются также по краям диапазона концентраций, но они существенно шире.
Регулярным называется модельный раствор, при образовании которого может выделяться или поглощаться теплота, но не изменяется объём, а энтропия смешения компонентов которого равна энтропии смешения идеальных газов.
Для регулярного раствора, состоящего из m компонентов, в рамках ОТРР выполняется соотношение:
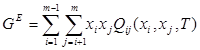 (1.4) (1.4)
Здесь 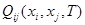 - энергия смешения. Для идеального раствора - энергия смешения. Для идеального раствора 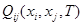 =0, а в областях граничной регулярности энергия смешения не зависит от мольных долей компонентов. =0, а в областях граничной регулярности энергия смешения не зависит от мольных долей компонентов.
Если в 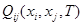 отдельно выделить концентрационно зависимую составляющую и разложить её в ряд Тейлора, то получится уравнение: отдельно выделить концентрационно зависимую составляющую и разложить её в ряд Тейлора, то получится уравнение:
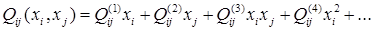 (1.5) (1.5)
При этом каждое из слагаемых в правой части будет зависеть от температуры.
Как показывает математическая обработка экспериментальных данных, для бинарных растворов достаточно первых трёх параметров 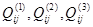 , чтобы в большинстве случаев корректно аппроксимировать термодинамические функции смешения системы. При этом , чтобы в большинстве случаев корректно аппроксимировать термодинамические функции смешения системы. При этом 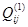 - энергия смешения компонентов i и j в растворе на основе компонента i, - энергия смешения компонентов i и j в растворе на основе компонента i,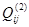 - энергия смешения компонентов i и j в растворе на основе компонента j. Обе эти величины – это термодинамические характеристики областей граничной регулярности двойной системы. А - энергия смешения компонентов i и j в растворе на основе компонента j. Обе эти величины – это термодинамические характеристики областей граничной регулярности двойной системы. А 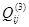 - это параметр, учитывающий отклонение от регулярности вне этих областей. - это параметр, учитывающий отклонение от регулярности вне этих областей.
В рамках данной работы принято считать растворы регулярными во всём диапазоне концентраций и принимать 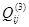 =0. С учётом этого, выражение для химического потенциала компонента s в растворе, содержащем m компонентов, запишется так: =0. С учётом этого, выражение для химического потенциала компонента s в растворе, содержащем m компонентов, запишется так:
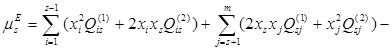
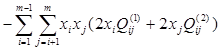 (1.6) (1.6)
Формулы ОТРР позволяют успешно описывать термодинамические свойства металлических, неметаллических и смешанных систем.
2. Расчётная часть
Как уже было сказано ранее, бериллиевая бронза БрБ2 содержит в своём составе (по массе) 97,5% Cu, 0,5% Ni, 2% Be.
Если условно обозначить медь, как компонент 1, никель, как компонент 2 и бериллий, как компонент 3, то можно для каждого компонента этой тройной системы переписать уравнение (1.3), подставив в него уравнение (1.6) в следующем виде:
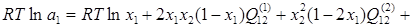
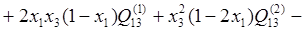
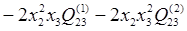 (2.1) (2.1)
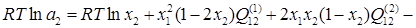
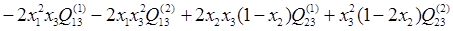 (2.2) (2.2)
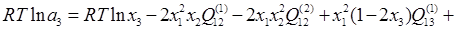
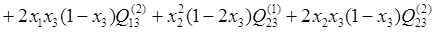 (2.3) (2.3)
Для определения активностей компонентов бронзы при 25°С необходимо установить температурные зависимости энергий смешения Q в низкотемпературном интервале. Для этого можно использовать диаграммы состояния бинарных систем.
Для систем Be – Cu и Be – Ni такие зависимости были получены предшествующими исследователями. В данной работе будет выполнен анализ зависимостей для системы Cu – Ni.
2.1 Расчёт зависимости энергий смешения компонентов системы Cu – Ni от температуры
Рассмотрим низкотемпературную часть диаграммы Cu – Ni (см. рис. 1.7). Ниже линии солидуса образуется ряд непрерывных твёрдых растворов с решёткой ГЦК. Однако при температурах ниже 342°С наблюдается купол расслаивания на твёрдый раствор на основе меди (обозначим его, как α-фазу) и твёрдый раствор на основе никеля (обозначим его, как γ-фазу). Внутри купола находится смесь этих фаз.
На границе купола α-фаза находится в равновесии с γ-фазой. Это можно записать следующими уравнениями:
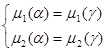 (2.4) (2.4)
Для любого из компонентов 1 и 2 и в α- и в γ-фазе справедливо соотношение:
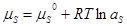 (2.5) (2.5)
Обе фазы имеют одинаковую структуру (ГЦК). Это можно объяснить высоким сродством меди и никеля. На диаграмме состояния (рис. 1.7) видно, что сплав плавится конгруэнтно во всём диапазоне концентраций. Более того, линии ликвидуса и солидуса расположены очень близко друг к другу, то есть плавление происходит почти в изотермических условиях, как у чистого металла. Аналогично происходит и испарение сплава.
На основании этого можно записать, что:
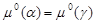 (2.6) (2.6)
Тогда система (2.4) перепишется в виде:
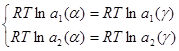 (2.7) (2.7)
Обозначим через х мольные доли компонентов в α-фазе, а через N – мольные доли компонентов в γ-фазе, и учитывая условия нормировки их на единицу, можно систему уравнений (2.7) с учётом (1.3) и (1.6) переписать в следующем виде:
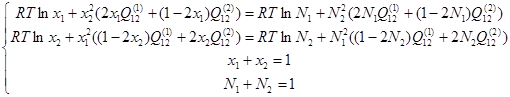 (2.8) (2.8)
Если бы были известны мольные доли x и N при 25°С, то можно было бы с помощью (2.8) непосредственно вычислить значения Q при этой температуре. Однако при столь низкой температуре невозможно получить экспериментальных данных о координатах купола расслаивания. Дело в том, что наступление равновесия между фазами происходит, благодаря диффузии атомов, а в комнатных условиях она протекала бы экстремально долго (несколько сотен лет). Поэтому необходимо изучить температурную зависимость энергий смешения и экстраполировать её на уровень комнатных температур.
Если T=const и известны все x и N, то система уравнений (2.8) линейна относительна параметров Q и может быть решена аналитически.
Обозначим 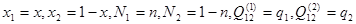 . Если теперь перенести правую часть системы (2.8) в левую, то она перепишется в виде: . Если теперь перенести правую часть системы (2.8) в левую, то она перепишется в виде:
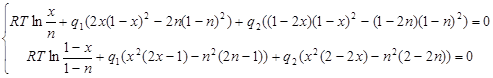 (2.9) (2.9)
Выразим 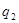 из первого уравнения системы (2.9): из первого уравнения системы (2.9):
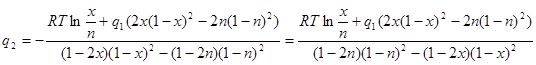 (2.10) (2.10)
Подставим (2.10) во второе уравнение системы (2.9):
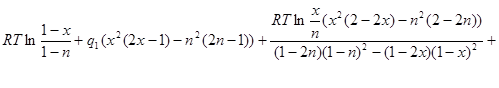
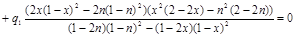 (2.11) (2.11)
Теперь можно выразить в явном виде величину 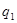 : :
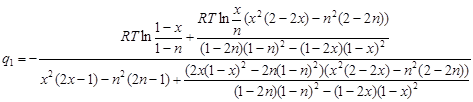 (2.12) (2.12)
Теперь приведём выражения в числителе и знаменателе дроби (2.12) к общему знаменателю:
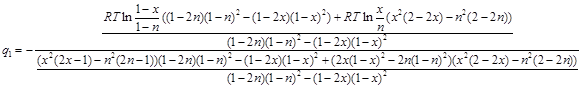
(2.13)
Умножив числитель и знаменатель дроби (2.13) на выражение 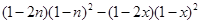 , окончательно получим: , окончательно получим:

(2.14)
Система уравнений (2.9) не имеет степеней свободы, поэтому случайная погрешность отсутствует. Возможно, пользуясь законом накопления ошибок, определить систематическую погрешность и рассчитать доверительный интервал для значений Q. В данной работе это не учитывается.
Координаты купола расслаивания при различных температурах были сняты с диаграммы состояния Cu – Ni (рис. 1.7) и представлены в таблице 2.1.
Табл. 2.1. Координаты купола расслаивания твёрдого раствора при разных температурах.
| t, o
C |
Состав α-фазы (Cu) |
Состав γ-фазы (Ni) |
| x1
|
x2
|
N1
|
N2
|
| 200 |
0,650 |
0,350 |
0,013 |
0,987 |
| 225 |
0,633 |
0,367 |
0,027 |
0,973 |
| 250 |
0,580 |
0,420 |
0,053 |
0,947 |
| 275 |
0,513 |
0,487 |
0,073 |
0,927 |
| 300 |
0,467 |
0,533 |
0,113 |
0,887 |
| 325 |
0,387 |
0,613 |
0,187 |
0,813 |
| 342 |
0,300 |
0,700 |
0,300 |
0,700 |
Для каждой из температур были проведены вычисления значений энергий смешения. 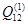 вычислены по формуле (2.14), а вычислены по формуле (2.14), а 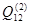 при известной при известной 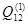 по формуле (2.10). Для вычислений была использована компьютерная программа, текст которой приведён в приложении А. по формуле (2.10). Для вычислений была использована компьютерная программа, текст которой приведён в приложении А.
Результаты вычислений приведены в таблице 2.2, а график температурной зависимости энергий смешения – на рисунке 2.1.
Табл. 2.2. Значения энергий смешения компонентов системы Cu – Ni при разных температурах
| T, K |
Q12
(1)
, Дж
/моль
|
Q12
(2)
, Дж
/моль
|
| 473 |
-3197,734 |
15175,28 |
| 498 |
-465,2206 |
13963,91 |
| 523 |
642,8817 |
12621,02 |
| 548 |
-507,406 |
11923,95 |
| 573 |
870,6937 |
11582,78 |
| 598 |
2055,722 |
11269,64 |
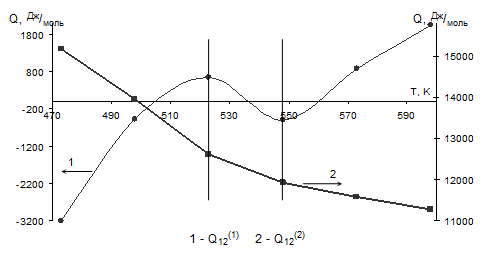
Рис. 2.1. Зависимости энергий смешения компонентов системы Cu – Ni от температуры.
2.2 Расчёт купола расслаивания твёрдого раствора Cu–Ni
Для проверки адекватности модели, использованной при решении, а следовательно и правильности определения значений энергий смешения необходимо решить обратную задачу – по известным температурным зависимостям величин Q рассчитать координаты купола расслаивания и сравнить его со снятым с диаграммы состояния. Фактически, необходимо решить систему относительно x, N и T.
В соответствии с правилом фаз Гиббса, система Cu – Ni имеет одну степень свободы. Это означает, что только один из параметров x, N, T является независимым. Для однозначного решения необходимо задавать один параметр и, решая систему (2.8), находить остальные.
Для учёта зависимостей 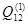 и и 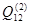 от температуры необходимо провести аппроксимацию этих функций полиномами. В рамках этой работы было проверено два способа аппроксимации. от температуры необходимо провести аппроксимацию этих функций полиномами. В рамках этой работы было проверено два способа аппроксимации.
Способ №1.
Результаты аппроксимации зависимостей Q=f(T) представлены в таблице 2.3. Там же приведены значения полученных коэффициентов достоверности аппроксимации (квадратов коэффициентов корреляции).
Табл. 2.3. Аппроксимация зависимостей Q=f(T).
| Линия |
Полином |
R2
|
| 1 |
Q = 33,285T - 17925 |
0,7556 |
| Q = -0,1902T2
+ 237T - 72123 |
0,7885 |
| Q = 0,0128T3
- 20,674T2
+ 11166T - 2E+06 |
0,9489 |
| Q = -0,0001T4
+ 0,2512T3
- 211,76T2
+ 79045T - 1E+07 |
0,9586 |
| Q = -1E-05T5
+ 0,0294T4
- 31,331T3
+ 16641T2
- 4E+06T + 5E+08 |
1 |
| 2 |
Q = -31,278T + 29506 |
0,9218 |
| Q = 0,2428T2
- 291,32T + 98689 |
0,9959 |
Видно, что для линии 1 высоких значений R2
удаётся достичь только при больших степенях полинома. К сожалению, при этом не очень точно вычисляются их коэффициенты. К тому же, с такими зависимостями трудно работать. Всё это послужило причиной того, что от данного способа автор работы отказался.
Способ №2.
Было принято решение разделить функции на три части соответствующие температурам 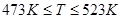 для первой части, для первой части, 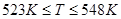 для второй и для второй и 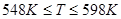 для третьей (на рис. 2.1 эти части разделены вертикальными прямыми). На каждом из этих отрезков зависимость можно аппроксимировать полиномом меньшей степени. Результаты приведены в таблице 2.4. для третьей (на рис. 2.1 эти части разделены вертикальными прямыми). На каждом из этих отрезков зависимость можно аппроксимировать полиномом меньшей степени. Результаты приведены в таблице 2.4.
Табл. 2.4. Аппроксимация частей зависимости Q=Q(T).
| Линия |
Часть |
Полином |
R2
|
| 1 |
1 |
Q = 76,812T - 39259 |
0,9437 |
| Q = -1,2995T2
+ 1371,1T - 361006 |
1 |
| 2 |
Q = -46,012T + 24707 |
1 |
| 3 |
Q = 51,263T - 28567 |
0,9981 |
| Q = -0,1545T2
+ 228,27T - 79216 |
1 |
| 2 |
1 |
Q = -51,085T + 39360 |
0,9991 |
| Q = -0,1052T2
+ 53,71T + 13310 |
1 |
| 2 |
Q = -27,883T + 27204 |
1 |
| 3 |
Q = -13,086T + 19091 |
0,9994 |
| Q = 0,0224T2
- 38,784T + 26444 |
1 |
Задав таким образом зависимости Q=f(T) как полиномы второй степени и зафиксировав один из параметров x, N, T, нужно решить систему (2.8). В этом случае система будет состоять из двух трансцендентных уравнений, и решить их совместно можно только численными методами. Автору работы не удалось этого сделать.
Поэтому было принято решение пожертвовать точностью аппроксимации функций Q=f(T) и определить их как линейные зависимости. В этом случае Q=aT+b и температура будет входить в уравнения системы (2.8) только в первой степени, что позволяет исключить её, как неизвестное.
Воспользуемся условными обозначениями, которые уже были использованы ранее.
Пусть 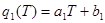 , а , а  . Тогда первое уравнение системы (2.9) запишется в виде: . Тогда первое уравнение системы (2.9) запишется в виде:
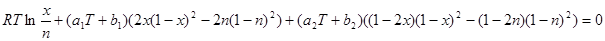 (2.15) (2.15)
Если перенести все слагаемые, содержащие Т, в левую часть, а все остальные – в правую часть уравнения, то получится:
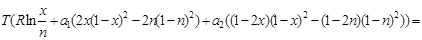
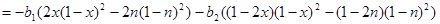 (2.16) (2.16)
Осталось только выразить температуру в явном виде:
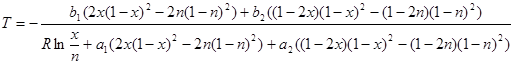 (2.17) (2.17)
Аналогично нужно выразить температуру и из второго уравнения системы (2.9):
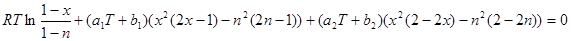 (2.18) (2.18)
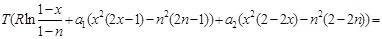
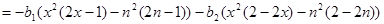 (2.19) (2.19)
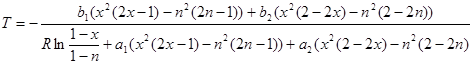 (2.20) (2.20)
Приравняв правые части равенств (2.17) и (2.20) и умножив их на -1, приведём уравнение к окончательному виду:
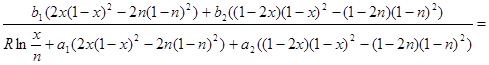
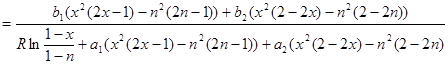 (2.21) (2.21)
Параметра а
и b
определим из данных таблицы 2.4. Чтобы решить трансцендентное уравнение (2.21), нужно задаться одним из параметров x, или n и численными методами подобрать второй параметр, а затем определить и температуру по любому из уравнений (2.17) или (2.20).
Для решения была использована надстройка «поиск решения» пакета MicrosoftExcel. Результаты решения представлены в таблице 2.5.
Табл. 2.5. Рассчитанный купол расслаивания твёрдого раствора при разных температурах
| t, o
C |
Состав α-фазы (Cu) |
Состав γ-фазы (Ni) |
| x1
|
x2
|
N1
|
N2
|
| 0 |
0,727 |
0,273 |
2,8E-06 |
0,999997 |
| 25 |
0,723 |
0,277 |
0,000014 |
0,999986 |
| 40 |
0,72 |
0,28 |
0,000035 |
0,999965 |
| 83 |
0,71 |
0,29 |
0,00027 |
0,99973 |
| 116 |
0,70 |
0,30 |
0,001 |
0,999 |
| 141 |
0,69 |
0,31 |
0,002 |
0,998 |
| 161 |
0,68 |
0,32 |
0,004 |
0,996 |
| 178 |
0,67 |
0,33 |
0,007 |
0,993 |
| 191 |
0,66 |
0,34 |
0,010 |
0,990 |
| 203 |
0,65 |
0,35 |
0,014 |
0,986 |
| 241 |
0,60 |
0,40 |
0,042 |
0,958 |
| 261 |
0,55 |
0,45 |
0,061 |
0,939 |
| 279 |
0,50 |
0,50 |
0,077 |
0,923 |
| 307 |
0,45 |
0,55 |
0,128 |
0,872 |
| 322 |
0,40 |
0,60 |
0,174 |
0,826 |
| 331 |
0,35 |
0,65 |
0,224 |
0,776 |
| 334 |
0,30 |
0,70 |
0,273 |
0,727 |
| 334 |
0,285 |
0,715 |
0,285 |
0,715 |
Сравнение данных таблиц 2.1 и 2.5 можно провести визуально, нанеся данные на один график. Сравнение проведено на рисунке 2.2.
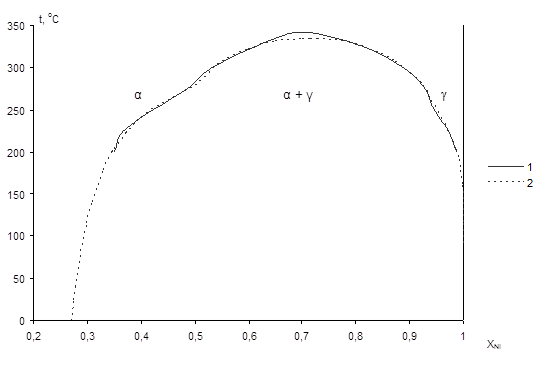
Рис. 2.2 Экспериментальный (1) и расчётный (2) купол расслаивания твёрдого раствора Cu – Ni
Из рисунка 2.2 видно, что экспериментальный и расчётный купол расслаивания твёрдого раствора Cu – Ni близки. По экспериментальным данным, критическая температура несмешиваемости равна 334°С.
Это позволяет говорить о том, что температурная зависимость Q=f(T) рассчитана правильно, и экстраполировать её до области комнатных температур.
2.3 Вычисление термодинамических активностей меди и никеля в бинарной системе при 25°С
Воспользовавшись уравнениями для Q=f(T) из таблицы 2.4, с использованием уравнений (1.3) и (1.6) можно рассчитать активности меди и никеля в твёрдом растворе Cu – Ni в зависимости от мольного содержания компонентов в нём.
Для расчётов использована компьютерная программа, текст которой представлен в приложении Б. Результаты представлены в таблице 2.6.
Табл. 2.6 Активности меди и никеля в бинарной системе при 25°С
| xCu
|
xNi
|
aCu
|
aNi
|
xCu
|
xNi
|
aCu
|
aNi
|
| 0,01 |
0,99 |
101,71 |
0,99 |
0,51 |
0,49 |
0,10 |
5,67 |
| 0,02 |
0,98 |
123,44 |
0,99 |
0,52 |
0,48 |
0,10 |
5,60 |
| 0,03 |
0,97 |
114,02 |
0,99 |
0,53 |
0,47 |
0,10 |
5,51 |
| 0,04 |
0,96 |
94,98 |
1,00 |
0,54 |
0,46 |
0,10 |
5,38 |
| 0,05 |
0,95 |
75,24 |
1,01 |
0,55 |
0,45 |
0,10 |
5,23 |
| 0,06 |
0,94 |
58,02 |
1,03 |
0,56 |
0,44 |
0,11 |
5,05 |
| 0,07 |
0,93 |
44,11 |
1,05 |
0,57 |
0,43 |
0,11 |
4,84 |
| 0,08 |
0,92 |
33,30 |
1,07 |
0,58 |
0,42 |
0,11 |
4,62 |
| 0,09 |
0,91 |
25,08 |
1,10 |
0,59 |
0,41 |
0,12 |
4,37 |
| 0,10 |
0,90 |
18,91 |
1,13 |
0,60 |
0,40 |
0,12 |
4,11 |
| 0,11 |
0,89 |
14,30 |
1,17 |
0,61 |
0,39 |
0,13 |
3,84 |
| 0,12 |
0,88 |
10,86 |
1,21 |
0,62 |
0,38 |
0,14 |
3,56 |
| 0,13 |
0,87 |
8,30 |
1,26 |
0,63 |
0,37 |
0,14 |
3,27 |
| 0,14 |
0,86 |
6,38 |
1,31 |
0,64 |
0,36 |
0,15 |
2,98 |
| 0,15 |
0,85 |
4,94 |
1,37 |
0,65 |
0,35 |
0,16 |
2,70 |
| 0,16 |
0,84 |
3,86 |
1,43 |
0,66 |
0,34 |
0,17 |
2,42 |
| 0,17 |
0,83 |
3,03 |
1,50 |
0,67 |
0,33 |
0,18 |
2,16 |
| 0,18 |
0,82 |
2,41 |
1,58 |
0,68 |
0,32 |
0,19 |
1,90 |
| 0,19 |
0,81 |
1,92 |
1,66 |
0,69 |
0,31 |
0,20 |
1,66 |
| 0,20 |
0,80 |
1,55 |
1,75 |
0,70 |
0,30 |
0,21 |
1,44 |
| 0,21 |
0,79 |
1,26 |
1,84 |
0,71 |
0,29 |
0,23 |
1,24 |
| 0,22 |
0,78 |
1,04 |
1,95 |
0,72 |
0,28 |
0,24 |
1,05 |
| 0,23 |
0,77 |
0,86 |
2,06 |
0,73 |
0,27 |
0,26 |
0,88 |
| 0,24 |
0,76 |
0,72 |
2,17 |
0,74 |
0,26 |
0,28 |
0,73 |
| 0,25 |
0,75 |
0,60 |
2,30 |
0,75 |
0,25 |
0,30 |
0,60 |
| 0,26 |
0,74 |
0,51 |
2,43 |
0,76 |
0,24 |
0,32 |
0,49 |
| 0,27 |
0,73 |
0,44 |
2,57 |
0,77 |
0,23 |
0,34 |
0,40 |
| 0,28 |
0,72 |
0,38 |
2,72 |
0,78 |
0,22 |
0,36 |
0,31 |
| 0,29 |
0,71 |
0,33 |
2,87 |
0,79 |
0,21 |
0,39 |
0,25 |
| 0,30 |
0,70 |
0,29 |
3,03 |
0,80 |
0,20 |
0,41 |
0,19 |
| 0,31 |
0,69 |
0,26 |
3,20 |
0,81 |
0,19 |
0,44 |
0,15 |
| 0,32 |
0,68 |
0,23 |
3,37 |
0,82 |
0,18 |
0,47 |
0,11 |
| 0,33 |
0,67 |
0,21 |
3,55 |
0,83 |
0,17 |
0,50 |
0,08 |
| 0,34 |
0,66 |
0,19 |
3,73 |
0,84 |
0,16 |
0,53 |
0,06 |
| 0,35 |
0,65 |
0,17 |
3,91 |
0,85 |
0,15 |
0,57 |
0,04 |
| 0,36 |
0,64 |
0,16 |
4,09 |
0,86 |
0,14 |
0,60 |
0,03 |
| 0,37 |
0,63 |
0,15 |
4,28 |
0,87 |
0,13 |
0,63 |
0,02 |
| 0,38 |
0,62 |
0,14 |
4,46 |
0,88 |
0,12 |
0,67 |
0,02 |
| 0,39 |
0,61 |
0,13 |
4,64 |
0,89 |
0,11 |
0,70 |
0,01 |
| 0,40 |
0,60 |
0,12 |
4,81 |
0,90 |
0,10 |
0,74 |
0,01 |
| 0,41 |
0,59 |
0,11 |
4,98 |
0,91 |
0,09 |
0,77 |
0,00 |
| 0,42 |
0,58 |
0,11 |
5,13 |
0,92 |
0,08 |
0,81 |
0,00 |
| 0,43 |
0,57 |
0,11 |
5,27 |
0,93 |
0,07 |
0,84 |
0,00 |
| 0,44 |
0,56 |
0,10 |
5,40 |
0,94 |
0,06 |
0,87 |
0,00 |
| 0,45 |
0,55 |
0,10 |
5,51 |
0,95 |
0,05 |
0,90 |
0,00 |
| 0,46 |
0,54 |
0,10 |
5,60 |
0,96 |
0,04 |
0,93 |
0,00 |
| 0,47 |
0,53 |
0,10 |
5,66 |
0,97 |
0,03 |
0,95 |
0,00 |
| 0,48 |
0,52 |
0,10 |
5,70 |
0,98 |
0,02 |
0,97 |
0,00 |
| 0,49 |
0,51 |
0,10 |
5,72 |
0,99 |
0,01 |
0,99 |
0,00 |
| 0,50 |
0,50 |
0,10 |
5,71 |
2.4 Вычисление термодинамических активностей компонентов бронзы БрБ2 при 25°С
Для расчёта активностей нужно воспользоваться формулами (2.1), (2.2) и (2.3). Мольные доли компонентов рассчитываются из известных массовых долей.
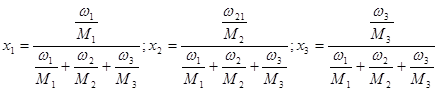 (2.22) (2.22)
Здесь ω – массовая доля, M – молярная масса компонента.
Данные о значениях энергий смешения системы Cu – Ni при 25°С получены из таблицы 2.4, для систем Be – Cu и Be – Ni они предоставлены предшествующими исследователями:
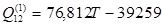 (2.23) (2.23)
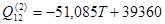 (2.24) (2.24)
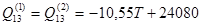 (2.25) (2.25)
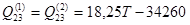 (2.26) (2.26)
Расчёты проведены с помощью компьютерной программы, текст которой приведён в приложении В.
Получены следующие результаты:
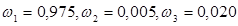 (2.27) (2.27)
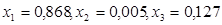 (2.28) (2.28)
 (2.29) (2.29)
Выводы
По результатам данной работы были установлены температурные зависимости энергий смешения твёрдого раствора системы Cu – Ni. Их правильность была доказана тем, что купол расслаивания твёрдого раствора, рассчитанный на основании этих зависимостей, практически совпал с экспериментальным. Это позволило экстраполировать купол расслаивания и зависимости Q=f(T) до области комнатных температур.
Были определены активности меди и никеля в твёрдом растворе при 25°С в зависимости от мольного содержания компонентов. При некоторых содержаниях активности оказались больше единицы. Это свидетельствует о расслоении твёрдого раствора на несколько фаз, возможно, интерметаллических.
Наконец, были определены активности компонентов бронзы БрБ2, содержащей бериллий, медь и никель. Эта бронза представляет из себя переохлаждённый раствор и является метастабильной. Это подтверждается тем, что активность бериллия оказалась больше единицы. Происходит выпадение бериллия в отдельную фазу из раствора, или образование интерметаллидов.
Рассчитанные активности будут использованы в дальнейшем для моделирования термодинамических свойств бериллиевой бронзы.
Приложения
Приложение А
Программа для расчёта энергий смешения состоит из двух частей. Первая часть – дополнительная, она готовит файл данных с координатами купола расслаивания, снятыми с диаграммы состояния. Текстприведённиже:
10 OPEN "source.txt" FOR OUTPUT AS #1
20 FOR i = 1 TO 6
30 READ t, x, n
40 REM 't'-температура, 'x' и 'n'-мольные доли меди в двух фазах
50 PRINT #1, (t + 273), x, n
60 NEXT i
70 CLOSE #1
80 DATA 200, 0.650, 0.013
90 DATA 225, 0.633, 0.027
100 DATA 250, 0.580, 0.053
110 DATA 275, 0.513, 0.073
120 DATA 300, 0.467, 0.113
130 DATA 325, 0.387, 0.187
140 END
Вторая часть – основная, именно она рассчитывает энергии смешения и выводит их в файл данных.
10 CLS : REM программа для расчёта энергий смешения
20 DIM t(6), x(6), n(6), q(6), r(6)
30 REM 't'-температура,'x' и 'n'-мольные доли
40 REM 'q' и 'r'-члены разложенной в ряд Тейлора энергии смешения
50 OPEN "source.txt" FOR INPUT AS #1
60 FOR i = 1 TO 6: REM вводисходныхданных
70 INPUT #1, t(i), x(i), n(i)
80 NEXT i
90 CLOSE #1
100 OPEN "Q.txt" FOR OUTPUT AS #1
110 FOR i = 1 TO 6: REM расчёт Q12(1) и Q12(2)
120 LET t = t(i): LET x = x(i): LET n = n(i)
130 LET a = 8.3144 * t * LOG((1 - x) / (1 - n)) * ((1 - 2 * n) * (1 - n) ^ 2 - (1 - 2 * x) * (1 - x) ^ 2)
140 LET b = 8.3144 * t * LOG(x / n) * (x ^ 2 * (2 - 2 * x) - n ^ 2 * (2 - 2 * n))
150 LET c = (x ^ 2 * (2 * x - 1) - n ^ 2 * (2 * n - 1)) * ((1 - 2 * n) * (1 - n) ^ 2 - (1 - 2 * x) * (1 - x) ^ 2)
160 LET d = (2 * x * (1 - x) ^ 2 - 2 * n * (1 - n) ^ 2) * (x ^ 2 * (2 - 2 * x) - n ^ 2 * (2 - 2 * n))
170 LET q = -(a + b) / (c + d): REM q=Q12(1)
180 LET e = 8.3144 * t * LOG(x / n) + q * (2 * x * (1 - x) ^ 2 - 2 * n * (1 - n) ^ 2)
190 LET f = ((1 - 2 * n) * (1 - n) ^ 2 - (1 - 2 * x) * (1 - x) ^ 2)
200 LET r = e / f: REM r=Q12(2)
210 LET q(i) = q
220 LET r(i) = r
230 PRINT #1, t(i), q(i), r(i)
240 NEXT i
250 CLOSE #1
260 END
ПриложениеБ
Текст программы для расчёта активностей в двойной системе приведён ниже:
10 CLS : REM программа для расчёта активностей меди и никеля
20 LET r = 8.3144: REM универсальная газовая константа
30 LET t = 298: REM температура 25 С = 298 К
40 LET q1 = -16369.02: REM Q12(1) при 25 С
50 LET q2 = 24136.67: REM Q12(2) при 25 С
60 OPEN "activ.txt" FOR OUTPUT AS #1
70 PRINT #1, "x1", "x2", "a1", "a2"
80 FOR x = .01 TO .99 STEP .01
90 REM x = x1 - мольная доля меди
100 LET y = 1 - x: REM y = x2 - мольная доля никеля
110 LET z1 = r * t * LOG(x) + (y ^ 2) * (2 * x * q1 + (1 - 2 * x) * q2)
120 LET z2 = r * t * LOG(y) + (x ^ 2) * ((1 - 2 * y) * q1 + 2 * y * q2)
130 REM z1 = RTln a1 и z2 = RTln a2
140 LET a1 = EXP(z1 / (r * t)): REM активность меди
150 LET a2 = EXP(z2 / (r * t)): REM активность никеля
160 PRINT #1, x, y, a1, a2
170 NEXT x
180 CLOSE #1
190 END
Приложение В
Текст программы для расчёта активностей в тройной системе приведён ниже:
10 CLS
20 LET r = 8.3144: REM r - универсальная газовая постоянная
30 LET t = 298: REM t - температура, 25 С = 298 К
40 LET rt = r * t: REM RT
50 REM 1 - Cu, 2 - Ni, 3 - Be
60 LET x1 = .868: LET x2 = .005: LET x3 = .127: REM мольныедоливбронзеБрБ2
70 DIM q1(3, 3): DIM q2(3, 3)
80 REM элементмассива q1(i,j) - это Qij(1) притемпературе t
90 REM элемент массива q2(i,j) - это Qij(2) при температуре t
100 LET q1(1, 2) = 76.812 * t - 39259
110 LET q2(1, 2) = -51.085 * t + 39360
120 LET q1(1, 3) = -10.55 * t + 24080
130 LET q2(1, 3) = q1(1, 3)
140 LET q1(2, 3) = 18.25 * t - 34260
150 LET q2(2, 3) = q1(2, 3)
160 REM вычисление z1=RTln a1
170 LET z1 = rt * LOG(x1) + 2 * x1 * x2 * (1 - x1) * q1(1, 2) + (x2 ^ 2) * (1 - 2 * x1) * q2(1, 2)
180 LET z1 = z1 + 2 * x1 * x3 * (1 - x1) * q1(1, 3) + (x3 ^ 2) * (1 - 2 * x1) * q2(1, 3)
190 LET z1 = z1 - 2 * x2 * x2 * x3 * q1(2, 3) - 2 * x2 * x3 * x3 * q2(2, 3)
200 REM вычисление z2=RTln a2
210 LET z2 = rt * LOG(x2) + 2 * x1 * x2 * (1 - x2) * q2(1, 2) + (x1 ^ 2) * (1 - 2 * x2) * q1(1, 2)
220 LET z2 = z2 + 2 * x2 * x3 * (1 - x2) * q1(2, 3) + (x3 ^ 2) * (1 - 2 * x2) * q2(2, 3)
230 LET z2 = z2 - 2 * x1 * x1 * x3 * q1(1, 3) - 2 * x1 * x3 * x3 * q2(1, 3)
240 REM вычисление z3=RTln a3
250 LET z3 = rt * LOG(x3) + 2 * x1 * x3 * (1 - x3) * q2(1, 3) + (x1 ^ 2) * (1 - 2 * x3) * q1(1, 3)
260 LET z3 = z3 + 2 * x2 * x3 * (1 - x3) * q2(2, 3) + (x2 ^ 2) * (1 - 2 * x3) * q1(2, 3)
270 LET z3 = z3 - 2 * x1 * x1 * x2 * q1(1, 2) - 2 * x1 * x2 * x2 * q2(1, 2)
280 REM вычисление активностей
290 LET a1 = EXP(z1 / rt)
300 LET a2 = EXP(z2 / rt)
310 LET a3 = EXP(z3 / rt)
320 PRINT a1, a2, a3
330 END
Список использованной литературы
1. Лахтин Ю.М., Леонтьева В.П. Материаловедение. Учеб. для вузов., 3-е изд., М: Машиностроение, 1990, 512 с.
2. Диаграммы состояния двойных металлических систем., Под ред. Лякишева Н.П., т.1., М: Машиностроение, 1996, 673 с.
3. Диаграммы состояния двойных металлических систем., Под ред. Лякишева Н.П., т.2., М: Машиностроение, 1997, 485 с.
4. Тюрин А.Г. Моделирование термодинамических свойств растворов. Учебное пособие., ЧелГУ, 1997, 74 с.
Размещено на http://www.
|