1. Гигиенические нормативы содержания фтора в питьевой воде
Фтор как весьма активный в биологическом отношении микроэлемент с начала 30-х годов нынешнего столетия привлек особое внимание гигиенистов, стоматологов, токсикологов, химиков, геохимиков и других специалистов. Интерес к фтору начал проявляться с 1931 г., когда было доказано, что причиной эпидемий "пятнистой эмали" зубов является повышенное содержание фтора в питьевой воде. Это открытие стимулировало изучение эндемического флюроза во всем мире. В изучение проблемы эндемического кариеса и флюороза большой вклад внесли русские исследователи С. Н. Черкинский, Т. А. Николаева, В. А. Книжников, Р. Д. Габович и др. Выяснилось, что противокариесное действие оптимальных концентраций фтора распространяется как на молочные, так и на постоянные зубы, а также на все возрастные группы населения. Эти сведения позволили утверждать о целесообразности искусственного обогащения питьевой воды фтором. Фторирование воды началось осуществляться с 1945 г., применявшиеся другие методы профилактики кариеса зубов не имели успеха и заболеваемость населения кариесом непрерывно росла. С 1957 г. впервые в истории развития водоснабжения в нашей стране началось фторирование воды в г. Норильске, рассматриваемое как мера профилактики заболеваний кариесом зубов.
Как указывалось выше, оптимальной концентрацией фтора в питьевой воде является 0,7...1,2 мг/л. Болеее низкие концентрации фтора принимают при фторировании в южных районах и в летний период, когда количество воды, поступающей в организм человека, увеличивается. Более высокие концентрации фтора принимают при фторировании воды в северных районах и в зимний период, т. е. при более низкой температуре окружающей среды. Необходимость фторирования определяется содержанием фтора в воде источников в количестве менее 0,5 мг/л. Согласно ГОСТ 2874—82 концентрация в воде фторид-ионов не Должна превышать 1,5 мг/л.
Концентрация фторид-ионов в природных водах нашей планеты варьирует в широких пределах — от 0,01 до 50—100 мг/л (Кения), в природных водах России от 0,01 до 8 мг/л. Низкие концентрации фторид-ионов встречаются в большинстве поверхностных источников водоснабжения. И лишь в открытых водоемах Южного Урала, Западной Сибири концентрация фторид- ионов достигает 11 мг/л.
Реклама

Подземные воды (артезианские, колодезные) богаче фторид-ионами, чем поверхностные, и среди них чаще встречаются источники с концентрацией фторид-ионов, превышающей предельно допустимую (1,5 мг/л). Однако, и среди этих источников 68—89% в России содержат менее 0,5 мг/л фторид-ионов.
Свыше 85% воды в города России подается из рек, причем содержание фторид-ионов в воде этих источников, превышающее 0,4 мг/л, встречается в редких случаях, да и это количество после обработки воды на очистных сооружениях снижается до предельно низкой величины. Поэтому вполне понятна та забота, которую проявляет наше государство по обеспечению населения качественной водой.
2. Технология фторирования воды
Для фторирования питьевой воды может быть использован ряд фторсодержащих соединений, таких как кремнефтористый натрий NaSiFe, кремнефтористая кислота H2
SiF6
, фтористый, натрийNaF, кремнефтористый аммоний[(NH4
)2
SiF6
, фтористый кальцийCaF6
, фтористоводородная кислотаHF, кремнефтористый калий K2
SiF6
, кремнефтористый алюминийк, фтористый алюминийAIF3
и ряд других (табл. 16.1).
В США и Канаде применяют для фторирования питьевой воды на 60% действующих установок кремнефтористый натрий, на 25% — кремнефтористоводородную кислоту, на 13% —фтористый натрий и только на 2% установок применяют кремнефтористый аммоний, фтористый кальций, фтористоводородную кислоту и другие соединения. В отечественной практике наиболее широкое применение получил кремнефтористый натрий, менее широкое — фтористый натрий и фторид-бифторид аммония.
Кремнефтористый натрий (ГОСТ 87—87*) — молекулярная масса 188,05, плотность 2,7 г/см3 — представляет собой мелкий, сыпучий, негигроскопический кристаллический порошок белого цвета (допускается серый или желтый оттенок), без запаха, удобен в эксплуатации. При длительном хранении на складе в закрытых бочках не слеживается. Плотность насыщенного раствора 1,0054, рН насыщенного раствора 3,5...4,0. В воде растворяется плохо.
Таблица 16.1
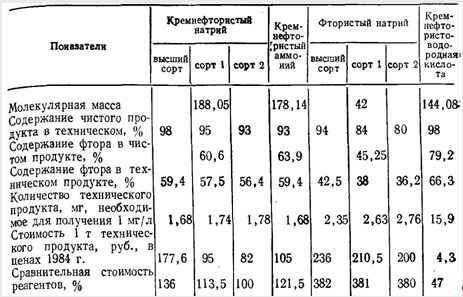
Согласно указанному ГОСТу, кремнефтористый натрий упаковывается заводами-поставщиками в фанерные барабаны (ГОСТ 9338—80) объемом до 50 л или в деревянные бочки вместимостью 40...50 л, выложенные внутри крафт-бумагой.
Фтористый натрий (ГОСТ 2871-85*), молекулярная масса 42, плотность 2,8 г/см3 представляет собой порошок белого или светло-серого цвета без запаха. Растворимость фтористого натрия с изменением температуры воды меняется незначительно. При обычно принятых температурах на водоочистных комплексах растворимость его составляет около 4%, рН раствора фтористого натрия —7,0. Реагент упаковывают в стальные сшивные барабаны, плотные сухотарные деревянные бочки или фанерные барабаны. Масса стального барабана 50... 150 кг, деревянной, бочки — 130... 150 кг, фанерного барабана — не более 50 кг. Деревянные бочки и фанерные барабаны внутри выкладываются двумя слоями оберточной бумаги, на бочках и барабанах делают - надпись: "Опасно. Яд".
Реклама

Кремнефтористоводородная кислота — молекулярная масса. 144,08 выпускается в виде 8...14%-ного раствора, являясь промежуточным продуктом в производстве фторсодержащих солей. В безводной форме она неизвестна. Это бесцветная, прозрачная, коррозионная жидкость с едким запахом, оказывающая раздражающее действие на кожу. Однопроцентный ее раствор имеет рН 1,2. Опыт показал, что применение кремнефтористоводородной кислоты для фторирования воды на установках малой производительности нецелесообразно, так как требуется разбавление кислоты водой, а при этом выпадает осадок, забивающий насосы, арматуру и трубы. Чтобы этого избежать, добавляют к кремнефтористоводородной кислоте небольшое количество фтористоводородной кислоты, что осложняет технологию использования этого метода.
Кремнефтористый аммоний, молекулярная масса 178,16, плотность 2,01 г/см3. Кристаллическое вещество белого цвета с розоватым или желтоватым оттенком без запаха. Недостатком этого реагента является его слеживаемость. Даже при кратковременном хранении он превращается в довольно плотные комья. Это свойство продукта вызывает необходимость дополнительных мероприятий при использовании его в качестве реагента: он нуждается в сушке и дроблении, что, конечно, создает дополнительные трудности в эксплуатации и увеличивает эксплуатационные расходы. Стоимость его ниже стоимости фтористого натрия. ГОСТ 9338—80 предусматривает упаковку кремнефтористого аммония в фанерные барабаны вместимостью до 50 л или деревянные бочки объемом 40...50 л, выложенные внутри крафт-бумагой, бумажные мешки массой до 50 кг. На каждом барабане или бочке должна быть надпись "Яд!"- Барабаны, бочки и мешки с кремнефтористым аммонием должны храниться в сухом месте.
Фтористый кальций — самый дешевый реагент, но его растворимость в воде крайне низка (0,0016 г на 100 мл воды при 25° С). Однако, фтористый кальций хорошо растворим в кислых растворах, в том числе в растворах коагулянта, 10%-ный раствор коагулянта может содержать 1 % фтор-иона.
Применяемые на практике установки по технологии приготовления растворов фторсодержащих соединений можно классифицировать следующим образом.
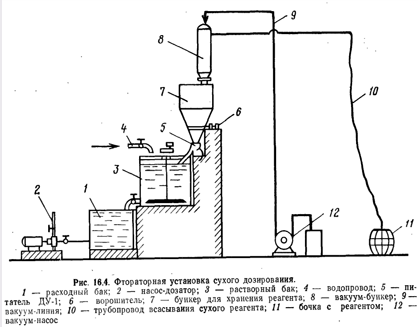
Во фтораторных установках сатураторного типа (рис. 16.1) в качестве реагента принят порошкообразный кремнефтористый натрий, который вводится в воду перед хлорированием. Предварительно реагент замачивают и размешивают в баке, а затем выливают через воронку в сатуратор (один раз в смену). В камере для реагента должно быть 8...10 кг кремнефтористого натрия. В основу работы фтораторной установки положен принцип объемного вытеснения.
Во фтораторных установках с растворными баками (рис. 16.2) в качестве реагента применяют кремнефтористый натрий. Загрузку в баки реагента осуществляют с помощью бункеров, оборудованных вибраторами и дозаторами барабанного типа. Для лучшего растворения реагента баки оборудованы мешалкой с частотой вращения 50...60 мин-1. Время перемешивания 2 ч. время отстаивания 2 ч. Концентрация раствора реагента в баках составляет 0,05% по фтору или 0,08% по чистой соли.
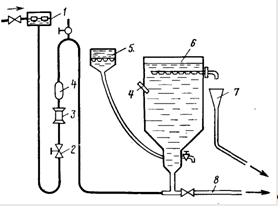
Рис. 16.1. Схема фтораторной установки с сатуратором.
1 — бак постоянного уровня; 2 — регулирующий вентиль; 4 — термометр; 5 — воронка приема реагента; 3— ротаметр; 7 — прием и отвод раствора реагента; б — сатуратор одинарного насыщения; 8 — сброс в канализацию
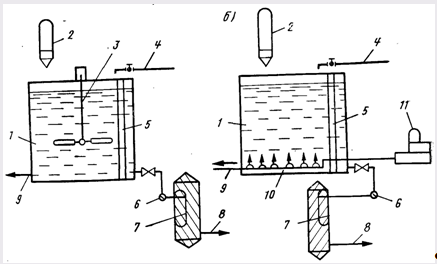
Рис. 16.2. Фтораторная установка с растворным баком с механическим побуждением (а) и с барбатированнем (б).
1 — растворный бак; 2 — бункер с дозирующим устройством; 3 — механическая мешалка; 4 — подача воды; 5 — поплавковое устройство; 6 — насос; 7 — напорный фильтр для осветления раствора фторсодержа- Щего реагента; 8 — фторпровод; 9 — сброс осадка; 10 — воздухораспределительная система; И — воздуходувка
Во фтораторных установках с затворно-растворными баками в качестве реагента принят фтористый натрий с расходом в сутки 20 кг. Установка состоит из системы баков: затворного — объемом 400 л, двух растворных — объемом 1500 л каждый, дозирующего бачка, снабженного поплавковым клапаном. Затворный и растворные баки оборудованы электромешалками. Растворяют фтористый натрий в воде, нагретой до 75...80°С, для чего в затворный бак вмонтирован электронагреватель. Крепкий раствор переливают в расходный бак, предварительно на 1/3 наполненный водой, бак дополняют водой до нужной отметки и раствор тщательно перемешивают. После определения содержания фтора в растворе последний через вентиль подают в дозирующий бак и затем в резервуар чистой воды.
Фтораторные установки с применением 8%-ной кремнефто- ристоводородной кислоты показаны на рис. 16.3.
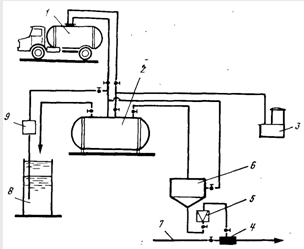
Рис. 16.3. Фтораторная установка с использованием кремнефтористоводородной кислоты. 1, 2 — авто- и стационарная цистерна; 3 — воздуходувка; 4 — эжектор; 5 — ротаметр; 6 — бак-мерник; 8 — емкость; 9 — ручной насос; 7 — водопровод
В зарубежной практике чаще всего фтористые соединения вводятся в воду: в сухом виде — непосредственно порошком, сухими дозаторами, через растворную камеру или в жидком виде — дозаторами для растворов. Первый способ чаще применяют на водоочистных комплексах большой производительности, жидкостное — на установках малой производительности. Дозаторы сухих реагентов применяют двух видов: объемные и массовые. Объемные дозаторы (рис. 16.4) подают определенный объем вещества за расчетный промежуток времени, массовые — массовое количество вещества. Основное отличие их состоит в следующем: объемные дозаторы, которые конструктивно проще и дешевле, имеет точность дозирования 3...5% массовые—1%; массовые дозаторы легче оборудовать записывающим устройством для регистрации дозируемого реагента и устройством для автоматической подачи реагента в воду. Важной и неотъемлемой частью сухих дозаторов является растворная камера. При непосредственном вводе сухих реагентов в воду они падают на дно нерастворенными. Максимальную концентрацию реагента в растворной камере принимают равной 1/4 концентрации насыщенного раствора при обычной температуре воды. Вместимость растворных камер принимают не менее 20 л. Для более полного смешения реагента с водой и его лучшего растворения предусматривают электрические мешалки или форсунки. Для точного регулирования количества воды, поступающей в растворную камеру, применяют различные водомеры. Из камеры раствор вводят в обрабатываемую воду.
Так как фторирование воды требует высокой точности дозирования реагента (±5%), для его подачи в жидком виде совершенно непригодны краны и насадки. В основном для дозирования реагентов в жидком виде применяют насосы-дозаторы мембранного и поршневого типа.
Дозу фторсодержащего реагента находят по формуле
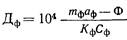
где тф
— коэффициент, зависящий от места ввода фтора в обрабатываемую воду, принимаемый при вводе фтора после очистных сооружений равным 1,0, при вводе фтора перед контактными осветлителями или фильтрами — 1,1; аф
— содержание фтора в обработанной воде, мг/л (оптимальная концентрация фтора в питьевой воде), равное для средней полосы России для зимнего периода—1, для летнего периода — 0,8; Ф — содержание фтора в исходной воде, мг/л, Кф
— содержание фтора в чистом реагенте, °/о, равное для кремнефтористого натрия — 60,6, для кремнефтористого аммония — 63,9, для фтористого натрия — 45.25, Сф — содержание чистого реагента в продажном техническом продукте, %, равное для кремнефтористого натрия высшего, I и II сортов соответственно 59,4; 57,5 и 56,4, для фтористого натрия — 42,5; 38; 36,2, а для кремнефтористого аммония, выпускаемого промышленностью одним сортом, — 59,4.
Как при мокром дозировании, так и при сухом реагенты для фторирования воды подают в виде раствора. Место введения раствора реагента выбирают в зависимости от способа очистки воды и техникоэкономических соображений, при этом должны быть соблюдены условия перемешивания реагента с питьевой водой и его наименьшие потери. При использовании артезианских вод, подаваемых потребителю без очистки, фтористые соединения поступают непосредственно в напорные водоводы. При небольшой нагрузке на фильтры фторсодержащие реагенты вводят перед фильтрами, при большой нагрузке — после фильтров, в трубопровод между фильтрами и резервуаром чистой воды или непосредственно в резервуар чистой воды. В некоторых случаях идут на потери фторидов, если это экономически выгодно. Примером является фтораторная установка на водоочистном комплексе в Вашингтоне, где реагент вводят в неочищенную воду. Потери фтор-иона составляют при этом 0,1 мг/л. На большинстве водоочистных комплексов фторирование является последней стадией обработки, не считая хлорирования. Хлорирование воды не удаляет фторидов. Хлор и фтор можно добавлять одновременно. Хлор и его производные оказывают одно неблагоприятное действие — они обесцвечивают реагенты, добавляемые при определении фторидов в воде, что может дать ошибку в определении концентрации фтора.
3. Технология дефторирования воды
фтор вода сорбция фильтрование
Для дефторирования воды используют ряд методов, которые можно объединить в две группы.
Метод сорбции фтора осадком гидроксида алюминия или магния, а также фосфата кальция целесообразно применять при обработке поверхностных вод, когда кроме обесфторивания требуются еще осветление и обесцвечивание. Вместе с тем этот метод может найти применение для обработки подземных вод при необходимости их одновременного умягчения (реагентным методом) и обесфторивания (рис. 16.5).
Метод фильтрования воды через фторселективные материалы основан на обменной адсорбции ионов, при которой фтор удаляется в процессе пропуска обрабатываемой воды через сорбент. Этот метод наиболее эффективен при обесфторивании подземных вод, как правило, не нуждающихся в других видах кондиционирования, или в тех случаях, когда одновременно с обесфториванием производят еще и опреснение (рис. 16.6).
Обесфторивание воды гидроксидом магния, который образуется в магнийсодержащей воде в присутствии извести, позволяет снизить содержание в воде и магния. Остаточное содержание фтора в воде после ее известкования Фост можно определить по формуле Скотта
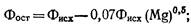
где ФИсх — содержание фтора в исходной воде, мг/л; (Mg) — количество магния, удаленного из воды при ее известковании, мг/л.
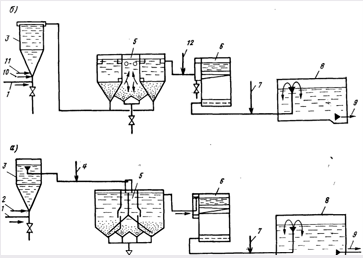
Рис. 16.5. Технологическая схема дефторирования воды свежеобразованным гидроксидом магния (а) и солями алюминия (б).
1 , 9 — подача исходной и отвод обесфторенной воды, 2 — ввод палочного реагента, 3 — смеситель, 4 — ввод солей магния, 5 — осветлитель со взвешенным осадком; 6 — фильтр; 7 — ввод хлора; 8 — резервуар чистой воды, 10 — подача кислоты; 11 — подача алюмосодержащего коагулянта; 12 — подача щелочного реагента
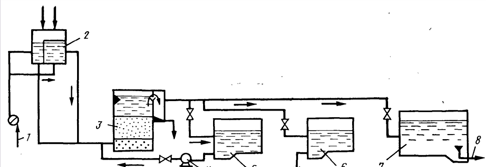
Рис. 16.6. Технологическая схема дефторнрования воды фильтрованием через модифицированную загрузку.
1 — насос подачи исходной воды; 2 — промежуточная емкость; 3 — скорый фильтр или К.О3; 5 — промывной насос, бак; 6 — бак регенерационного раствора; 7 — резервуар обесфторенной воды; 8 — подача обесфторенной воды потребителю
Для снижения содержания фтора в воде на 1 мг требуется 50...60 мг магния или 100...150 мг Mg(OH)2. При недостатке магния в исходной воде для повышения эффекта обесфторивания в нее вводят сульфат или хлорид магния. При избытке магния образующийся в результате взаимодействия гидроксида магния с фтором фторид магния переходит затем в малорастворимый оксифторид магния.
Исследования, выполненные в МГСУ, показали, что процесс сорбции фтора свежеобразованным гидроксидом магния при рН>9,5 протекает быстро и интенсивно, практически не зависит от температуры и заканчивается за 8...12 мин, сорбционная способность гидроксида магния может быть использована более полно путем пропуска обрабатываемой воды через его взвешенный слой. Отличительной особенностью осадка гидроксида магния является чрезвычайная легкость. Поэтому скорость вое ходящего движен ия воды в осветлителях должна быть 0,2.. ...0,3 мм/с. При этом концентрация взвешенных веществ слое взвешенного осадка составит 1,6... 2 г/л. Высота ело осадка принимается 2 ... 2,5 м. Время пребывания воды в ело контактного осадка не менее 1 ч. В этом случае расход магния на удаление 1 мг фтора значительно меньше — около 30 мг для ориентировочных расчетов расход солей магния на обесфторивание воды осаждением гидроксида магния с использованием его сорбционной способности во взвешенном слое следует принимать равным 2 мг-экв на 1 мг удаляемого из воды фтор при его содержании в воде до 7 мг/л. В связи с тем, что процесс является сорбционным, с увеличением начальной концентрации фтора в воде удельный расход магния на обесфторивание будет уменьшаться. При недостатке в природных водах солей магния необходимое их количество для обесфторивания может быть подсчитано по формуле, предложенной В. А. Клячко
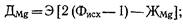 (16.3) (16.3)
где Э — эквивалентная масса вводимой в воду соли магния, мг; для MgS04
— 60,2, для MgS04
*7H2
0- 123,25, для MgCl2
-47,7 для MgCl2
*6H20 — 101,65; Фисх
— содержание фтора в исходной воде, мг/л; Жм§ — магнезиальная жесткость этой воды, мг-экв/л; 2 —расход солей магния, мг-экв/л, на удаление 1 мг фтора из 1 л обрабатываемой воды.
При этом необходимое количество извести Дсао
для осаждения гидроксида магния определяется химической реакцией:
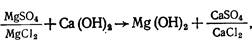
и может быть подсчитано по формулам при (Са2+
)>Щ
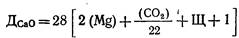
где Дсао
—доза извести, мг/л, считая на СаО; (СО2
) — содержание СО2
в воде, мг/л; (Mg) — содержание Mg, мг/экв-л, в обрабатываемой воде после введения в нее количества магния, необходимого для сорбции фтора; (Са) — содержание в исходной воде кальция, мг-экв/л; Щ — щелочность исходной воды мг-экв/л.
Технологическая схема установки для обесфторивания природных вод сорбцией на гидроксиде магния состоит из вертикальногосмесителя, осветлителей со слоем взвешенного осадка с коническими или пирамидальными днищами и скорых осветлительных фильтров (см. рис. 16.5).
Обесфторивание воды солями алюминия основано на сорбции фтора осадком гидроксида алюминия. Это связано с образованием на поверхности твердой фазы малорастворимых фторидов. При этом эффективность процесса находится в обратной зависимости от рН воды. По мере снижения рН воды при постоянной дозе сульфата алюминия эффективность обесфторивания возрастает, что объясняется неоднородностью состава осадков при гидролизе сульфата алюминия при различных рН. При низких значениях рН в осадке преимущественно образуется основной сульфат алюминия — А1 (ОН) SO4, эффективность обесфторивания возрастает, уменьшается содержание в нем гидроксида алюминия, который сорбирует фтор в меньшей степени, чем основной сульфат алюминия. По данным В. В. Ломако, для обесфторивания воды при значениях рН, близких к нейтральным, требуются очень большие дозы серно-кислого алюминия. Поэтому удаление фтора из воды этим способом наиболее целесообразно вести при рН 4,3 ..5,0. При таких значениях расход сульфата алюминия на 1 мг удаленного фтора составит 25.. 30 мг/л. Следовательно, обесфторивание воды гидроксидом алюминия требует ее предварительного подкисления с последующим подщелачиванием для снижения коррозионного действия воды. Технологическая схема состоит из вертикального смесителя, осветлителей со взвешенным осадком и скорых осветлительных фильтров. Раствор кислоты для подкисления вводится перед смесителем, сульфат алюминия — в смеситель, известь для подщелачивания воды — перед фильтрами. Большие расходы кислоты и извести, а также необходимость точного дозирования реагентов делают этот метод обесфторивания воды дорогим и сложным в эксплуатации.
Удаление фтора из воды с помощью трикальцийфосфата основано на сорбции свежеобразованным трикальцийфосфатом, который связывает имеющийся в воде фтор в малорастворимое соединение— [Са9
(Р04
)6
Са]F2
, выпадающее в осадок. Расход трикальций — фосфата на удаление 1 мг фтора составляет 23...30 мг. Этот процесс описывается следующей реакцией:
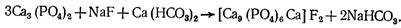
Скорость восходящего потока воды в слое взвешенного осадка принимают 0,6...0,8 мм/с. Содержание фтора снижается с 5 до 1 мг/л при расходе реагента 30 мг на 1 мг удаленного фтора. В качестве технологической рекомендуется схема, представленная на рис. 16.5. Для получения трикальций фосфата в вертикальный смеситель вначале вводят известь, а затем раствор ортофосфорной кислоты. После этого вся масса воды передается в осветлитель и поступает в слой взвешенного осадка. Здесь протекает основная часть процесса, образуется малорастворимый фторид, который в осадкоуплотнителе выпадает в осадок. Весь цикл обработки воды заканчивается на скорых осветлительных фильтрах, где она освобождается от мелких хлопьев, не выпавших в осадок в осветлителе. После этого вода подвергается обеззараживанию, аккумулируется в резервуарах и насосами II подъема подается в сеть потребителя.
Технико-экономическое сравнение трех рассмотренных сорб- ционных методов обесфторивания воды свидетельствуют о том, что наиболее целесообразно применять для указанной цели гидроксид магния.
НИИ КВОВ АКХ предложен контактно-сорбционный метод обесфторивания природных вод. Коагулянт вводят в воду непосредственно перед контактными осветлителями. В первоначальный период — 1,5...2,0 ч подается повышенная доза коагулянта 100...150 мг/л по А1203. При этом на зернах и в порах загрузки образуется гидроксид алюминия, который впоследствии сорбирует фтор. В этот период — период "зарядки" фильтрат, содержащий большое количество ионов фтора и алюминия, отводят в специальную емкость для последующего использования в качестве промывных вод. После "зарядки" дозу коагулянта снижают до 20...25 мг/л, что обеспечивает эффективное извлечение фтора за счет сохранения сорбционной способности гидроксида алюминия. Процесс дефторирования воды можно осуществлять и без "зарядки" при постоянной дозе коагулянта, величина которой определяется качеством исходной воды. Контактно-сорбционное обесфторивание приемлемо при обработке вод, содержащих фтор — до 5 мг/л, сероводород — до 2 мг/л, щелочность — до 6 мг-экв/л. На 1 мг удаляемого фтора расходуется около 80 мг сульфата алюминия.
Несомненный интерес представляет электрокоагуляционное обесфторивание природных вод, что объясняется возможностью удаления фтора без применения химических реагентов, вместе с которыми в воду вводится значительное количество дополнительных солей, а также высокая активность электролитически, полученного гидроксида алюминия. В качестве растворимых анодов применяют алюминий и дюралюминий, для экономии энергозатрат варьируют токовой нагрузкой и расстоянием между электродами, электролиз ведут при постоянном и переменном токе. При электролизе в воду с анода переходят катионы алюминия, которые и адсорбируют фтор. Растворение 1 г металлического алюминия эквивалентно введению 6,35 г сернокислого алюминия. Теоретический расход электроэнергии на получение 1 г алюминия должен составлять около 12 Вт-ч. Фактический расход электроэнергии значительно выше из-за тепловых потерь, дополнительного сопротивления оксидной пленки, образующейся на поверхности электродов, и ряда других причин.
Основным фактором, влияющим на сорбционную способность электролитически полученного гидроксида алюминия, является концентрация ионов водорода. В слабо кислой среде фтор сорбируется получаемым осадком значительно лучше, чем в нейтральной и щелочной. Оптимальное значение рН обрабатываемой воды находится в пределах 6,4...6,6. Повышение или понижение активной реакции среды приводит к снижению эффективности дефторирования воды. Причиной этого, как и в случае реагентной обработки воды, является конкуренция гидроксил-ионов при высоких значениях рН и растворение хлопьевидного осадка в кислой среде. Расход металлического алюминия при предварительном подкислении воды составил около. 12 г на каждый 1 г удаляемого фтора, расход кислоты — 0,2 л/м3.
В состав обесфторивающей установки входит емкость для соляной кислоты, насос-дозатор, электрокоагулятор, фильтр,. Центробежный насос и контрольно-измерительная аппаратура.
Подземные воды, используемые для хозяйственно-питьевого- водоснабжения, не нуждаются в осветлении, поэтому для их обесфторивания наиболее целесообразно применять фильтрационные (ионообменные) методы. В качестве сорбентов для извлечения фтора из воды могут быть применены сильноосновные катиониты и аниониты, магнезиальные сорбенты, фосфат кальция, специально обработанные активированные угли, активированный оксид алюминия, модифицированные загрузки, клиноптилолит.
Обесфторивание воды сильноосновными катионитами и анио- нитами целесообразно при ее одновременном опреснении. Очевидно, что в современных условиях ионообменный метод обес- фторирования воды с применением сильноосновных ионитов не может иметь самостоятельного значения по экономическим соображениям. Он может быть рекомендован только для случая •обработки воды в целях одновременного обессоливания и удаления фтора. Первоначально обрабатываемая вода поступает на напорные фильтры, загруженные активированным углем, назначение которых извлекать органические вещества из обрабатываемой воды для сохранения обменной способности анионита. Затем вода передается на водород — катионитовые фильтры, загруженные сильноосновным катионитом КУ-2, которые служат для извлечения из воды катионов. Образующийся в процессе водород — катионирования диоксид углерода в результате распада бикарбонатов удаляется в дегазаторе. После удаления углекислоты вода собирается в промежуточном резервуаре, откуда насосами подается на группу анионитовых фильтров, загруженных сильноосновным анионитом. Здесь помимо удаления из воды анионов сильных кислот происходит задержание фтора. Технологическая схема заканчивается буферным натрий-катионитовым фильтром, который сглаживает возможные проскоки на предыдущих ступенях обработки и поддерживает постоянное значение величины рН в фильтрате. Регенерация фильтров с загрузкой из активного угля и анионита производится едким натром. Водород-катионитовые фильтры регенерируются раствором соляной кислоты.
Как видно, технологическая схема отличается громоздкостью, сложностью реагентного хозяйства, что объясняет ограниченность ее применения.
Дефторирование воды активированным оксидом алюминия обеспечивает наилучшие результаты по удалению фтора из подземных вод. Зернистый активированный оксид алюминия является наиболее дешевым сорбентом, простым в изготовлении и емким по поглощению фтора. При фильтровании обрабатываемой воды через активированный оксид алюминия происходит поглощение фтора сорбентом. В начале фильтроцикла содержание фтора в фильтрате близко к нулю. С течением времени поглотительная способность уменьшается и при достижении 1,5 мг/л рабочий цикл обесфторивания воды прекращается, так как сорбент нуждается в регенерации. Регенерация сорбента производится пропуском через него раствора едкого натра или сульфата алюминия. В процессе регенерации из сорбента вытесняется поглощенный им фтор. После регенерации сорбент отмывается водой для удаления продуктов регенерации и не прореагировавшего реагента.
Сорбционная способность активированного оксида алюминия может быть повышена применением для регенерации сорбента вместо раствора едкого натра раствора сульфата алюминия. При этом в процессе удаления фтора из воды активированный оксид алюминия действует как анионит (АН), заряженный при регенерации обменными ионами S042-. Этот процесс описывается следующей реакцией:
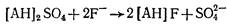
Уместно отметить, что при этом происходит поглощение не только ионов фтора, но и бикарбонатных ионов:
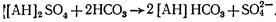
По данным Е. Ф. Золотовой, поглощение активированным оксидом алюминия ионов фтора происходит интенсивнее, чем бикарбонатных ионов.
В процессе обесфторивания воды в результате ионного обмена происходит увеличение концентрации в фильтрате сульфатных ионов. Количественно это увеличение эквивалентно уменьшению концентрации суммы ионов фтора и бикарбонатных ионов. Однако, известно, что содержание сульфатов в питьевой воде регламентируется. Согласно ГОСТ 2874—82, оно не должно превышать 500 мг/л. Поэтому увеличение содержания сульфатов при обесфторивании воды необходимо учитывать при проектировании и расчете комплексов по улучшению качества воды.
Исследования, выполненные в институте ВОДГЕО, показали что для загрузки обесфторивающих фильтров может быть использован оксид алюминия, выпускаемый отечественной химической промышленностью. Однако, перед загрузкой его необходимо подвергнуть вторичной активации прокаливанием при 800°С в течение 3 ч. После остывания его смачивают 15%-ным раствором кальцинированной соды и снова прокаливают при 800° С в течение 30 мин. Перед введением фильтра в работу загрузку необходимо взрыхлить, отрегенерировать 2%-ным раствором едкого натра и нейтрализовать избыток щелочи 0,5%-ным раствором соляной кислоты.
Основными технологическими сооружениями рассматриваемого метода обесфторивания воды (см. рис. 16.6) являются скорые напорные или открытые фильтры, загруженные оксидом алюминия. Помимо фильтров установка по удалению фтора из воды должна иметь реагентное хозяйство для приготовления регенерационных растворов, баки для хранения воды, необходимой для взрыхления и отмывки сорбента, также насосное и воздуходувное оборудование.
Рассматриваемая технологическая схема отличается известной простотой, возможностью компактного решения планировки станции, надежностью при эксплуатации. Кроме того, обесфторивание воды по данному методу позволяет получить наибольший технико-экономический эффект, так как себестоимость обработки воды здесь минимальная по сравнению со всеми ранее рассмотренными методами.
Обесфторивание воды, на алюмомодифицированных материалах показывает, что после обработки солями алюминия песка, керамзита, дробленого клиноптилолита и других фильтрующих загрузок они способны эффективно извлекать из фильтруемой воды фтор — ионы. Максимальной сорбционной емкостью по фтору из рассматриваемых материалов обладает алюмомодифицированный клиноптилолит, который в естественной форме фтор из воды практически не извлекает. Механизм сорбции фтора алюмомодифицированным клиноптилолитом может быть представлен следующим образом. При контакте алюмосодержащего реагента с клиноптилолитом (Кл), который является природным катионообменником, в последнем замещаются обменные катионы Са2+, Mg2+, Na+ на катионы алюминия из раствора — модификатора:
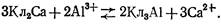
При последующем фильтровании очищаемой воды через алюмо- модифицированный материал начинается реобмен катионов алюминия из клиноптилолита. Алюминий взаимодействует с анионами воды (SO4
2-
, ОН-
, F-
). Одновременно с гидролизом и образованием основных солей алюминия протекает процесс дефторирования воды. Извлечение фтора осуществляется за счет ионообмена и образования алюмофторидных комплексов, которые адсорбируются клиноптилолитом:
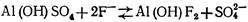
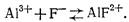
Сорбционная емкость алюмомодифицированных клиноптилолитов составляет 0,5... 1 мг фтора на 1 г сорбента.
Технологическая схема обесфторивания воды путем ее фильтрования через алюмомодифицированную загрузку клиноптилолита состоит из скорых фильтров, загруженных модифицированным клиноптилолитом. Регенерацию истощенной загрузки осуществляют в два приема. Первоначально производят взрыхление и отмывку сорбента от фторсодержащих осадков, задержанных на поверхности и в порах загрузки. Затем клиноптилолит модифицируют, пропуская через загрузки концентрированный 4...6 %-ный раствор солей алюминия (например, сернокислого алюминия). Раствор-модификатор циркулирует по замкнутому циклу бак—фильтр—бак. После модификации на фильтры подают исходную воду. Первые порции фильтрата с большим содержанием алюминия и низким значением рН отводят в специальный резервуар для повторного использования.
Гиперфильтрационное обесфторивание природных вод является новым способом в технологии обесфторивания природных вод, основанным на применении полупроницаемых мембран (гиперфильтрация и электродиализ).
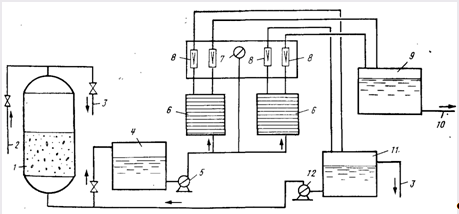
Рис. 16.7. Технологическая схема дефторирования воды обратным осмосом.
1 — фильтр предварительной очистки; 2, 10 — подача исходной и отвод обесфтореиной воды; 4 — бак осветленной воды; 5 — насос высокого Давлении; 6 — гиперфильтрационные аппараты; 8 — ротаметры; 7 — манометр; 9 — бак обеефторенной воды; 11 — бак концентрата; 3 — сброс в Канализацию; 12 — насос
Исследования, проведенные НИИ КВОВ АКХ, показали, что при фильтровании фтор - содержащей воды через полупроницаемые мембраны при давлениях выше осмотических происходит извлечение фтор-ионов из воды. В качестве обесфторивающих гиперфильтрационных установок могут быть использованы аппараты фильтр-прессового, трубчатого и рулонного типов, а также аппараты с полыми волокнами.
Производственная установка (рис. 16.7) состоит из песчаного фильтра предварительной очистки, бака осветленной воды, насосов высокого давления, гиперфильтрационных аппаратов, ротаметров для измерения расхода фильтрата и сбросного раствора. Кроме того, установка оснащена электроконтактными манометрами, которые вместе с клапанами-регуляторами давления обеспечивают автоматизацию ее работы. Расход электроэнергии 3...4 кВт*ч на 1 м3 обесфторенной воды.
Литература
Алексеев Л. С., Гладков В. А. Улучшение качества мягких вод. М.,
Стройиздат, 1994 г.
Алферова Л. А., Нечаев А. П. Замкнутые системы водного хозяйства промышленных предприятий, комплексов и районов. М., 1984.
Аюкаев Р. И., Мельцер В. 3. Производство и применение фильтрующих
материалов для очистки воды. Л., 1985.
Вейцер Ю. М., Мииц Д. М. Высокомолекулярные флокулянты в процессах очистки воды. М., 1984.
Егоров А. И. Гидравлика напорных трубчатых систем в водопроводных очистных сооружениях. М., 1984.
Журба М. Г. Очистки воды на зернистых фильтрах. Львов, 1980.
|