| Федеральное агентство по образованию Государственное образовательное учреждение высшего профессионального образования
«Норильский индустриальный институт»
Кафедра
Технологические машины и оборудование
Контрольная работа №1
по Материаловедению
Выполнила студентка группы
ММ-07(з) Андреева О.М. Шифр 07331
Проверила: Сарафанова А.Я.
Норильск 2010
1.
Опишите условия получения крупнозернистой структуры при самопроизвольно развивающейся кристаллизации (используя теорию Тамманна)
Систематическое исследование процесса образования центров кристаллизации и их роста вначале на прозрачных органических веществах, а затем и металлах было проведено Г. Тамманом. Им установлена в общем виде зависимость между числом центров кристаллизации, скоростью роста и степенью переохлаждения. Однако более поздние исследования процессов кристаллизации, особенно исследования А. А. Бочвара, К. П. Бунина и др., показали ограниченное значение схемы Таммана для процесса кристаллизации реальных жидких металлов, поскольку они содержат нерастворенные (взвешенные) частицы, служащие центрами кристаллизации. Все же многие закономерности, установленные Тамманом на основе опытов, нашли качественное подтверждение в последующих работах и оказывайте полезными при анализе процессов кристаллизации.
Исследуя кристаллизацию прозрачных органических веществ при разных температурах, Г. Тамман установил, что число зарождающихся в единицу времени кристаллов и скорость роста кристаллов определяются степенью переохлаждения. Зависимость число зарождающихся в единицу времени кристаллов и скорость роста кристаллов от переохлаждения выражается кривой с максимумом. При теоретической температуре кристаллизации (л = 0) значения числа зарождающихся в единицу времени кристаллов и скорость роста кристаллов равны нулю и процесс кристаллизации идти не может, что находится в полном соответствии с изложенным выше положением о необходимости переохлаждения для протекания процесса. С увеличением переохлаждения значения числа зарождающихся в единицу времени кристаллов и скорость роста кристаллов возрастают, достигают максимума и затем понижаются; при больших величинах переохлаждения практически падают до нуля.
Увеличение числа зарождающихся в единицу времени кристаллов и скорость роста кристаллов при малых степенях переохлаждения обусловлено тем, что вблизи равновесной точки (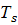 ,) подвижность атомов велика и ускорение кристаллизации с увеличением степени переохлаждения вызывается увеличением разности свободных энергий жидкого и кристаллического состояний. Снижение числа зарождающихся в единицу времени кристаллов и скорость роста при больших степенях переохлаждения вызвано тем, что при больших переохлаждениях и, следовательно, при низких температурах подвижность атомов уменьшена, а тем самым уменьшена и способность системы к превращению. При больших степенях переохлаждения число зарождающихся в единицу времени кристаллов и скорость роста кристаллов становятся равными нулю, так как подвижность атомов уже недостаточна для того, чтобы осуществилась перестройка их из хаотического расположения в жидкости в правильное в кристалле. ,) подвижность атомов велика и ускорение кристаллизации с увеличением степени переохлаждения вызывается увеличением разности свободных энергий жидкого и кристаллического состояний. Снижение числа зарождающихся в единицу времени кристаллов и скорость роста при больших степенях переохлаждения вызвано тем, что при больших переохлаждениях и, следовательно, при низких температурах подвижность атомов уменьшена, а тем самым уменьшена и способность системы к превращению. При больших степенях переохлаждения число зарождающихся в единицу времени кристаллов и скорость роста кристаллов становятся равными нулю, так как подвижность атомов уже недостаточна для того, чтобы осуществилась перестройка их из хаотического расположения в жидкости в правильное в кристалле.
Реклама

Размер образовавшихся кристаллов зависит от соотношения величин скорости роста кристаллов и числа зарождающихся в единицу времени кристаллов при температуре кристаллизации, при данной степени переохлажден. При большом значении скорости роста кристаллизации и малом значении числа зарождающихся в единицу времени кристаллов, образуются немногочисленные крупные кристаллы; при малых значениях скорости роста кристаллов и больших числа зарождающихся в единицу времени кристаллов (большое переохлаждение) образуете большое число мелких кристаллов. Наконец, в соответствии с кривыми Таммана если удается очень сильно переохладить жидкость без кристаллизации, то скорость роста кристаллов и числа зарождающихся в единицу времени кристаллов становятся равными нулю, жидкость сохраняется непревращенной, незакристаллизовавшейся. Соли, силикаты, органические вещества весьма склонны к переохлаждению. Для металлов же требуется переохладить жидкость до температуры, когда подвижность атомов станет мала и такое состояние окажется достаточно устойчивым.
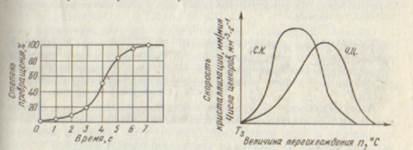
Рис.1 Кинетическая кривая кристаллизации.
Рис.2 Скорость роста кристаллов и скорость зарождения центров кристаллизации в зависимости от степени переохлаждения.
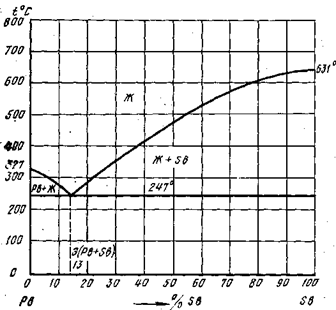
2. Вычертите диаграмму состояния системы свинец-олово. Опишите взаимодействие компонентов в жидком и твердом состояниях, укажите структурные составляющие во всех областях диаграммы состояния и объясните характер изменения свойств сплавов в данной системе с помощью правила Курнакова
 А А
Линия АСВ
является линией ликвидус
(начало кристаллизации), линия D
СЕ
линией солидус
(конец кристаллизяции). На линии АС
начинают ( при охлаждении) выделяться кристаллы свинца, а на линии СВ
— кристаллы
олова. На линии D
СЕ
из жидкости концентрации 13% одновременно выделяются кристаллы свинца и олова.
Реклама

Ниже эвтектической горизонтали DCE находятся две фазы – кристаллы свинца и олова. Левее эвтектической концентрации из жидкости выделяются вначале кристаллы свинца, а затем эвтектика. Поэтому структурное состояние доэвтектического сплава можно обозначить через свинец + эвтектика ( свинец + олово) и заэвтектического В + эвтектика (свинец + олово) .
3.
Опишите линейные несовершенства кристаллического строения и их влияние на свойства металлов
Линейные дефекты.
Линейные несовершенства имеют малые размеры в двух измерениях и большую протяженность в третьем измерении. Эти несовершенства называются дислокациями. Кристаллическая решетка с краевыми дислокациями показана на рис. 1.
Краевая дислокация (рис. 1,б и в) представляет собой локализованное искажение кристаллической решетки, вызванное наличием в ней «лишней» атомной полуплоскости или экстраплоскости, перпендикулярной к плоскости чертежа.
Наиболее простои и наглядный способ образования дислокаций в кристалле— сдвиг (рис. 1, а) Если верхнюю часть кристалла сдвинуть относительно нижней на одно межатомное расстояние, причем зафиксировать положение, при котором сдвиг охватывает не всю плоскость скольжения, а только часть ее АВС
D
,
то граница АВ
между участком, где скольжение уже произошло, и не нарушенным участком в плоскости скольжения и будет дислокацией (рис. 1, а).
Если экстраплоскость находится в верхней части кристалла, то дислокацию называют положительной
и обозначают ┴ (рис. 1,в), а если в нижней-то отрицательной
и обозначают ┬ (рис. 1,г).
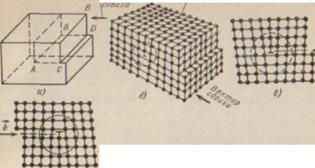
Рис.1 Краевые дислокации: а – сдвиг, создавший краевую дислокацию; б – пространственная схема краевой дислокации; в, г – схемы расположения атомов у дислокации.
Кроме краевых различают еще винтовые дислокации. Винтовые дислокации в отличие от краевых располагаются параллельно направлению сдвига (линия А
D
на рис. 2), При наличии винтовой дислокации кристалл можно рассматривать как состоящий из одной атомной плоскости, закрученной в виде винтовой поверхности. На рис. 2,б показано расположение атомов на винтовой поверхности вдоль винтовой дислокации.
Дислокации окружены полями упругих напряжений, вызывающих искажение кристаллической решетки. В краевой дислокации выше края экстраплоскости межатомные расстояния меньше нормальных, а ниже края — больше.
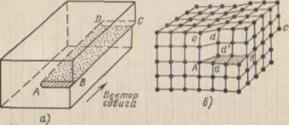
Рис.2 Винтовая дислокация: а – сдвиг, создавший винтовую дислокацию; б – расположение атомов.
Энергия искажения кристаллической решетки является одной из важнейших характеристик дислокации любого тина. Чтобы оценить степень искажения решетки, вызванной линейной дислокацией, следует сравнить совершенный кристалл с кристаллом, содержащим дислокацию. Критерием этого искажения служит вектор Бюргерса.
Определение вектора Бюргерса для кристалла, содержащего винтовую дислокацию, производят аналогично. В краевой дислокации вектор Бюргерса перпендикулярен к ее линии, а у винтовой — параллелен ей. Если вектор Бюргерса охватывает несколько дислокаций, то величина его соответствует геометрической сумме векторов отдельных дислокаций. Вектор Бюргерса позволяет найти силы, требуемые для продвижения дислокации, силы взаимодействия и энергию дислокаций и т. д.
Дислокации образуются в процессе кристаллизации металлов (при срастании зерен и блоков) из группы вакансий, а также в процессе пластической деформации и фазовых превращений.
Силовые (упругие) поля дислокаций взаимодействуют между собой. Если дислокации, расположенные в одной плоскости скольжения, обладают одинаковым знаком, то они отталкиваются одна от другой); если дислокации разного знака, то они взаимно притягиваются. Сближение дислокаций разного знака приводят к их взаимному уничтожению (аннигиляции).
Дислокации не могут обрываться внутри кристаллита. Они мо! \ г прерываться на других дислокациях или на границах раздела' (границы зерен, поверхность кристалла и т. д.). В связи с этим внутри кристалла дислокации образуют замкнутые петли или взаимосвязанные сетки.
Важной характеристикой дислокаций является плотность. Под плотностью дислокаций понимают суммарную длину дислокации (см), приходящуюся на единицу объема V кристалла (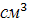 ). Таким образом, размерность плотность дислокаций (см2
). ). Таким образом, размерность плотность дислокаций (см2
).
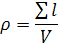
Плотность дислокации экспериментально определяют путем подсчета числа выходов дислокаций, пересекающих единицу площади металлографическою шлифа. При травлении металлографического шлифа на его поверхности можно выявить ямки или точки, соответствующие выходу дислокации.
4.
Вычертите диаграмму состояния железо-карбид железа, укажите структурные составляющие во всех областях диаграммы состояния, опишите превращения и постройте кривую охлаждения в интервале температур от 1600 до 0°С (с применением правила фаз) для сплава, содержащего 1,6% С. Выберите для заданного сплава любую температуру, лежащую между линиями ликвидуса и солидуса, и определите: состав фаз, т. е. процентное содержание углерода в фазах; количественное соотношение фаз
Линия АВСП
является ликвидусом системы, линия AHJECF — солидусом.
Так как железо, кроме того, что образует с углеродом химическое соединение Fe3
С, имеет две аллотропические формы α и γ то в системе существуют следующие фазы:
жидкость
(жидкий раствор углерода в железе), существующая выше линии ликвидус, обозначаемая везде буквой L
;
цементит
Feэ
С — линия DFKL
,
обозначаемая в дальнейшем химической формулой или буквой Ц;
феррит
— структурная составляющая, представляющая собой α-железо, которое в незначительном количестве растворяет углерод; обозначается буквой Ф, α
или 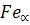 . Область феррита в системе железо — углерод расположена левее линии GPQ и AHN. . Область феррита в системе железо — углерод расположена левее линии GPQ и AHN.
аустенит
— структура, представляющая собой твердый раствор углерода в γ-железе. Область аустенита на диаграмме — NJESG
.
Обозначается аустенит А,
γ или Feу
(С).
Сплавы, содержащие 1.6% С, кристаллизуются в интервале температур, ограниченном линиями ВС
и J
Е.
Ниже липни ВС
сплавы состоят из жидкой фазы и аустенита. В процессе кристаллизации состав жидкой фазы изменяется по линии ликвидус, а аустенита — по линии солидус.
После затвердевания (ниже линии солидус J
Е)
сплавы получают однофазную структуру - аустенит.
Первичные кристаллы аустенита (так же как и δ-феррита) имеют вид дендритов, величина и строение которых определяются перегревом металла выше линии ликвидус, его составом и условиями охлаждения в процессе кристаллизации.
Определяем процентное содержание углерода в фазах:
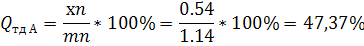
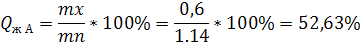
Количественное соотношение фаз определяем по графику:
Построим кривую охлаждения:
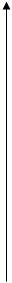 температура температура
А+Ф(δ)
А
       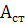
  перлит перлит
Время
5.
В структуре углеродистой стали 30 после закалки не обнаруживается остаточного аустенита. В структуре углеродистой стали У12 после закалки наблюдается до 30% остаточного аустенита. Объясните причину этого явления в связи с мартенситными кривыми для данных сталей. Какой обработкой можно устранить остаточный аустенит?
Мартенситное превращение не протекает до конца), поэтому в закаленных сталях, имеющих точку 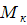 ниже 20°С, а именно в углеродистых сталях, содержащих свыше 0,4 — 0,5% С,
присутствует остаточный аустенит. Его количество тем больше, чем ниже температура точек Мн
и Мк
, т. е. чем выше содержание в аустените углерода и легирующих элементов (за исключением Со и А1). В стали с 0,6—1,0% С количество остаточного аустенита не превышает 10%, а в стали, содержащей 1,3 — 1,5% С, оно достигает 30-50%, ниже 20°С, а именно в углеродистых сталях, содержащих свыше 0,4 — 0,5% С,
присутствует остаточный аустенит. Его количество тем больше, чем ниже температура точек Мн
и Мк
, т. е. чем выше содержание в аустените углерода и легирующих элементов (за исключением Со и А1). В стали с 0,6—1,0% С количество остаточного аустенита не превышает 10%, а в стали, содержащей 1,3 — 1,5% С, оно достигает 30-50%,
В некоторых сталях с высоким содержанием углерода и легирующих элементов - например, в стали с 1,3%С и 12% Сг, количество остаточного аустенита после закалки с высоких температур может достигать 80-100%. Это объясняется снижением температуры, соответствующей точке Мн
в область отрицательных температур. При больших количествах остаточного аустенита (20 — 30%) его можно наблюдать в микроструктуре закаленной стали в виде светлых нолей между иглами мартенсита.
Если задержать на некоторое время охлаждение при температуре, лежащей ниже температуры, соответствующей точке Мн
например 20°С, то аустенит, сохранившийся непревращенным при охлаждении до этой температуры, становится более устойчивым. Подобная стабилизация аустенита выражается в том, что при последующем понижении температуры превращение аустенита в мартенсит возобновляется не сразу, а происходит при более низкой температуре и менее интенсивно. Количество образующегося в итоге мартенсита оказываемся меньше, чем при непрерывном охлаждении. Это явление стабилизации проявляется более сильно в интервале температур Мн
— Мк
и зависит от температуры, при которой задерживалось охлаждение. Температура, ниже которой проявляется этот эффект стабилизации, по предложению А. П. Гуляева, обозначается Мс
. Явление стабилизации иногда объясняют релаксацией напряжений, которые стимулируют мартенситное превращение.
Остаточной обработкой можно устранить термической обработкой, например отжиг.
|