Кооперативные межмакромолекулярные реакции с участием лигносульфонатов
Известно, что в результате кооперативных реакций между линейными синтетическими полиэлектролитами образуются полиэлектролитные солевые комплексы. Описаны также полиэлектролитные комплексы, в состав которых включены макромолекулы модельных биологических и природных полиэлектролитов, таких как полипептиды, полисахариды, белки, нуклеиновые кислоты [1- 4]. В последние годы обнаружено, что лигносульфонаты — водорастворимые производные природного полимера лигнина — в растворах взаимодействуют с синтетическими поликатионами, образуя полимерные комплексы [5,6]. Однако собственно реакции, приводящие к образованию таких комплексов, а также строение и свойства последних практически не исследованы.
В данной работе изучено взаимодействие в водных растворах лигносульфонатов со слабым полимерным основанием поли-М,М-диметиламино-этилметакрилатом (ПА) с позиций, развитых при изучении кооперативных реакций между полиэлектролитами. Интерес к исследованию такого рода в значительной степени обусловлен широкой распространенностью и доступностью лигносульфонатов, являющихся отходами целлюлозно-бумажного производства.
В качестве исходного лигносульфоната использовали сульфитно-дрожжевую бражку Слокского ЦБК. Лигносульфонаты фракционировали методом препаративной ГПХ на Сефадексе G-75. Превращение лигносульфоновых кислот в солевую форму осуществляли нейтрализацией 0,1 М NaOH. Полученные растворы лигносульфонатов натрия (JIC-Na) концентрировали в кристаллизаторах и высушивали в вакуум-эксикаторе над Р2
05
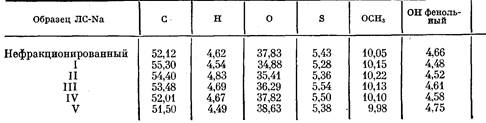
при комнатной температуре. Функциональные группы в образцах определяли принятыми в химии лигнина методами [7]. Элементный и функциональный составы, а также соответствующие полуэмпирические формулы ЛС-Na приведены в таблице. Условный грамм-эквивалент принимали равным массе структурного звена ЛС-Na, приходящегося на один атом серы, исходя из полуэмпирической формулы. Средневесовые молекулярные массы Mw
фракций и исходного ЛС-Na определяли методом аналитической гель-фильтрации на смеси сефадексов G-200, G-100, G-75 (50: 25: 25 вес. % соответственно), используя в качестве элюента и растворителя 0,1 I NaCl. Приведенные в таблице молекулярные- массы образцов рассчитывали из уравнения [8]
Реклама

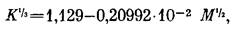
где К - коэффициент распределения.
ПА получали радикальной полимеризацией соответствующего мономера по методике, описанной в работе [9]. Mw
ПА, рассчитанный из данных светорассеяния, составлял 5 105
.
Реакцию между полиэлектролитами проводили медленно приливая раствор ПА к раствору ЛС-Na при постоянном перемешивании. рН растворов полиэлектролитов иих смеси контролировали при помощи потенциометра рН-121 со стеклянным электродом в качестве измерительного. Точность измерений 0,05 ед. рН. Титрование вели в токе инертного газа при 293 К и постоянном перемешивании. Время установления постоянного значения рН ~2 мин. При обработке кривых потенциометрического титрования разбавлением раствора в процессе титрования пренебрегали.
Изучение реакции между макромолекулами лигносульфонатов и ПА проводили в разбавленных водных растворах. Лигносульфонаты характеризуются довольно широким ММР, поэтому нами были изучены реакции с участием отдельных фракций лигносульфонатов. Последние, являясь солями сильных лигносульфоновых кислот, ведут себя в водных растворах как сильные полиэлектролиты. В связи с этим в качестве химически комплементарного полимера было выбрано слабое полимерное полиоснование.
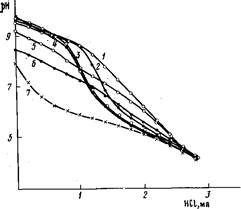
Рис. 1. Кривые потенциометрического титрования эквимоль-ных смесей ПА и JIC-Na: 1 - фракция IV, 2 - III, 3 - II, 4 -I, 5 - нефракционированный JTC-Na, 6 - фракция V, 7 - ПА. [JIC-Na] = [ПА] =0,0012 осново-моль/л; [НС1]=0,01 моль/л
Смешение растворов JIC-Na и ПА, как следовало ожидать, для реакций слабых полиоснований с полимерными анионами сопровождалось повышением рН раствора. На рис. 1представлены кривые потенциометрического титрования эквимольных (в расчете на сульфо- и аминогруппы) смесей полиэлектролитов (кривые 1—6)и свободного ПА (кривая 7)соляной кислотой. Видно, что кривые титрования смесей различных фракций JIC-Na, а также нефракционированного JIC-Na с ПА лежат гораздо выше кривой титрования ПА. Это свидетельствует о том, что реакция между макромолекулами JIC-Na и ПА происходит по механизму электростатического взаимодействия между сульфогруппами JIC-Na и аминогруппами полиоснования и может быть представлена схемой
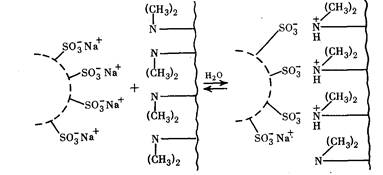
Согласно рис. 1, количество щелочи, выделяющейся при смешении растворов JIC-Na и свободного полимерного основания, тем больше, чем выше молекулярная масса ЛС-Na.
В интервале больших и средних величин молекулярных масс зависимость количества выделяющейся щелочи от величины молекулярной массы ЛС-Na выражена слабо, однако очевидна при переходе к низкомолекулярным ЛС-Na. Из рис. 1 также видно, что кривые потенциометрического титрования смесей ПА с высокомолекулярными фракциями I, II, III имеют две точки перегиба.
Реклама

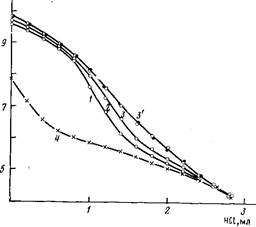
Рис. 2. Кривые потенциометрического титрования смесей ПА и фракции I различных составов: Z=l (1); 0,91 (2); 0,77 (5); 0,66 (?) и ПА (4). [ПА] =0,0012 осново-моль/л, [НС1]=0,01 моль/л
По аналогии с кривыми титрования смесей синтетических полиэлектролитов первый перегиб на кривых титрования соответствует завершению реакций образования солевых связей между сульфогруппами ЛС-Na и протонированными аминогруппами поликатиона, а второй — оттитровыванию свободных аминогрупп ПА. Несмотря на то что аминогруппы введены в эквивалентном по-отношению к сульфогруппам количестве, часть из них не вступает в образование межмолекулярных солевых связей. Обнаруженное нами отклонение от рассчитанной стехиометрии обусловлено особенностью химического строения высокомолекулярных ЛС-Na. Из опубликованных в литературе данных [10,11] следует, что с возрастанием молекулярной массы увеличивается степень разветвленное™ макромолекул лигносульфонатов. Поэтому появление точек перегиба, соответствующих оттитровыванию свободных аминогрупп на кривых 2,3и 4(рис. 1), может быть объяснено возникновением пространственных затруднений при взаимодействии высокомолекулярных ЛС-Na с ПА. При уменьшении молекулярной массы доля доступных сульфогрупп возрастает и низкомолекулярные ЛС-Na реагируют с линейным полиоснованием в стехиометрических соотношениях. Это следует из рассмотрения кривых 1и 6рис. 1, соответствующих двум низкомолекулярным фракциям IV и V.

Для установления составов полиэлектролитных комплексов, образованых высокомолекулярными ЛС-Na, или, что то же, для нахождения доли доступных сульфогрупп, способных образовывать солевые связи с аминогруппами ПА, было изучено поведение смесей полиэлектролитов разного состава. В таких смесях содержание поликатиона оставляли постоянным, а количество ЛС-Na варьировали. На рис. 2 приведены кривые потенциометрического титрования смесей ПА с наиболее высокомолекулярной фракцией I различного состава. Видно, что увеличение содержания фракции I сопровождается смещением кривой титрования в область более высоких значений рН. При составе реакционной смеси £=[ПА]:[1]=0,77 (в дальнейшем будем называть его характеристическим Zx
) на кривой титрования обнаруживается один скачок, соответствующий полному оттитровыванию аминогрупп ПА, включенных в полимерный комплекс. Кривая титрования смеси состава Z=0,66<ZX
практически совпадает с кривой титрования смеси характеристического состава. Для смесей двух последующих фракций II и III характеристические составы были найдены в пределах 0,8-0,9.
Сравнительно небольшие отклонения от рассчитанной стехиометрии [ПА]:[ЛС-Na] = 1, предполагающей доступность всех сульфогрупп ЛС-Na в реакции с аминогруппами ПА, позволяют утверждать, что ионогенные группы в макромолекулах ЛС-Na расположены главным образом на периферии. Если, следуя лит. данным [12], рассматривать макромолекулу ЛС-Na как ограниченно набухающую сферическую частицу, заряд которой равномерно распределен по объему, то следует ожидать более существенного отклонения характеристических составов полиэлектролитных комплексов от эквимольных, особенно для высокомолекулярных фракций ЛС-Na. Слабая зависимость этого отклонения от величины молекулярной массы ЛС-Na в области больших значений последней также не может быть объяснена в рамках сферической модели. Полученные нами данные значительно в лучшей степени соответствуют представлению о дискообразной форме макромолекул лигносульфонатов, выдвинутому недавно в работе [13].
Количественное описание реакции ПА—ЛС-Na проводили в терминах зависимости глубины превращения Э в межмакромолекулярной реакции от рН среды, рассчитанной из данных потенциометрического титрования. Как и в случае реакции между линейными синтетическими полиэлектролитами, глубину превращения оценивали по уравнению
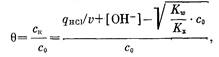
где с„ — концентрация звеньев, вступивших в реакцию; с0
— начальная концентрация любого из макромолекулярных компонентов; [ОН-
]—концентрация гидроксилионов в растворе; Кх
— характеристическая константа диссоциации ПА: Kw
— ионное произведение воды.
На рис. 3 представлены зависимости 6 от рН в реакциях ПА с различными образцами ЛС-Na, взятыми в соотношении [ПА]: [ЛС-Na] =1. Видно, что для высоко- и среднемолекулярных фракций ЛС-Na (кривые 1—4)крутизна кривых Э (рН) вплоть до 8~0,3 практически неизменна. Небольшое расхождение в крутизне при больших глубинах превращениясвязано с различиями в отклонении характеристического состава полиэлектролитных комплексов, образованных различными фракциями JIC-Na от эквимольного. Существенно, что реакции ПА — JIC-Na для всех изученных лигносульфонатов протекают в узком интервале рН. Это указывает на-кооперативный характер взаимодействия полиэлектролитов, макромолекулы которых являются химически комплементарными по отношению друг к другу.
Следует отметить также, что в рассматриваемом интервале молекулярных масс JIC-Na наблюдается некоторая зависимость растворимости поликомплексов ПА — JIC-Na в щелочных средах от величины молекулярной массы JIC-Na. Ниже приводятся значения 8 для различных фракций JIC-Na, выше которых происходит фазовое разделение в смесях полиэлектролитов, т. е. результирующий полиэлектролитный комплекс становится нерастворимым.
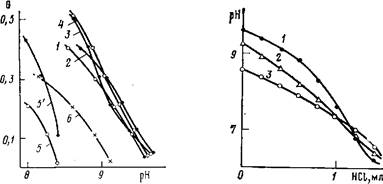
Рис. 3 Рис. 4
Рис. 3. Зависимость 6 от рН для реакций ПА с фракциями JIC-Na I (1), II (2), III (3), IV (4), V (5). V с учетом состава ПЭК (5'), JIC-Na нефракционированный (6). [JIC-Na] = [ПА] =0,0012 осново-моль/л
Рис. 4. Кривые потенциометрического титрования эквимольных смесей ПА с фракциями ЛС-Na I (1),. I+V (50:50 мол.%) (2), V (3). [ПА] =0,0012 осново-моль/лг
[НС1]=0,01 моль/л
Согласно этим данным, для трех первых фракций с уменьшением молекулярной массы JIC-Na возрастает способность частиц полиэлектролитного комплекса ПА — JIC-Na удерживаться в растворе. Такая закономерность, по-видимому, отражает улучшение растворимости за счет уменьшения молекулярных масс самих частиц поликомплекса по мере уменьшения молекулярной массы полианиона. Если бы этот фактор был единственным, то для фракции IV можно было ожидать еще более широкого интервала значений 0, в котором имеет место образование водорастворимых полиэлектролитных комплексов. Однако появление опалесценции в такой смеси наблюдается уже при 9~0,2. Ухудшение растворимости, вероятно, вызвано присутствием в этой фракции низкомолекулярных JIC-Na. О наличии низкомолекулярных JIC-Na в этой фракции свидетельствуют данные аналитической гель-хроматографии, указывающие на ее широкое ММР.
Практически полная нерастворимость частиц полиэлектролитного комплекса, образованного фракцией V, очевидно, связана с особенностями химического строения низкомолекулярных лигносульфонатов. В работе [14] установлено, что форма макромолекул лигносульфонатов с Ж<1104
отлична от рассмотренной ранее и приближается к стержнеобразной. В низкомолекулярных лигносульфонатах практически все сульфогруппы принимают участие в межмакромолекулярной реакции (рис. 1, кривая 6), т. е. их свойства приближаются к свойствам линейных полиэлектролитов. Благодаря высокому значению их эквивалентной массы (~600) такиеЛС-Na ведут себя в реакции с противоположно заряженными полиэлектролитами аналогичносинтетическим олигомерам [15]. Короткая цепочка JIC-Na в отличие от высокомолекулярных, рассмотренных выше, при взаимодействии с длинной цепочкой полимерного основания присоединяется к последней сразу значительной частью всех звеньев. Продукты незавершенных реакций того и другого типа (6<1) схематически изображены ниже.

(а — ЛС-Na высокомолекулярный, б— ЛС-Na низкомолекулярный). Случай бпредполагает значительно большую гидрофобизацию частиц поликомплекса по мере присоединения к ней олигомерных молекул ЛС-Na. Соответствующие поликомплексы выделяются из растворов в виде мелкодисперсных осадков уже при малых значениях Э.
Рассмотренная ситуация предполагает, что при не слишком высоких Э значительная доля олигомерных молекул ЛС-Na, введенных в реакцию, остается свободной, и состав полимерного комплекса непрерывно изменяется с ростом глубины превращения. Для таких систем естественно определять 8 учитывая это изменение состава полиэлектролитного комплекса и относить эту величину только к тем реагирующим цепям ЛС-Na, которые включены в частицу поликомплекса.
Из рис. 3 (кривая 5)видно, что кривая 0 (рН), рассчитанная с учетом действительного состава поликомплекса и изменения его при уменьшении рН, значительно круче (и смещена в область более глубоких значений 0), чем соответствующая кривая (кривая 5), рассчитанная по уравнению (1), не учитывающему изменения состава полиэлектролитного комплекса и предполагающему, что он имеет эквимольный состав во всей области изменения 8.
Малые начальные 8 и сравнительно низкие значения рН смесей в случае реакции ПА с исходным нефракционированный ЛС-Na, очевидно, также обусловлены присутствием в образце значительного количества низкомолекулярных ЛС-Na. Для подтверждения правильности этого предположения была изучена модельная смесь, которая состояла из ЛС-Na наиболее высоко- и наиболее низкомолекулярной фракций, взятых в равных эквивалентных количествах. Поведение этой смеси сравнивали с поведением каждой из фракций ЛС-Na.
На рис. 4 изображены кривые потенциометрического титрования смесей ПА с отдельными фракциями I и V, а также модельной смеси. Как и следовало ожидать, присутствие низкомолекулярных ЛС-Na приводит к смещению кривой титрования модельной смеси в область меньших значений рН по сравнению с кривой титрования исходной смеси ПА —I. Такое смещение можно вызвать введением в реакционные смеси низкомолекулярных электролитов — солей. Ионы, образующиеся при диссоциации солей, экранируют электростатическое взаимодействие противоположно заряженных цепей друг с другом, что приводит к смещению равновесия межмакромолекулярной реакции в сторону разрушения полимерного комплекса [15]. В данном случае роль такого электролита играет низкомолекулярная фракция V, короткие отрицательно заряженные цепочки которой не способны при рН<8,5 связываться с ПА, как это видно из сравнения кривых 5 и 6рис. 3 (кривая 6построена без учета реального состава образующихся полиэлектролитных комплексов). Поведение в изученных реакциях нефракционированных образцов ЛС-Na и смесей фракций свидетельствует об избирательности реакций по отношению к высокомолекулярным ЛС-Na.
Таким образом, в данной работе на примере взаимодействия JIC-Na и ПА в водных средах убедительно показано, что взаимодействие лигно-сульфонатов с положительно заряженными линейными полиэлектролитами (полиаминами) имеет электростатическую природу. Такие реакции, подобно изученным ранее, имеют кооперативный характер и сильно зависят от молекулярной массы лигносульфонатов в области невысоких значений последних. Особенности реакции с участием высокомолекулярных JIC-Na в первую очередь связаны со специфическим строением их макромолекул и хорошо согласуются с представлением о них как о частицах, имеющих в растворах форму дисков, причем основная часть сульфогрупп JIC-Na располагается в периферийной области таких макромолекул и способна вступать в образование солевых связей со звеньями линейного противоположно заряженного полиэлектролита.
Литература
1.Зезин А.В., Рогачева В.Б. В кн.: Успехи химии и физики полимеров. М.: Химия, 1973, с. 3.
2.Юсупов Р.В. Вопр. мед. химии, 1972, № 2, с. 189.
3.Bixler Н.., Michaels A.S. In: Encyclopedia of Polymer Science and Technology. 1969, v. 10, p. 765.
4.Chiancone E., Bruzzeci M.R., Antonini E. Biochemistry, 1966, v. 5, № 9, p. 2823.
5.Goran Strom. In: Annual Report of the Swedish Institute for Surface Chemistry, 1978/1979, p. 14.
6.Шулъга Г.M., Можейко Л.Н., Рекнер Ф.В., Метра А.Я. Изв. АН ЛатвССР, 1980, № 5, с. 126.
7.Закис Г.Ф., Можейко Л.Н., Телышева Г.М. Методы определения функциональных групп лигнина. Рига: Зинатне, 1975. 176 с.
8.Соколов О.М., Бабикова Н.Д., Богомолов Б.Д., Попова В.Л. Химия древесины, 1977, № 5, с. 73.
9.Харенко О.А., Харенко А.В., Калюжная Р.И., Изумрудов В.А., Касаикин В.А., Зезин А.Б., Кабанов В.А. Высокомолек. соед. А, 1979, т. 21, № 12, с. 2719.
10.Лигнины / Под. ред. Сарканена К. В. и Людвига К. X. М.: Лесная пром-сть, 1975. 631 с.
11.Можейко Л.Н., Сергеева В.И., Гринева Л.А., Балъцере Д.Ю. Химия древесины, 1972, № 11, с. 77.
12.Rezanowich A., Yean W. G., Goring D. A. I. J. Appl. Polymer Sci., 1964, v. 8, № 4, p. 1801.
13.Goring D.A. I., Vuong R., Gancet C, Chanzy H.J. Appl. Polymer Sci., 1979, v. 27, № 4, p. 931.
14.Иин У., Резанович А., Горинг Д. В кн.: Химия и биохимия лигнина, целлюлозы и гемицеллюлоз. М.: Лесная пром-сть, 1969, с. 158.
15.Харенко А.В. Дис. на соискание уч. ст. канд. хим. наук. М.: МГУ, 1977. 78 с.
|