БИОКОСНАЯ СИСТЕМА ГИДРОСФЕРЫ
Введение
Вода имеет особое значение для живого вещества Земли, она является обязательным условием его существования и главной составной частью. Вода составляет около 60 % суммарной массы живых организмов суши и 80 % массы организмов океана. Все физиологические процессы и биохимические реакции протекают в водных растворах. Огромное количество воды разлагается при фотосинтезе. Взаимодействие живого вещества с гидросферой является одним из генеральных процессов в биосфере.
1. Состав Мирового океана — результат
биогеохимической деятельности
организмов
Основную массу водной оболочки Земли образуют соленые воды Мирового океана, покрывающие 2
/з поверхности Земли. Их объем Равен примерно 1379×106
км3
, в то время как объем всех вод суши (включая ледники и подземные воды до глубины 5 км) — менее 90×106
км3
. Так как океанические воды составляют около 93 % всех вод биосферы, можно считать, что их химический состав определяет основные черты состава гидросферы в целом.
Современный химический состав океана представляет собой итог его длительного изменения под влиянием деятельности живых организмов. Образование первичного океана было обусловлено теми же процессами дегазации твердого вещества планеты, которые привели к формированию газовой оболочки Земли. По этой причине состав атмосферы и гидросферы тесно связан, их эволюция происходила также взаимосвязанно.
Как отмечено ранее, среди продуктов дегазации преобладали пары воды и углекислый газ. С того момента, как температура поверхности планеты опустилась ниже 100 °С, пары воды стали конденсироваться и образовывать первичные водоемы. На поверхности Земли возник процесс круговорота воды, который положил начало циклической миграции химических элементов в системе суша—океан—суша.
В соответствии с составом выделявшихся газов первые скопления воды на поверхности планеты были кислыми, обогащенными главным образом НС1, а также HF, H3
BO3
, H2
S. Вода океана прошла множество круговоротов. Кислые дожди энергично разрушали алюмосиликаты, извлекая из них легкорастворимые катионы — натрий, калий, кальций, магний, которые накапливались в океане. Катионы постепенно нейтрализовывали сильные кислоты, и воды древней гидросферы приобрели хлор-кальциевый состав.
Реклама

Среди разнообразных процессов трансформации дегазируемых соединений, очевидно, протекала деятельность сгущений термо-литотрофных бактерий. Появление цианобактерий, обитавших в воде, предохранявшей их от губительной ультрафиолетовой радиации, ознаменовало начало фотосинтеза и биогеохимического продуцирования кислорода. Уменьшение вследствие фотосинтеза парциального давления СО2
способствовало осаждению крупных масс карбонатов Fe2+
, затем Mg2+
и Са3+
.
Свободный кислород стал поступать в воды древнего океана. На протяжении длительного отрезка времени восстановленные и недоокиеденные соединения серы, двухвалентного железа и марганца были окислены. Состав океанической воды приобрел хлоридно-сульфатный состав, близкий к современному.
Химические элементы в гидросфере находятся в разнообразных формах. Среди них наиболее характерны простые и сложные ионы, а также молекулы, находящиеся в состоянии сильно разбавленных растворов. Распространены ионы, сорбционно связанные с частицами коллоидных и субколлоидных размеров, присутствующими в морской воде в виде тонкой взвеси. Особую группу составляют элементы органических соединений.
Общее количество растворенных соединений в морской воде (соленость)
в поверхностных слоях океанов и окраинных морей колеблется от 3,2 до 4 %. Во внутриконтинентальных морях соленость меняется в более широких пределах. Средняя соленость Мирового океана принята равной 35%.
Еще в середине XIX в. ученые обнаружили замечательную геохимическую особенность океанической воды: несмотря на колебания солености, соотношение главных ионов остается постоянным. Солевой состав океана является своего рода геохимической константой.
В результате настойчивой работы ученых многих стран был накоплен обширный аналитический материал, характеризующий содержание в воде морей и океанов не только главных, но и рассеянных химических элементов. Наиболее обоснованные данные о средних значениях (кларках) химических элементов в воде Мирового океана приведены в сводках Э.Д. Голдберга (1963), А.П. Виноградова (1967), Б. Мейсона (1971), Г. Хорна (1972), А.П. Лисицина (1983), К.Н. Турекиана (1969). В табл. 4.1 использованы результаты преимущественно двух последних авторов.
Как видно из приведенных данных, основную массу растворенных соединений составляют хлориды распространенных щелочных и щелочно-земельных элементов, меньше содержится сульфатов, еще меньше гидрокарбонатов. Концентрация рассеянных элементов, единицей измерения которых служит мкг/л, на три математических порядка ниже, чем в горных породах. Диапазон значений кларков рассеянных элементов достигает 10 математических порядков, т.е. примерно такой же, как в земной коре, но соотношения элементов совершенно иные. Отчетливо доминируют бром, стронций, бор и фтор, концентрация которых выше 1000 мкг/л. В значительном количестве присутствуют иод, барий, их концентрация превышает 10 мкг/л.
Реклама

Таблица 4.1
Содержание растворимых форм химических элементов в Мировом океане
| Химический элемент или ион
|
Средняя концентрация
|
Отношение концентрации в сумме солей к кларку гранитного слоя
|
Общая масса, млн т
|
| в воде, мкг/л
|
в сумме солей, 10-4
%
|
| С1 |
19 353 000,0 |
5529,0 |
3252,0 |
26513610000 |
| SО4
2
-
|
2 701 000,0 |
771,0 |
— |
3700370000 |
| S |
890000,0 |
254,0 |
63,0 |
1216300000 |
| НСО3
-
|
143000,0 |
41,0 |
— |
195910000 |
| Na |
10764000,0 |
3075,0 |
14,0 |
14746680000 |
| Mg |
1297000,0 |
371,0 |
3,1 |
1776890000 |
| Са |
408000,0 |
116,0 |
0,5 |
558960000 |
| К |
387000,0 |
111,0 |
0,4 |
530190000 |
| Вг |
67 300,0 |
1922,9 |
874,0 |
92 201 000 |
| Sr |
8100,0 |
231,4 |
1,0 |
1 1 097 000 |
| В |
4450,0 |
127,1 |
13,0 |
6 096 500 |
| SiO2
|
6200,0 |
176,0 |
— |
8494000 |
| Si |
3000,0 |
85,0 |
0,00028 |
4 1 10 000 |
| F |
1300,0 |
37,1 |
0,05 |
1 781 000 |
| N |
500,0 |
14,0 |
0,54 |
685 000 |
| Р |
88,0 |
2,5 |
0,0031 |
120 560 |
| I |
64,0 |
1,8 |
3,6 |
87690 |
| Ва |
21,0 |
0,57 |
0,00084 |
28770 |
| Мо |
10,0 |
0,29 |
0,22 |
13700 |
| Zn |
5,0 |
0,14 |
0,0027 |
6850 |
| Fe |
3,4 |
0,097 |
0,0000027 |
4658 |
| U |
3,3 |
0,094 |
0,036 |
4521 |
| As |
2,6 |
0,074 |
0,039 |
3562 |
| Al |
1,0 |
0,029 |
0,00000036 |
1370 |
| Ti |
1,0 |
0,029 |
0,0000088 |
1370 |
| Сu |
0,90 |
0,025 |
0,001 1 |
1233 |
| Ni |
0,50 |
0,014 |
0,00054 |
685 |
| Mn |
0,40 |
0,011 |
0,000016 |
548 |
| Cr |
0,20 |
0,0057 |
0,00017 |
274 |
| Hg |
0,15 |
0,0043 |
0,130 |
206 |
| Cd |
0,11 |
0,0031 |
0,019 |
151 |
| Ag |
0,10 |
0,0029 |
0,065 |
137 |
| Se |
0,09 |
0,0026 |
0,019 |
123 |
| Co |
0,03 |
0,00086 |
0,0012 |
41,1 |
| Ga |
0,03 |
0,00086 |
0,0012 |
41,1 |
| Pb |
0,03 |
0,00086 |
0,0012 |
41,1 |
| Zr |
0,026 |
0,00070 |
0,0000041 |
34,0 |
| Sn |
0,020 |
0,00057 |
0,00021 |
27,4 |
| Аu |
0,011 |
0,00031 |
0,26 |
15,1 |
Часть находящихся в воде металлов — молибден, цинк, уран, титан, медь — имеет концентрацию от 1 до 10 мкг/л. Концентрация никеля, марганца, кобальта, хрома, ртути, кадмия значительно ниже — сотые и десятые доли мкг/л. В то же время железо и алюминий, играющие роль главных элементов в земной коре, в океане имеют концентрацию более низкую, чем молибден и цинк. В наименьшем количестве в океане растворены такие элементы, как ниобий, скандий, бериллий и торий.
Для определения некоторых геохимических и биогеохимических показателей необходимо знать концентрацию элементов не только в морской воде, но и в твердой фазе растворимых веществ, т.е. в сумме солей морской воды. В таблице приведены данные, для расчета которых величина средней солености принята равной 35 г/л.
Как было показано выше, ведущим фактором эволюции химического состава океана на протяжении геологической истории была суммарная биогеохимическая деятельность живых организмов. Не менее важную роль организмы играют в современных процессах дифференциации химических элементов в океане и выведения их масс в осадок. Согласно биофильтрационной гипотезе, разработанной А. П. Лисициным, планктонные (преимущественно зоопланктонные) организмы ежедневно профильтровывают через свои тела около 1,2×107
км3
воды, или около 1 % объема Мирового океана. При этом тонкие минеральные взвеси (частицы размером 1 мкм и менее) связываются в комочки (пеллеты).
Размеры пеллетов от десятков микрометров до 1 — 4 мм. Связывание тонких взвесей в комочки обеспечивает более быстрое оседание на Дно взвешенного материала. Одновременно часть растворенных в в
оде химических элементов в телах организмов переходит в нерастворимые соединения. Наиболее распространенными примерами биогеохимического связывания растворенных элементов в нерастворимые соединения могут служить образования известкоых (кальцитовых) и кремниевых (опаловых) скелетов планктонныx организмов, а также извлечение карбоната кальция известковыми водорослями и кораллами.
Среди пелагических илов
(глубоководных отложений океана) можно выделить две группы. Первые состоят преимущественно из биогенных образований планктона, вторые образованы в основном частицами не биогенного происхождения. В первой группе наиболее распространены известковые (карбонатные) илы, во второй — глинистые илы. Карбонатные илы занимают около трети площади дна Мирового океана, глинистые — более четверти. В карбонатных осадках возрастает концентрация не только кальция и магния, но также стронция и йода. В илах, где преобладают глинистые компоненты, значительно больше металлов. Некоторые элементы очень слабо выносятся из раствора в илы и постепенно накапливаются в морской воде. Их следует называть талас-софилъными.
Рассчитав отношение между концентрациями в сумме растворимых солей морской воды и илах, мы получим величину коэффициента талассофилъности КТ
,
показывающего, во сколько раз данного элемента больше в солевой части океанической воды по сравнению с осадком. Талассофильные элементы, аккумулирующиеся в растворенной солевой части воды, имеют следующие коэффициенты КТ
:
Химический элемент
|
По отношению
к глинистым илам.
|
По отношению к известковым илам
|
| Иод |
180 0 |
36,0 |
| Бром |
27 5 |
27 5 |
| Хром |
27 0 |
27 0 |
| Сера |
19 5 |
19 5 |
| Натрий |
. 7 7 |
15 4 |
| Магний |
1 8 |
0 9 |
| Стронций |
1 3 |
0 1 |
| Бор . |
06 |
2 3 |
| Калий |
04 |
3 8 |
| Молибден |
0 01 |
10 0 |
| Литий |
0.09 |
1.0 |
Зная массу элемента в Мировом океане и величину его годового поступления, можно определить скорость его удаления из океанического раствора. Например, количество мышьяка в океане составляет примерно 3,6×109
т, с речным стоком приносится 74×103
т/год. Следовательно, за период, равный 49 тыс. лет, происходит полное удаление всей массы мышьяка из Мирового океана.
Оценку времени нахождения элементов в растворенном состоянии в океане предпринимали многие авторы: Т.Ф. Барт (1961), Э.Д. Гольдберг (1965), Х.Дж. Боуэн (1966), А.П.Виноградов (1967) и др. Данные разных авторов имеют большие или меньшие расхождения. Согласно нашим расчетам, периоды полного удаления растворенных химических элементов из Мирового океана характеризуются следующими интервалами времени (в годах, в последовательности увеличения периода в каждом ряду):
n×102
: Th, Zr, Al, Y, Sc
n×103
: Pb, Sn, Mn, Fe, Co, Cu, Ni, Cr, Ti, Zn
n×104
: Ag, Cd, Si, Ba, As, Hg, N
n×105
: Mo, U, I
n×106
: Ca, F, Sr, В, К
n×107
: S, Na
n×108
: С1, Br
При всей ориентировочности таких расчетов порядки полученных величин позволяют выделить группы рассеянных элементов, различающиеся длительностью нахождения в океаническом растворе. Элементы, наиболее интенсивно концентрирующиеся в глубоководных илах, имеют наименьшую длительность нахождения в океане. Таковы торий, цирконий, иттрий, скандий, алюминий. К ним близки периоды нахождения в океаническом растворе свинца, марганца, железа, кобальта. Большая часть металлов полностью выводится из океана на протяжении нескольких тысяч или десятков тысяч лет. Талассофильные элементы находятся в растворенном состоянии сотни тысяч лет и более.
Значительные массы рассеянных элементов в океане связываются дисперсным органическим веществом. Его основным источником служат отмирающие планктонные организмы. Процесс разрушения их остатков наиболее активно происходит до глубины 500—1000 м. Поэтому в осадках шельфовых и неглубоких приконтинентальных морей скапливаются огромные массы дисперсного органического вещества морских организмов, к которым добавляются органические взвеси, вынесенные речным стоком с суши.
Основная часть органического вещества океана находится в растворенном состоянии и лишь 3 — 5 % в виде взвеси (Виноградов А. П., 1967). Концентрация этих взвесей в воде невелика, но их общая масса во всем объеме океана весьма значительна: 120 — 200 млрд т. Ежегодное накопление высокодисперсного органического детритуса в осадках Мирового океана, по данным В.А.Успенского, превышает 0,5×109
т.
Дисперсное органическое вещество сорбирует и увлекает в осадки определенный комплекс рассеянных элементов. Об их содержании с известной условностью можно судить по микроэлементарному составу крупных скоплений органического вещества — залежей каменного угля и нефти. Концентрация элементов в этих объектах обычно приводится по отношению к золе; не менее важны Данные по отношению к исходному, неозоленному материалу.
Как видно из табл. 4.2, микроэлементный состав каменных углей и нефти принципиально различается.
Таблица 4.2
Средние концентрации рассеянных металлов в каменном угле и нефти, 10-4
%
| Химический элемент
|
В сухом веществе каменных углей (В. Р. Клер, 1979)
|
В золе каменных углей (Ф.Я.Сапрыкин, 1975)
|
В золе нефтей (К. Краускопф, 1958)
|
| Ti |
1600 |
9200 |
— |
| Мn |
155 |
— |
— |
| Zr |
70 |
480 |
50-500 |
| Zn |
50 |
319 |
100-2500 |
| Cr |
18 |
— |
200-3000 |
| V |
17 (10-200) |
— |
500-25000 |
| Сu |
11 |
— |
200-8000 |
| Pb |
10 |
93 |
50-2000 |
| Ni |
5 |
214 |
1000-45000 |
| Ga |
4,5(0,6-18) |
64 |
3-30 |
| Co |
2 |
63 |
100-500 |
| Mo |
2 |
21 |
50-1500 |
| Ag |
1,5 |
— |
5 |
| Sn |
1,2 |
15 |
20—500 |
| Hg |
0,2 |
— |
— |
| As |
— |
— |
1500 |
| Ba |
— |
— |
500-1000 |
| Sr |
— |
— |
500-1000 |
Примечание
. Прочерк означает отсутствие данных
В нефти иное соотношение значительно более высокая концентрация многих рассеянных элементов. Высокое содержание титана, марганца и циркония в каменных углях обусловлено минеральными примесями. Среди рассеянных металлов наибольшая концентрация характерна для цинка, хрома, ванадия, меди и свинца.
В органическом веществе активно накапливаются многие токсичные элементы (мышьяк, ртуть, свинец и др.), которые беспрестанно удаляются из океанической воды. Следовательно, дисперсное органическое вещество, как и минеральные взвеси, выполняет роль глобального сорбента, регулирующего содержание рассеянных элементов и предохраняющего среду Мирового океана от опасных уровней их концентрации. Количество рассеянных элементов, связанное в дисперсном органическом веществе, весьма значительно, учитывая, что масса вещества в осадочных породах в сотни раз превышает суммарное количество всех залежей каменных углей, углистых сланцев и нефти. В соответствии с данными Дж. Ханта (1972), Н.Б. Вассоевича (1973), А.Б. Ронова (1976) общее количество органического вещества в осадочных породах составляет (15×20)×1015
т.
Массы рассеянных элементов, аккумулированные в органическом веществе осадочной толщи Земли, измеряются многими миллиардами тонн.
2. Особенности геохимии поверхностных
вод суши
Океан беспрестанно пополняется за счет стока воды с суши, который согласно данным М.И.Львовича (1986) равен примерно 44×103
м3
/год[1]
. Следовательно, меньше чем за 35 тыс. лет в океан поступит столько воды, сколько в нем находится в настоящее время. Динамическое постоянство объема океана поддерживается испарением и переносом через атмосферу в парообразном состоянии 44×103
км3
/год воды, выпадающей на сушу в виде атмосферных осадков. Ниже приведен годовой водный баланс Земли (по М.И.Львовичу, 1986):
Элементы водного баланса Объем, км3
Дренируемая часть суши:
осадки.........................................................................106000
речной сток................................................................ 44230
испарение................................................................... 61 770
Бессточная часть суши:
осадки ......................................................................... 7500
испарение................................................................... 7500
Мировой океан:
осадки .........................................................................411 600
приток речных вод..................................................... 44230
испарение...................................................................455 830
Земля в целом:
осадки.........................................................................525 100
испарение...................................................................525 100
Химический состав выпавших осадков при взаимодействии с растительностью и почвой изменяется под влиянием гумусовых кислот, метаболических выделений высших растений и почвенных микроорганизмов. Конечный продукт разрушения органического вещества — углекислый газ — хорошо растворяется в воде с образованием угольной кислоты. Все это усиливает растворяющую способность поверхностных вод по отношению к минеральному веществу земной коры. В то же время стекающая по поверхности суши вода захватывает частицы минерального вещества, преобразованного под влиянием жизнедеятельности организмов, и переносит их в форме взвеси. Таким образом, состав, как растворимых соединений, так и тонких взвесей в значительной мере обусловлен жизнедеятельностью организмов.
Растворимые соединения в речном стоке.
Речные воды создают мощный геохимический поток, играющий важную роль в общепланетарном массообмене между Мировой сушей и Океаном. Мобилизация химических элементов, включающихся в водную миграцию, происходит в результате деятельности живых организмов. Речные воды следует рассматривать как сложные растворы, содержащие дисперсные взвеси и соединения, находящиеся в истинно растворимом состоянии.
В речных водах различают следующие главные формы химических элементов:
1) простые и комплексные ионы;
2) нейтральные молекулы (обе группы форм имеют размер 2 — 3 нм и менее);
3) коллоидные частицы (размер менее 0,1 мкм), состоящие из устойчивых гумусовых веществ, аморфных продуктов разрушения глинистых минералов и оксидов железа;
4) высокодисперсные частицы (размер от 0,1 до 1 — 2 мкм), состоящие преимущественно из глинистых минералов;
5) крупные взвешенные частицы (размер от 2 — 3 до 10 мкм), представленные обломочными минералами.
Минерализация воды и количество дисперсных взвесей (мутность)
в разных реках сильно варьируют. В соответствии с данными геохимика Д. Ливингстона (1963), средняя минерализация рек Мира принята равной 120 мг/л. Исходя из этой цифры и объема годового речного стока в 44×1015
л/год, количество растворенных соединений, ежегодно выносимых с суши, составляет 5,3×102
т. Согласно данным А.П. Лисицина (1983), среднее содержание взвешенных дисперсных частиц в континентальном стоке равно 500 мг/л. Следовательно, вынос тонкодисперсного вещества всеми реками равен 22×109
т/год, т.е. в 4,2 раза больше, чем растворимых соединений.
Соотношение масс растворимых соединений и твердых взвесей в речном стоке в значительной мере зависит от характера растительности суши. Факты свидетельствуют, что на протяжении геологической истории это соотношение неоднократно менялось.
На основании этого французский почвовед Г. Эрар (1956) разработал теорию биорексистазии. Эпохи биостазии (биологического павновесия)
характеризуются широким распространением устойчивых лесных фитоценозов, препятствующих механической эрозии почв, но способствующих вовлечению химических элементов в водную миграцию в растворимых формах. В эпохи рексистазии биологическое равновесие нарушается, и площадь лесов сильно сокращается. Вследствие этого активизируются денудационно-эро-зионные процессы и в речном стоке преобладают твердые взвеси.
В составе растворимых соединений в речных водах преобладают анионы [НСО3
]-
, [SO4
]2-
, Cl-
. В варьирующих микроколичествах находятся все остальные элементы.
Известны многочисленные попытки объяснить концентрацию рассеянных химических элементов в природных водах с помощью теории ионных растворов, причем в качестве главного рассматривался один фактор: ионный потенциал либо концентрация водородных ионов (рН), либо окислительно-восстановительный потенциал. Р. Гаррелс и Ф. Маккензи (1971) для объяснения распределения элементов в природных водах использовали физико-химические расчеты исходя из модели: неразбавленный раствор — осадок. В этом случае нахождение элемента в растворе зависит от сочетания окислительно-восстановительных и кислотно-щелочных условий, которые наглядно представлены на Eh — рН-диаграммах. Для процессов растворения — осаждения макрокомпонентов такой подход вполне приемлем, но для рассеянных элементов не всегда отвечает действительности. По этой причине наряду с попытками применить к природным водным растворам те или иные теории очень важно обобщить имеющиеся фактические данные.
В речных водах содержатся растворимые формы рассеянных элементов, не захваченные в биологический круговорот. Текучие воды на поверхности суши обычно имеют рН от 4,5 до 8,5. При таких значениях рН многие металлы (цинк, хром, медь, бериллий, свинец, кадмий, никель, кобальт и др.) могут находиться в растворенном состоянии, выпадать в осадок и вновь переходить в раствор. Но их фактическое содержание в природных водах так незначительно, что регулирующее действие рН не сказывается. Концентрация металлов в чистой воде часто ниже их содержания в растворах после осаждения гидроксидов. В отдельных случаях, когда образуются ничтожно малые количества нерастворимых гидроксидов металлов, они находятся в виде субколлоидных сгустков, которые не выпадают в осадок, а в состоянии разбавленных коллоидных растворов активно мигрируют. В то же время находящиеся в растворе элементы могут образовывать комплексные соединения с органическими веществами, сорбироваться гелями соединений макроэлементов (в первую очередь гидроксидами железа), высокодисперсными частицами глин и осаждаться в таких условиях, когда теоретически этого не должно быть.
Значительная часть рассеянных элементов присутствует в природных водах не в виде простых ионов, а в форме комплексных соединений. В этом случае устойчивость элемента в растворе сильно возрастает и не ограничивается теми кислотно-щелочными и окислительно-восстановительными условиями, в которых может находиться в растворе простой ион. Как показал В. В. Щербина (1972), образование неорганических комплексных соединений характерно для хрома, никеля, кобальта, меди, цинка, урана. При этом возникают соединения типа [Cu(NH3
)2
]+
; [Cu(CO3
)2
]2-
; [ZnQ3
]-
; [Zn(S04
)2
]2
- и др.
Весьма важное значение для водной миграции имеют комплексные органические, особенно внутрикомлексные (хелатные) соединения металлов. В этих соединениях ион металла имеет ионную и координационную связи с отдельными функциональными группами внутри молекулы. Ионная связь осуществляется обычно группами СООН, ОН, NH2
, SO3
H, координационная связь — группами —NH2
, NH—N=, =NOH—, -ОН, =С=О, =S=0, =S—. В комплексообразовании принимают участие аминокислоты, ароматические соединения (полифенолы), кислоты жирного ряда, гетероциклические соединения типа хинолина, гуминовые и фульвокислоты (Якушевская И.В., 1973). Устойчивость комплекса зависит от поляризуемости катиона-комплексообразователя и органического соединения, реакции среды и концентрации рассеянного металла. Обычно комплексы устойчивы в слабокислых и нейтральных водах, при сильном возрастании рН они разрушаются. Наибольшая устойчивость хелатных соединений соответствует низкой концентрации металла, увеличение концентрации приводит к их разрушению.
Растворимые комплексные органические соединения металлов распространены очень широко. На территории лесных ландшафтов с кислыми почвами эти соединения являются преобладающей формой растворенных металлов. С усилением засушливости и соответственным повышением рН почвенных растворов и поверхностных вод значение комплексов уменьшается, хотя и остается достаточно высоким.
Геохимические и биоклиматические различия водосборных площадей и разнообразие форм рассеянных элементов обусловливают сильную вариацию их концентраций в речных водах. Поэтому определение величины средней концентрации в водах суши более условно, чем в воде океана.
Наиболее обоснованные данные, полученные А.П.Виноградовым (1967), А.П. Лисициным (1978), Э. Голдбергом (1965), Х. Боуэном (1966), К. Турекианом (1969) использованы для расчетов, приведенных в табл. 4.3.
Несмотря на то, что общая минерализация пресных речных вод значительно меньше соленых морских, глобальный вынос рассеянных элементов в растворенном состоянии весьма значителен. Для фтора, стронция, железа, алюминия он равен миллионам тонн, для кальция, натрия, магния, сульфатной серы, хлора, кремния — сотням миллионов тонн, для калия — десяткам миллионов тонн, для брома, йода, бора, а также цинка, марганца и меди сотням тысяч тонн в год. Большая часть рассеянных элементов удаляется с суши в количестве десятков тысяч тонн в год. Лишь отдельные элементы выносятся в меньшем количестве.
Таблица 4.3
Содержание растворимых форм химических элементов в речных водах и интенсивность их вовлечения в водную миграцию
| Химический элемент и ион
|
Средняя концентрация
|
Глобальный вынос с речным стоком, тыс т/год
|
Коэффициент водной миграции
|
| в воде, мкт/л
|
в сумме солей, %
|
| С1 |
6400 |
5,33 |
262400 |
313,0 |
| SO4
2
-
|
12000 |
10,00 |
492 000 |
— |
| S |
3960 |
3,30 |
162360 |
82,5 |
| Со
pr
|
6900 |
5,75 |
283 000 |
— |
| НСО3
|
58500 |
488,75 |
2398500 |
— |
| Скар6
|
11 508 |
9,58 |
471 828 |
— |
| Са |
13000 |
10,80 |
533000 |
4,6 |
| Mg |
3300 |
2,75 |
135300 |
2,3 |
| Na |
4500 |
3,75 |
184500 |
1,7 |
| К |
1500 |
1,25 |
61500 |
0,5 |
| NCV |
1000 |
0,83 |
41000 |
— |
| N |
225 |
0,19 |
9225 |
— |
| SiO2
|
13100 |
10,9 |
537100 |
— |
| Si |
5700 |
4,75 |
233 700 |
0,15 |
| Fe |
670 |
0,558 |
27470 |
0,15 |
| Al |
75 |
625×10-4
|
3075 |
0,01 |
| Sr |
80 |
667×10-4
|
3280 |
2,90 |
| P |
20 |
11,7×10-4
|
820 |
0,21 |
| F |
40 |
333×10~4
|
1640 |
0,46 |
| Ba |
25 |
208,0×10-4
|
1025 |
0,31 |
| Br |
20 |
167,0×10-4
|
820 |
76,0 |
| Zn |
20 |
167,0×10-4
|
820 |
3,27 |
| В |
18 |
150,0×10-4
|
738 |
15,0 |
| Mn |
10 |
83,0×10-4
|
410 |
0,12 |
| Сu |
7 |
58,0×10~4
|
287 |
2,64 |
| Ti |
4 |
33,0×10-
4
|
164 |
0,01 |
| I |
3 |
25,0×10-4
|
123 |
50,0 |
| Zr |
2,5 |
21,0×10-4
|
103 |
0,12 |
| As |
2 |
17,0×10~4
|
82 |
8,95 |
| N1 |
2,5 |
21,0×10-4
|
123 |
0,81 |
| Li |
2,2 |
18,0×10~4
|
90 |
0,08 |
| Rb |
1,8 |
15,0×10~4
|
74 |
0,08 |
| V |
1,0 |
8,3×10~4
|
41 |
0,11 |
| Cr |
1,0 |
8,3×10~4
|
41 |
0,24 |
| Mo |
0,9 |
7,5×10-4
|
37 |
5,77 |
| Pb |
1 |
8,3×10-
4
|
41 |
0,52 |
| Sb |
0,9 |
7,5×10~4
|
37 |
37,5 |
| Sn |
0,5 |
4,2×10~4
|
21 |
1,56 |
| U |
0,3 |
2,5×10-4
|
12 |
0,96 |
| Co |
0,25 |
2,1×10~4
|
10 |
0,29 |
| Ag |
0,2 |
1,7×10~4
|
8,2 |
35,42 |
| Cd |
0,2 |
1,7×10~4
|
8,2 |
10,63 |
| Ga |
0,09 |
0,75×10-4
|
3,7 |
0,04 |
| Hg |
0,07 |
0,58×10~4
|
2,9 |
17,58 |
| Th |
0,05 |
0,42×10-4
|
2,1 |
0,03 |
| Sc |
0,02 |
0,17×10~4
|
0,8 |
0,02 |
Интенсивность водной миграции химических элементов.
Представление о выносе растворенных масс элементов должно быть дополнено оценкой степени интенсивности вовлечения их в водную миграцию. Б. Б. Полынов в 1933 г. показал, что интенсивность водной миграции элемента определяется не его содержанием в воде, а отношением содержания в воде и в дренируемой горной породе. А. И.Перельман (1974) предложил использовать коэффициент водной миграции КВ
,
который равен отношению концентраций элемента в сухом остатке воды и в породе. Оценивая интенсивность вовлечения элемента в водную миграцию в глобальном масштабе, необходимо рассчитать отношение среднего содержания в твердом остатке речных вод к кларку этого же элемента в гранитном слое континентов.
По интенсивности вовлечения в водную миграцию, характеризуемой Къ
,
элементы группируются следующим образом (в по-следовальности уменьшения числового значения КВ
в каждом ряду):
n×102
: С1
n×10: S, I, Br, Ag, Sb, Hg, В, Cd
n: As, Mo, Ca, Zn, Sr, Cu, Mg, Na, Sn
n×10-1
: U, Ni, Pb, F, Co, Ba, Cr, P, Mn, Si, V, Zr
n×10-20
: Ga, Th, Al, Ti, Sc
Миграция элементов в составе речных взвесей.
Рассмотренные факты и выводы относятся к элементам, находящимся в растворенном состоянии. Иное соотношение химических элементов и их масс наблюдается в веществе, мигрирующем в речных водах во взвесях. Это объясняется тем, что масса взвесей в годовом стоке рек более чем вчетверо превышает массу растворимых соединений и что состав речных взвесей имеет специфические особенности.
Речные взвеси состоят преимущественно из высокодисперсных глинистых частиц, мелких обломков кварца и сгустков гидрокси-Дов железа. Концентрация большей части элементов (кремния, алюминия, железа и др.) во взвесях значительно выше, чем в сумме растворимых соединений в речной воде. В то же время для кальция характерно обратное соотношение.
А.П. Лисицин и его сотрудники показали, что основная масса Рассеянных элементов, переносимых речными водами, связана со взвесями. Как следует из данных, приведенных в табл. 4.4, во взвешенном веществе рек переносится: свыше 98 % массы элементов с очень низкими коэффициентами водной миграции КВ
< 0,5) — алюминия, титана, галлия, свинца, тория, скандия; от 90 до 98 % массы элементов со значениями Къ
от 0,05 до 0,9 — кремния, железа, марганца, фосфора, бария, циркония, рубидия, хрома, кобальта, никеля. Даже некоторые элементы, обладающие высокой интенсивностью водной миграции и значениями Кв
от 1 до 10, мигрируют преимущественно не в растворенном состоянии. От 65 до 85 % массы магния, цинка, меди, молибдена, ежегодно выносимой реками с территории Мировой суши, переносится в формах, фиксированных на взвешенных частицах. Лишь для ограниченного числа элементов — азота, хлора, серы, кальция, натрия, брома — характерно преобладание масс водорастворимых соединений в речном стоке.
Таблица 4.4
Вынос химических элементов, содержащихся во взвешенном веществе рек
| Химический элемент
|
Концентрация, мкг/л (В. В. Гордеев, 1983)
|
Годовой вынос взвешенных форм элементов, 103
т/год
|
Сумма растворенных и взвешенных форм, 103
т/год
|
Количество взвешенных форм от суммарного выноса, %
|
| Si |
117000 |
4797000 |
5030700 |
95,4 |
| А1 |
38200 |
1 566 200 |
1 569 275 |
99,8 |
| Fe |
23500 |
963 000 |
990970 |
97,2 |
| Са |
11500 |
471 500 |
1 004 500 |
46,9 |
| К |
6900 |
282 900 |
344 400 |
82,1 |
| Mg |
5750 |
235750 |
371 050 |
63,5 |
| Na |
4600 |
188600 |
373 100 |
50,4 |
| Ti |
1840 |
75440 |
75604 |
92,8 |
| Р |
510 |
20910 |
21730 |
96,2 |
| Mn |
500 |
20500 |
20910 |
98,0 |
| Ва |
280 |
11480 |
12505 |
91,8 |
| Zn |
143 |
5863 |
6683 |
87,7 |
| Zr |
92 |
3772 |
3875 |
97,3 |
| Sr |
69 |
2829 |
6109 |
46,3 |
| Pb |
69 |
2829 |
2870 |
98,6 |
| Rb |
55 |
2255 |
2329 |
96,8 |
| Cr |
60 |
2460 |
2501 |
98,4 |
| Ni |
38,6 |
1583 |
1705 |
92,8 |
| Cu |
37 |
1517 |
1825 |
83,1 |
| В |
32 |
1312 |
2050 |
64,0 |
| Li |
14 |
574 |
664 |
86,4 |
| Sc |
9,2 |
377 |
380 |
99,2 |
| Co |
8,3 |
340 |
350 |
97,1 |
| Ga |
8,3 |
340 |
344 |
98,8 |
| Th |
4,6 |
187 |
189 |
99,6 |
| As |
2,3 |
94,3 |
176 |
53,4 |
| Mo |
1,4 |
57,4 |
94,0 |
60,6 |
| Sb |
0,9 |
36,9 |
74,0 |
50,0 |
| Ag |
0,6 |
24,6 |
32,8 |
75,0 |
| Cd |
0,32 |
13,1 |
21,9 |
59,8 |
| U |
0,14 |
57,4 |
17,7 |
32,2 |
Важно отметить, что относительное содержание химических элементов в речных взвесях не соответствует кларкам земной коры. Следовательно, взвешенное вещество рек — не механически измельченный материал земной коры, а результат его определенного преобразования. Интенсивность такого преобразования может быть оценена значением коэффициента Кр
,
равным отношению средней концентрации элемента в речной взвеси к его кларку гранитного слоя земной коры континентов.
По значениям коэффициента Кр
можно выделить три группы элементов. Элементы первой группы характеризуются значениями Кр
меньше единицы, т.е. уменьшением относительного содержания во взвесях по сравнению с кларком гранитного слоя земной коры. В эту группу входят кальций и натрий, а также строн-Чии, барий, литий. Относительное содержание магния во взвесях по отношению к земной коре существенно не меняется (Кр
=1).
Вторую группу образуют элементы, у которых Кр
равны или немногим более единицы. Таковы титан, цирконий, галлий, а также железо и марганец. К третьей группе относятся элементы, концентрация которых возрастает во взвесях, а значение Кр
—
от 2 до 9. Эту группу образуют тяжелые металлы: свинец, цинк, медь, никель, кобальт, хром, ванадий, кадмий.
Ясно выраженная аккумуляция тяжелых металлов в речных взвесях дает основание предполагать, что это явление связано с биогеохимическими процессами. В водную миграцию на суше вовлекаются химические элементы, не захваченные в биологический круговорот. Возможно, что вынос значительных масс тяжелых металлов, прочно фиксированных на дисперсных продуктах выветривания и почвообразования, является одним из механизмов предохранения живого вещества суши от избыточных масс этих элементов.
Природные геохимические аномалии в поверхностных водах суши.
На участках высоких концентраций рассеянных химических элементов поверхностные воды обогащаются элементами, присутствующими в избытке. Так образуются природные гидрогеохимические аномалии.
Особенно заметное обогащение происходит в тех случаях, когда поверхностные и грунтовые воды контактируют с сульфидными рудами. Окисление сульфидов железа сопровождается гидролизом сульфатов, выпадением гидроксидов железа и образованием серной кислоты, которая усиливает растворяющую способность воды. Возникающие при окислении сульфидов цинка, меди, никеля сульфаты хорошо растворимы и активно вовлекаются в водную миграцию.
В результате реакций с другими растворенными соединениями и взаимодействия с поверхностью взвешенных частиц значительная часть мигрирующих металлов относительно быстро выводится из раствора и их концентрация достигает уровня местного геохимического фона По этой причине протяженность природных гидрогеохимических аномалий в речных водах небольшая и редко превышает несколько сотен метров.
На значительно большее расстояние — до нескольких километров — распространяются аномально высокие концентрации в донных осадках, представляющих собой осажденные частицы водных взвесей. Определение металлов в воде небольших водотоков и особенно в их донных отложениях успешно использовалось при рекогносцировочных геохимических поисках месторождений руд во многих районах нашей страны, а также в Канаде, США, Англии, Замбии, Уганде, на Филиппинах и в других странах.
Аккумуляция химических элементов в воде оказывает влияние на водные биоценозы. Широко распространены различные проявления эвтрофизации небольших плохо проточных водоемов. Концентрация металлов в плавающих и погруженных растениях в водоемах конечного стока, как правило, выше среднепланетарных значений. Высокие природные концентрации некоторых элементов в поверхностных и грунтовых водах отдельных районов вызывают повышенное содержание этих элементов в местной растительности. Если растительность используется в качестве корма для сельскохозяйственных животных, то это вызывает заболевание скота. Подобные случаи изучены в США Р. Ибенсом и X. Шаклет-том (1973), в Ирландии и Англии Дж.Уэббом, И.Торнтоном и К.Флетчером (1966), в нашей стране В.В.Ковальским (1974).
В заключение необходимо подчеркнуть, что природные геохимические аномалии в поверхностных водах Мировой суши очень локальны и не оказывают заметного влияния на баланс масс химических элементов в глобальных биогеохимических циклах.
3. Трансформация геохимического состава
природных растворов на контакте речных и
океанических вод
С суммарным речным стоком в океан поступают огромные массы химических элементов. Ежегодно с речным стоком выносится в составе взвесей и растворенных форм соответственно (млн. т): железа — 963 и 27; марганца — 20,5 и 0,41; цинка — 5,86 и 0,82; меди— 1,51 и 0,28; свинца — 2,8 и 0,04; никеля — 1,58 и 0,12; кобальта — 0,34 и 0,01. Согласно данным А. П. Лисицина и др. (1983), из этого количества более 92 % выпадает в краевых морях и особенно в устьях рек, лишь 7,8 % достигает глубоководных областей океана.
Вместе с осаждением значительной части взвесей и соединений главных химических элементов осаждаются и рассеянные металлы, часто образующие крупные месторождения. Значительная часть запасов руд марганца, меди, ванадия и других металлов имеет осадочное происхождение.
Еще большее количество металлов выпадает в рассеянном состоянии, осаждаясь с распространенными соединениями. Например, быстрое разрушение комплексных железоорганических соединений в щелочной морской воде и энергичное осаждение образовавшихся сгустков гидроксидов железа сопровождаются сорбционным захватом скандия, кобальта, никеля, меди, ванадия и др.
При осаждении фосфатов накапливается другой комплекс рассеянных элементов.
Таким образом, периферийная зона Мировою океана служит глобальной геохимической ловушкой, задерживающей большую часть вещества, сносимого с континентов. Тем не менее, значительные массы рассеянных элементов проходят этот фильтр и поступают в открытый океан.
Проблема геохимии океана рассмотрена в монографии В.Коржа (1991). Для выяснения влияния океана на некоторые биогеохимические процессы, протекающие на суше, необходимо отметить следующее. Геохимическая структура состава океанических и континентальных вод принципиально различается. Если в речных водах преобладающая часть рассеянных элементов сосредоточена в материале взвесей, то в океане возрастает удельное значение растворенных форм. Количество форм элементов в составе взвесей в океанической воде в сотни и тысячи раз меньше их растворимых форм. Даже такие не склонные к нахождению в растворе элементы, как свинец, скандий, иттрий, цирконий, титан, хром, присутствуют в океане преимущественно в растворенном состоянии.
Кроме того, состав Мирового океана формируется под воздействием не только речного стока, но и поступлений из недр Земли в результате вулканической деятельности и процессов формирования океанической коры в тектонически активных зонах дна.
Сопоставление состава континентальных и океанических вод также выявляет их различие. В речной воде в тысячи раз меньше хлора, брома, натрия, в сотни раз — бора, сульфатной серы, магния, калия, в десятки — стронция, кальция, лития, рубидия, фтора, иода. В то же время, в речных водах в десятки раз больше марганца, иттрия, свинца, тория, значительно больше кремния, титана, цинка, меди. Следовательно, при поступлении речных вод в Мировой океан происходит существенная перегруппировка растворимых масс рассеянных элементов. Это наглядно представлено на графиках (рис. 4.1). Столь сильное различие в составе воды океана и суши в значительной мере обусловливает неодинаковую концентрацию химических элементов в живом веществе океана и суши, отмеченную в гл. 2.
Современный состав Мирового океана является итогом длительной истории. Как показано в подразд. 4.1, основную массу солей морской воды составляют хлориды и сульфаты натрия, магния, кальция и калия. Такое соотношение катионогенных и анионогенных химических элементов с позиций геохимии парадоксально. Первые содержатся в земной коре в количестве нескольких процентов каждый, вторые — в сто раз меньше (кларк хлора- 1,7×10-2
%, кларк серы - 4,7×10-2
%).
Так как катионы и анионы находятся в морской воде в эквивалентных количествах, то они не могли поступать из одного источника, в частности за счет выщелачивания из земной коры континентов. Расчеты показывают, что из того количества хлора, который в настоящее время имеется в океане в форме ионов, всего лишь 1 — 2 %
могли быть извлечены из земной коры. Следовательно, катионы и анионы морской воды имеют разное происхождение. Помимо упомянутых хлора и серы к анионогенным элементам океана относятся азот, бром, иод, бор, мышьяк, селен, некоторые металлы, в частности ртуть. Есть все основания предполагать, что поступление основной массы этих элементов связано с дегазацией вещества мантии Земли.
Соотношение масс гидросферы и земной коры близко к соотношению паров воды и силикатного расплава при излиянии базальтов. Очевидно, выплавление первичной земной коры базальтового состава сопровождалось выносом паров воды, из которых после конденсации был образован древний океан. Одновременно в газообразной форме выносились перечисленные выше анионогенные элементы. В дальнейшем в результате выветривания и почвообразования, при нарастающем воздействии биогеохимических процессов происходило выщелачивание катионогенных элементов из земной коры и в океане постепенно установилось существующее ныне равновесие анионов и катионов.
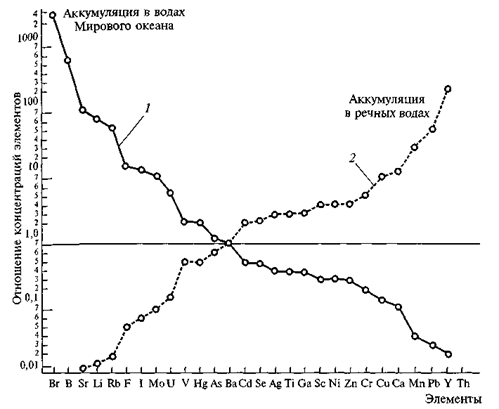
Рис. 4.1. Соотношение средних концентраций рассеянных химических элементов в океанических и речных водах:
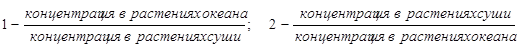
Литература
1. Биогеохимия океана / Под ред А.С. Монина, А.П. Лисицина. — М Наука, 1983. - 368 с.
2. Вернадский В.И. Живое вещество в химии моря // Избр. соч.: В 5 т. — М.: Изд-во АН СССР, 1960. — Т. 5. — С. 160-183.
3. Виноградов А.П. Введение в геохимию океана. — М.: Наука, 1967 — 213с.
4. Гордеев В.В. Речной сток в океан и черты его геохимии. — М.: Наука 1983. -160с.
5. Корж В.Д. Геохимия элементного состава гидросферы. — М.: Недра 1991. -243 с.
[1]
В этот объем входит собственно полный речной сток (39×103
км3
/год), сток ледников Антарктиды и Гренландии (3×103
км3
/год) и подземный сток суши помимо речного (2×103
км3
/год).
|