Министерство Образования и Науки РФ
Казанский Государственный Технологический
Университет
Кафедра Общей Химической Технологии
КУРСОВАЯ РАБОТА
по курсу: Технология химических производств
на тему:
Производство нитробензола
Казань 2010
Содержание
Задание
1. Теоретическая часть
Технологическая схема производства нитробензола
2. Практическая часть
Материальный баланс процесса.
Технологические и технико-экономические показатели процесса
3. Реклама
Список литературы
Задание:
1. Составить и описать технологическую схему производства нитробензола
2. Составить материальный баланс процесса
3. Рассчитать технологические и технико-экономические показатели
4. Реклама
В основу расчета принять следующие реакции
C6
H6
+HNO3
→C6
H5
NO2
+H2
O
C6
H5
NO2
+HNO3
→C6
H4
(NO2
)2
+H2
O
Исходные данные:
Производительность установки ,т/сут:
1. по нитробензолу
2. по динитробензолу
|
25
10
|
Конверсия бензола %
Концентрация бензола % масс
|
44
99.2
|
Состав нитрующей смеси % масс
1. азотная кислота
2. серная кислота
3. вода
|
21
58.6
20.4
|
| Массовое соотношение бензол-нитрирующая смесь |
1 : 4.3 |
| Потери бензола % масс |
3 |
1. Теоретическая часть
Технологическая схема производства нитробензола
Нитробензол (темп, пл, +5,7°, темп. кип. 210,9°) представляет собой нерастворимую в воде желтоватую жидкость с запахом горького миндаля; ядовит, как все нитросоединения.
Впервые нитрование бензола было осуществлено Митчерлихом. В промышленности оно было начато в 1847 г.
Нитрующую смесь для нитрования бензола до нитробензола составляли с таким расчетом, чтобы количество азотной кислоты лишь немного превышало теоретическое, а серную кислоту берут в таком количестве чтобы к концу процесса нитрования в отработанной кислоте содержалось около 70%
Нитрование проводится при 40°. Повышение температуры способствует образованию динитробензола.
Процесс нитрования можно проводить по периодической, и по непрерывной схеме.
При периодической процесс начинают с наполнения нитратора бензолом затем включают печку, подогревают бензол до 40 — 45° и постепенновводят нитрующую смесь, регулируя поступление и охлаждение нитратора водой таким образом, чтобы поддерживать температуру процесса около 40°.
Закончив приливание нитрующей смеси, прекращают охлаждение и дают температуре подняться до 50°. При низкой температуре содержимое нитратора «выдерживают» около 1 часа, втечение этого времени реакция нитрования почти полностью заканчивается; остается всего около 1% непрореагировавшего бензола. После выдержки содержимое нитратора сливают или передавливают в сифонную трубку в отстойник-сепаратор, представляющий собой цилиндрический аппарат с коническим дном и мешалкой. В отстойнике продукты нитрования разделяются на два слоя: верхний — нитрообензольный и нижний — кислотный. Из отстойника отработанная кислота, содержащая 70—72% H2
SO4
, небольшое количество окисленных продуктов, окислов азота и растворенного и эмульгированного бензола, поступает в сборник. Сырой нитробензол промывают в отстойнике несколько раз холодной водой, а затем раствором соды.
Реклама

Начиная с 30-х годов XX века, нитробензол на крупных установках стали получать непрерывным методом. В процессах непрерывного нитрирования бензола применяются нитраторы различных систем. Простотой, надежностью конструкции отличается нитратор с вертикальной циркуляцией реакционной массы (рисунок 2).
Такой нитратор представляет собой чугунный, или выполненный кислотоупорной стали котел с змеевиками и быстроходной пропеллерной мешалкой, помещенной внутри направляющего вертикального стального цилиндра. Бензол и нитрующая смесь непрерывно поступают через трубки в центральную часть нитратора смешиваются с его содержимым, скользят .снизу вверх, омывая змеевики, а затем сверху вниз через направляющий цилиндр. Избыток реакционной смеси непрерывно отводится из штуцера в верхней части нитратора.
Рисунок 1. Типовая схема процесса получения нитросоединений
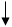 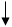
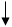 Нитрирующая смесь Нитрирующая смесь
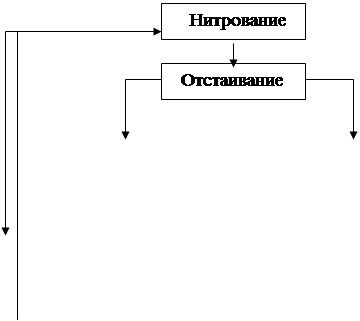
отработанная Кислый
кислота нитропродукт
 Исходное Промытая Исходное Промытая
  вещество и отработ. вещество и отработ.
нитропродукт кислота
На денитрацию
и концентрирование  вода вода
раствор
Nа2
СО3
Промывные воды
Рисунок 2. Нитратор непрерывного действия.
Для доведения реакции нитробензола до конца выходящую из нитратора реакционную смесь будут дополнительно выдерживать в цилиндрическом резервуаре с мешалкой (дозреватель). Остальные процессы отстаивание и промывка сырого нитробензола — также легко осуществляются по непрерывкой схеме.
2. Практическая часть
Материальный баланс процесса
| ПРИХОД |
РАСХОД |
| Кг/ч |
Кмоль/ч |
Кг/ч |
Кмоль/ч |
С6
Н6
HNО3
Н2
SO4
Н2
О(пр)
С6
Н5
NО2
С6
Н4
(NО2
)2
Н2
О(1)
Н2
О(2)
Примесь бензола
|
1547.94
1397.79
3900.5
1357.85
-
-
-
-
12.48
|
19.85
22.19
39.78
75.42
-
-
-
-
-
|
840.84+46.44потери
708.12
3900.5
1357.85
736.63
416.67
152.46
44.64
12.48
|
10.78+0.6потери
11.24
39.78
Реклама

75.42
5.99
2.48
8.47
2.48
|
| Σ = 8216.56 |
Σ = 8216.63 |
Mr(C6
H6
)=12*6+6=78 кг/кмоль
Mr(HNО3
)=1+14+16*3=63 кг/кмоль
Mr(Н2
SO4
)=32.06+2+16*4=98.06 кг/кмоль
Mr(С6
Н5
NО2
)=12*6+5+14+16*2=123 кг/кмоль
Mr(С6
Н4
(NО2
)2
)=12*6+4+14*2+16*4=168 кг/кмоль
Mr(Н2
О)=18 кг/кмоль
1. Производительность установки по нитробензолу:
mвсего
(С6
Н5
NО2
) = 25т/сут = 25 * 1000/24 = 1041.67 кг/ч
wвсего
(С6
Н5
NО2
) = 1041.67/123 = 8.47 кмоль/ч
2. Количество прореагировавшего бензола, исходя из уравнения реакции:
wпрор
(C6
H6
) = w(С6
Н5
NО2
) = 8.47 кмоль/ч
mпрор
(C6
H6
) = 8.47 * 78 = 660.66 кг/ч
3. Учитывая конверсию, всего чистого бензола было:
660.66 – 44 %
х – 100 %
х= mчист
(C6
H6
) = 660.66 * 100/44 = 1501.5 кг/ч
4. Учитывая потери 3% масс, всего чистого бензола вступило в реакцию:
1501.5 – 97 %
х – 100 %
х = mчист всего
(C6
H6
) = 1501.5 * 100/97 = 1547.94 кг
wчист всего
(C6
H6
) = 1547.94/78 = 19.85 кмоль/ч
mпотерь
(C6
H6
) = 1547.94 – 1501.5 = 46.44 кг
wпотерь
(C6
H6
) = 46.44/78 = 0.6 кмоь/ч
5. Учитывая концентрацию бензола 99.2 % масс, технического бензола, вступившего в реакцию:
1547.94 – 99.2 %
х – 100%
х = mтех
(C6
H6
) = 1547.94 * 100/99.2 = 1560,42 кг
mпримеси
(C6
H6
) = 1560.42 – 1547.94 = 12.48 кг/ч
6. Массовое соотношение бензол – нитрирующая смесь 1: 4,3
на 1 кг бензола берется 43 кг нитрирующей смеси, масса нитрирующей смеси:
mсмесь
= mчист всего
(C6
H6
) * 4.3 = 1547.94 * 4.3 = 6656.14 кг
7. Состав нитрирующей смеси:
- азотная кислота:
6656/14 – 100 %
х – 21 %
х = m(HNО3
) = 6656.14 * 21/100 = 1397.79 кг
w(HNО3
) = 1397.79/63 = 22.19 кмоль/ч
- серная кислота
m(Н2
SO4
) = 6656.14 * 58.6/100 = 3900.5 кг/ч
w(Н2
SO4
) = 3900.5/98.06 = 39.78 кмоль/ч
- вода
m(Н2
О) = 6656.14 * 20.4/100 = 1357.85 кг/ч
w(Н2
О) = 1357.85/18 = 75.42 кмоль/ч
8. Количество воды из первой реакции:
w(Н2
О)(1) = w(С6
Н5
NО2
) =8.47 кмоль/ч
m(Н2
О)(1) = 8.47 * 18 = 152,46 кг/ч
9. Не прореагировавшего бензола:
mнепр
= mчист
(C6
H6
) – mпрор
(C6
H6
) = 840.84 кг/ч
wнепр
(C6
H6
) = 840.84/78 10.78 кмоль/ч
10. Производительность по динитробензолу:
10т/сут = 10 * 1000/24 = 416.67 кг/ч
w(С6
Н4
(NО2
)2
) = 416.67/168 = 2.48 кмоль/ч
11. Количество нитробензола пошедшего на реакцию:
mвсего
(С6
Н5
NО2
) = w(С6
Н4
(NО2
)2
) = 2.48 кмоль/ч
mпрор
(С6
Н5
NО2
) = 2.48 * 123 = 305.04 кг
12. Количество оставшегося нитробензола:
mвсего
(С6
Н5
NО2
) – mпрор
(С6
Н5
NО2
) = 1041.67 – 305.04 = 736.63 кг
wост
(С6
Н5
NО2
) 736.63/123 = 5.99 кмоль/ч
13. Количество HNО3
прошедшего на обе реакции:
wо
(HNО3
) = w1
(HNО3
) + w2
(HNО3
)
w1
(HNО3
) = wвс
(С6
Н5
NО2
) = 8.47 кмоль/ч
w2
(HNО3
) = w(С6
Н4
(NО2
)2
) = 2.48 кмоь/ч
wо
(HNО3
) = 10.95 кмоль/ч
не прореагировавший
wост
(HNО3
) = wост
(HNО3
) - wо
(HNО3
) = 22.19 – 10.95 = 11.24 кмоль/ч
mост
(HNО3
) = 11.24 * 65 = 708.12 кг/ч
14. Масса и количество воды, полученной во второй реакции:
w(Н2
О)(2) = w(С6
Н4
(NО2
)2
) = 2.48 кмоль/ч
m(Н2
О)(2) = 2.48 *18 = 44.64 кг/ч
Технологические и технико-экономические показатели
процесса
1. Пропускная способность установки: 8216,56 кг/ч
2. Конверсия или степень превращения бензола =
=M(C6
H6
) подано – M(C6
H6
) непрореагировало / M(C6
H6
) подано = 1547.94-(840.84+46.44) * 1547ю94 = 0.49 %
3. Теоретические расходные коэффициенты:
по С6
Н6
:
sт
С
6
Н
6
= Mr(C6
H6
) / Mr(C6
Н5
NO2
) = 78 / 123 = 0,63 кг/кг;
поНNО3
:
sт
Н
N
О
3
:= Mr(НNО3
) / Mr(C6
Н5
NO2
) = 63/ 123 = 0,51 кг/кг.
4. Фактические расходные коэффициенты:
по С6
Н6
:
sф
С6Н6
= m(C6
H6
)техн
/ m(C6
Н5
NO2
) = 1547.94+12.48 / 736.63 = 2.12 кг/кг;
sф
Н
N
О3
= m(НNО3
)техн
/ m(C6
Н5
NO2
) =1397.79+3900.5+1357.85 / 736.63 = 9.03 кг/кг.
Выход на поданное сырье C6
Н5
NO2
:
1) Фактический выход:
QФ
= m(C6
Н5
NO2
) = 736.63 кг;
2) Теоретический выход:
Mr(С6
Н6
) ¾Mr(C6
Н5
NO2
), 78 ¾ 123,
m(С6
Н6
) ¾QТ
; 1547.94 ¾QТ
;
QТ
= (1547.94 * 123) / 78 = 2440.98 кг;
Выход C6
Н5
NO2
по бензолу:
bС6Н6
= QФ
/ QТ
* 100%= 736.63 / 2440.98 * 100% = 30.18%
5. Выход на превращенное сырье:
Mr(С6
Н6
) ¾Mr(C6
Н5
NO2
), 78 ¾ 123,
m(С6
Н6
) ¾QТ
; 660.66 ¾QТ
;
Qт
' = 660.66 * 123/78 = 1041.81 кг
β' C
6Н6
= QФ
/ QТ
* 100 % = 736.63/1041.81 *100% = 70.71 %
3. Реклама
Оптовая фирма химического сырья предлагает организацию оптовых поставок нитробензола в качестве сырья для производства анилина и селективного растворителя при очистке нефтяных смазочных масел.
Крупным химическим предприятиям
специальные скидки!!!
Заказывая нитробензол у нас вы экономите на стоимости сырья и снижаете себестоимость своей продукции!!!
Обращаться по адресу: г. Казань
ул. Магистральная 76. ООО «Нитробензолхим»
тел. 256-67-89.
Список литературы:
1. Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза. Изд. 2-е, пер. М., «Химия», 1975, 736 с.
2. Юкельсон И.И. Технология основного органического синтеза. М.: «Химия», 2008, 846 с.
3. Общая химическая технология /Под ред. А.Г. Амелина. М.: «Химия», 2007, 400 с.
4. Расчеты химико-технологических процессов /Под ред. И.П. Мухленова. Л.:Химия, 2009, 300 с.
5. С.И. Вольфкович Общая химическая технология. М.: Государственное научно-техническое издательство химической литературы. 2009, 633с.
|