Контрольная работа
по химии
вариант № 5
2009
Полиоксиэтиленовые цепи как гидрофильные части многих ПАВ и полимеров
Все свойства простых и сложных систем ионогенных ПАВ определяются электростатическими взаимодействиями. Свойства неионных ПАВ контролируются совершенно другими, а именно гидрофильными взаимодействиями. Наиболее важную группу неионных ПАВ составляют ПАВ с олиго группами в качестве полярных "головок". Если обозначить оксиэтиленовую группу символом Е, то простое неионное ПАВ с алкильной липофильной цепью можно сокращенно записать как Cm
Ew
. Гидрофобная часть молекул может быть более сложной, многие НПАВ содержат ароматические группы.
Для типичных ионных ПАВ, как и для многих других ПАВ, объем полярной группы намного меньше объема неполярной части молекулы. Однако это не так в случае полиоксиэтиленовых ПАВ, поскольку объемы обеих частей молекулы близки. Более того, обычно полярная часть молекулы больше неполярной. В связи с этим уместно и полезно рассматривать неионогенное ПАВ как короткий блок-сополимер AB. Самым ярким свойством неионных ПАВ является температурная зависимость их физико-химических свойств. Иногда это осложняет практическое использование НПАВ, но в то же время может быть и преимуществом, поскольку появляется возможность создавать системы, свойства которых управляются температурой. Главная проблема здесь состоит в понимании и контроле специфических температурно-зависимых взаимодействий между полярным растворителем и полиоксиэтиленовыми цепями НПАВ. Такие взаимодействия присущи не только НПАВ, они важны также для полимеров, содержащих оксиэтиленовые группы. Таким образом, вполне логично рассматривать оксиэтилированные ПАВ и полимеры в одном контексте.
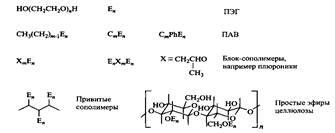
Некоторые оксиэтилированные полимеры и НПАВ
Использующиеся для различных нужд ПАВ редко бывают химически гомогенными. Все типы ПАВ характеризуются широким распределением неполярных частей молекул: различаются по длине алкильные цепи, варьируется степень их ненасыщенности и т.д. Негомогенность технических ПАВ по составу определяется исходным сырьем, используемым для синтеза ПАВ. Но это обычно мало влияет на анализ физико-химических данных и моделирование систем. Что касается неионогенных ПАВ, то дополнительным источником значительной гетерогенности являются полярные группы.
Реклама

Таким образом, неионные ПАВ, которые находят широкое практическое использование, необходимо рассматривать как смеси поверхностно-активных веществ. Конечно, существуют хорошо охарактеризованные индивидуальные неионогенные ПАВ, но они очень дороги. Их значение для проведения научных работ и для развития наших знаний трудно переоценить. Далее мы будем в основном анализировать результаты, полученные при исследовании таких индивидуальных ПАВ.
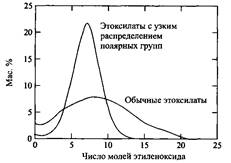
Обычные оксиэтилированные НПАВ характеризуются намного более широким распределением по размеру полярных групп по сравнению с недавно разработанными этоксилатами с узким распределением по полярным группам.
Температурная зависимость KKM и размеров мицелл оксиэтилированных ПАВ
Критическая концентрация неионных полиоксиэтилированных ПАВ типа Cm
En
сильно зависит от числа атомов углерода в неполярной цепи и в меньшей степени от числа оксиэтиленовых групп, слабо повышаясь при увеличении длины полярной цепи. Зависимость логарифма KKM от числа атомов углерода в алкильной цепи выражается прямой, наклон которой значительно больше, чем для ионных ПАВ. Увеличение алкильной цепи на одну метиленовую группу приводит к уменьшению KKM в три раза, а не в два. Свойства неионогенных ПАВ четко коррелируют с растворимостью углеводородов в воде, что слабее выражено в случае ионных ПАВ вследствие противодействующего электростатического эффекта, который тем заметнее, чем ниже ККМ. Температурные зависимости KKM неионных ПАВ отличаются от соответствующих зависимостей для ионных ПАВ по двум признакам: зависимости более ярко выражены и обычно наблюдается монотонное снижение KKM с увеличением температуры, а не увеличение KKM при более высоких температурах.
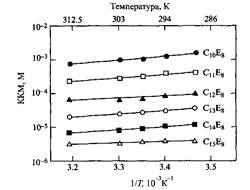
Логарифмические зависимости KKM от обратной температуры для ряда НПАВ, содержащих по восемь оксиэтиленовых групп в молекуле. Число атомов углерода в алкильной цепи изменяется сверху вниз следующим образом: 10, 11, 12, 13, 14 и 15.
Мицеллы неионных ПАВ характеризуются толстым межфазным слоем, составленным полярными группами, а не резким переходом от углеводородного мицеллярного ядра к окружающей воде, что характерно для ионных ПАВ. Именно изменение межмолекулярных взаимодействий в полярном слое отвечает за специфическое температурное поведение неионных ПАВ.
Сферическая мицелла типична для НПАВ с длинными полиоксиэтиленовыми цепями, особенно при низких температурах и концентрациях. Как и мицеллы ионных ПАВ, мицеллы неионных ПАВ могут расти, но при совсем других условиях. Так, зависимость размера мицелл НПАВ от температуры противоположна зависимости, характерной для ионных ПАВ.
Реклама

Важнейшие свойства неионных ПАВ иллюстрирует рис., где приведены зависимости гидродинамических радиусов мицелл от температуры для относительно разбавленных растворов трех НПАВ. Наблюдается незначительное или умеренное увеличение размера мицелл вплоть до высоких температур. Если НПАВ содержит более длинные оксиэтиленовые цепи, рост мицелл с температурой вообще замедляется. Для НПАВ с короткой оксиэтиленовой цепью, например С12Е5, характерен резкий рост мицелл с увеличением температуры.
В целом можно сделать следующие выводы о влиянии различных факторов на изменение размера мицелл НПАВ.

Схематическое изображение мицеллы НПАВ
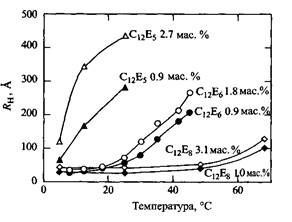
Для НПАВ с небольшими полярными группами размер мицелл увеличивается ростом температуры, эта зависимость существенно слабее для НПАВ с более крупными полярными группами. Размер мицелл характеризуется гидродинамическим радиусом
1. Увеличение размера мицелл в первую очередь контролируется длиной оксиэтиленовой цепи, причем чем короче цепь, тем более ярко выражена склонность мицелл к росту под влиянием и температуры, и концентрации НПАВ.
2. Росту мицелл ПАВ любых типов способствует увеличение длины алкильной цепи. Например, для ПАВ с 16 атомами углерода в алкильной цепи сильнее проявляется склонность к росту мицелл, чем для ПАВ с 12 атомами углерода в алкильной цепи.
3. Присутствие других растворенных веществ влияет на размер мицелл в случае НПАВ не так, как на ионные ПАВ. Электролиты с высаливающим эффектом инициируют увеличение размера мицелл, тогда как электролиты с всаливающим эффектом ингибируют рост мицелл. Ионные ПАВ замедляют рост мицелл, даже совсем небольшие добавки могут полностью ингибировать увеличение размеров мицелл.
Исследование влияния температуры на поведение НПАВ с помощью фазовых диаграмм
Фазовые диаграммы систем НПАВ - вода во многом аналогичны фазовым диаграммам ионных ПАВ, причем НПАВ с более длинными оксиэтиленовыми цепями подобны ионным ПАВ с одной углеводородной цепью, а с более короткими оксиэтиленовыми цепями - ионным ПАВ с двумя углеводородными цепями. Тем не менее ясно, что системы имеют принципиальные различия. Рассмотрим в качестве примера фазовую диаграмму НПАВ с водой. При низких температурах при возрастании концентрации НПАВ наблюдается следующая последовательностью фаз: мицеллярная, прямая гексагональная, биконтинуальная кубическая, ламелярная и твердая фаза ПАВ. В мицеллярной фазе наблюдается сильный рост мицелл с увеличением и температуры, и концентрации. Главное отличие от фазовой диаграммы ионного ПАВ состоит в том, что в случае НПАВ фаза с высоким содержанием воды при повышении температуры разделяется на две жидкие фазы. А при дальнейшем повышении температуры происходит образование новой жидкой фазы. Области устойчивости ламелярной фазы и обращенной мицеллярной фазы при повышении температуры заметно расширяются за счет неустойчивости прямых фаз.

Фазовая диаграмма системы неионное ПАВ - вода в зависимости от логарифма объемной доли НПАВ. При нагревании мицеллярного раствора происходит фазовый переход с разделением на два изотропных раствора. Граница двухфазной области называется нижней кривой растворимости, координаты минимума этой кривой - критические температура Tc
, и состав
Если сравнить фазовое поведение ряда НПАВ с одинаковой алкильной цепью, но с окиэтиленовыми цепями различной длины, то обнаружится резкое изменение свойств систем. На фазовых диаграммах НПАВ с длинными оксиэтиленовыми цепями присутствуют следующие фазы: мицеллярная, кубическая, образованная дискретными мицеллами, и прямая гексагональная фаза. Укорочение оксиэтиленовой цепи сопровождается усилением склонности мицелл к росту, в результате перечисленные фазы постепенно исчезают. Вместо них устойчивыми становятся другие фазы: ламелярная и фаза раствора, обогащенного НПАВ, а при повышении температуры образуется также губчатая фаза. Например, при смешении НПАВ Q2E3 с водой мицеллы не возникают, а сразу образуются две фазы: ламелярная фаза и очень разбавленный раствор. Эта ситуация напоминает фазовое поведение лецитина. Наряду с ламелярной фазой в таких системах устойчива обращенная мицеллярная фаза, которая узким каналом протягивается к обогащенной водой части фазовой диаграммы.
L3
или губчатая фаза
Впервые эта фаза была открыта при исследовании фазовых диаграмм системы СюЕб и была названа "аномальной", поскольку обнаружение при повышенной температуре второй мицеллярной области было совершенно неожиданным. В настоящее время хорошо известно, что эта фаза относится к биконтинуальному типу, в котором бислойные пленки ПАВ связаны между собой на макроскопических расстояниях. Бислойные пленки обеспечивают нулевую или небольшую среднюю кривизну поверхностям, разделяющим каналы воды.
Губчатая фаза в основном характерна для неионных ПАВ и изучена главным образом для них. Однако в последние годы стало понятно, что такую фазу могут образовать ПАВ любых классов при оптимальном балансе гидрофобной и гидрофильной частей молекул. Для ионных ПАВ образование губчатой фазы обычно инициируется добавлением электролита.
Влияние температуры на последовательность возникновения самоассоциированных структур
На основе анализа множества фазовых диаграмм легко выводится последовательность фазовых структур, образующихся при повышении температуры. Эта последовательность такова: сферические мицеллы, дискретная кубическая фаза, удлиненные мицеллы, гексагональная фаза, ламелярная фаза, биконтинуальная кубическая фаза, губчатая фаза и обращенные мицеллы. Некоторые структуры приведены на рис. Отметим, что повышение температуры и увеличение длины оксиэтиленовой цепи оказывают противоположные эффекты на последовательность образования фаз. Кроме того, для каждого определенного ПАВ в области доступных температур характерно образование лишь нескольких структур.
Информативность концепций критического параметра упаковки и спонтанной кривизны
Рассмотрим концепции критического параметра упаковки и спонтанной кривизны для описания принципов самоорганизации ПАВ. Безразмерный критический параметр упаковки или число ПАВ определяется объемом гидрофобной части молекулы ПАВ, деленным на произведение площади полярной группы и длины вытянутой молекулы ПАВ. Спонтанная кривизна пленки ПАВ считается положительной, если она искривлена в сторону гидрофобного домена.
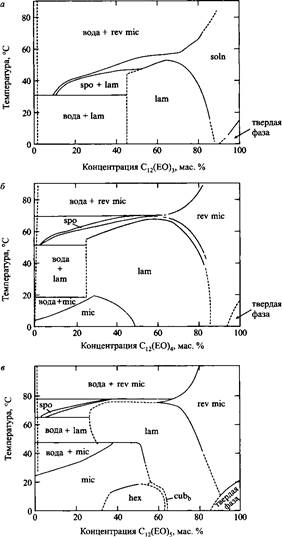
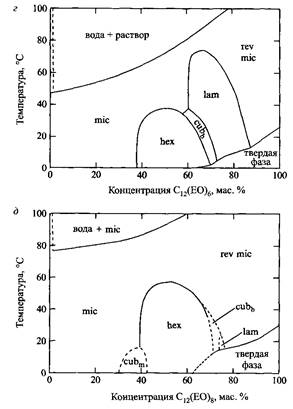
Упрощенные фазовые диаграммы систем НПАВ - вода для НПАВ с 12 атомами углерода в алкильной цепи и различным числом оксиэтиленовых групп. Обозначения mic, revmic и spo относятся к фазам изотропных растворов, ahex, lam, cubm
и cubb соответственно обозначают гексагональную, ламелярную и дискретную и биконтинуальную кубические жидкокристаллические фазы.
Последовательность образующихся самоорганизованных структур свидетельствует о том, что число НПАВ постепенно увеличивается с ростом температуры. Это можно объяснить только уменьшением площади полярной группы при увеличении температуры. Таким образом, полярные группы более плотно упаковываются на поверхности агрегата при повышенных температурах. Это согласуется с уменьшением гидратации полярных групп при увеличении температуры. Аналогичным образом уменьшается с ростом температуры и спонтанная кривизна.
Так как необычные температурные зависимости специфичны для всего класса неионных оксиэтилированных ПАВ, постараемся разобраться в механизме, ответственном за это. С увеличением температуры уменьшается взаимодействие между
оксиэтиленовыми группами и молекулами воды
изменяется от положительной до отрицательной. При некоторой промежуточной температуре спонтанная кривизна становится равной нулю; в этом состоянии НПАВ считается "сбалансированным". Такое изменение спонтанной кривизны с температурой свидетельствует о том, что вода является хорошим растворителем для полярных групп НПАВ при низких температурах, но взаимодействие оксиэтиленовых групп с водой становится невыгодным при повышении температуры
Для фазовых диаграмм оксиэтилированных ПАВ и полимеров характерна кривая растворимости с нижней критической точкой. Отсюда вытекает, что на эффективное взаимодействие между молекулами растворенного вещества сильно влияет температура, и с ростом температуры отталкивание сменяется притяжением. Это, в свою очередь, может отражать изменения взаимодействий между молекулами растворенного вещества, растворенного вещества и растворителя, молекулами растворителя или комбинацию таких изменений. Экспериментально подтверждены все изменения, однако до сих пор у исследователей нет согласия относительно эффекта, контролирующего состояние системы. Механизм, связанный с взаимодействиями вода - вода, который отражает температурное изменение структуры воды вблизи оксиэтиленовых групп, маловероятен, поскольку обсуждаемые явления наблюдаются и в других растворителях. Предложена также другая модель, отражающая изменение сетки водородных связей между молекулами воды и эфирными атомами кислорода НПАВ. Представляет интерес проанализировать модель, основанную на влиянии температуры на изменение конформации молекул НПАВ, поскольку эта модель имеет большую предсказательную силу.
Полиоксиэтиленовая цепь может существовать во множестве конформационных состояний, характеризующихся различными энергиями. Конформация оксиэтиленовой группы относительно связи C-C и конформация относительно связи C-O обладает наименьшей энергией среди всех конформеров. Такая низкоэнергетическая конформация характеризуется большим дипольным моментом и будет доминировать при низких температурах. В то же время у такой конформации небольшой статистический вес. С увеличением температуры будут реализовываться другие конформации с большим статистическим весом. Эти конформации имеют меньший или нулевой дипольный момент, как, например, анти-анти-анти-конформация.
Следовательно, в результате конформационных изменений полиоксиэтиленовые цепи при повышении температуры будут постепенно становиться менее полярными, что приведет к невыгодности их взаимодействия с молекулами воды и, как следствие, к их дегидратации. В то же время взаимодействие оксиэтиленовых групп между собой станет энергетически более выгодным, что приведет к более плотной упаковке полярных групп в агрегатах молекул НПАВ, а также к более ярко выраженной склонности к фазовому разделению в более концентрированной фазе. Последовательность самоорганизованных структур при повышении температуры также является логическим следствием уменьшения полярности окси-этильных групп. Подобные представления, как будет показано ниже, применимы для объяснения многих экспериментальных данных, например для объяснения увеличения адсорбции гомополимеров, сополимеров и ПАВ при повышении температуры вследствие ухудшения свойств растворителя. Независимо от принятой модели, температурные эффекты неионогенных полимеров и НПАВ удобнее всего анализировать на основе представлений о том, что вода является хорошим растворителем для оксиэтиленовых групп при низких температурах и плохим растворителем при высоких. Таким образом, мы можем эффективно регулировать взаимодействие растворенное вещество - растворитель при изменении температуры.
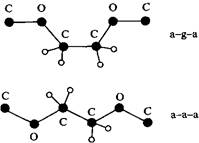
Конформации оксиэтиленовых групп, различающиеся по стабильности и полярности. Верхняя низкоэнергетическая анти-гош-анти-конформация более полярна, чем показанная внизу анти-анти-анти-конформация.
|