Химический элемент №
42, Мо
ЗАДАНИЕ.
4.
Электронное строение атома.
4.1. Составьте электронную формулу данного элемента.
4.2. Дайте объяснение физического смысла всех индексов у данного химического элемента в системеД.И. Менделеева (порядковый номер, номер периода, номер группы, принадлежность к группе «А» или «Б»). Определите возможность «Эффекта провала электрона».
4.3. Выделите валентные подуровни в электронной формуле атома химического элемента, определитепринадлежность химического элемента к типу s-, p-, d-, f-элементов.
4.4. Напишите наборы квантовых чисел для всех валентных электронов.
4.5. Определите принадлежность химического элемента к металлам или неметаллам, спрогнозируйтевеличины степени окисления.
4.6. Распределите валентные электроны атома химического элемента по энергетическим ячейкам в соответствии с принципом наименьшей энергии и правилом Гунда.
4.7. Прогнозируйте тип гибридизация валентных атомных орбиталей при образовании бинарных соединений (фторидов, хлоридов и др.).
5. Соединение данного химического элемента с неметаллами.
5.1. С водородом.
5.2. С галогенами.
5.3. С серой.
5.4. С азотом.
5.5. С углеродом.
5.6. С кислородом.
6. Оксиды и гидроксиды данного химического элемента.
6.1. Запишите ряд оксидов данного химического элемента (прогноз по электронной формуле иковалентности).
6.2. Прогнозируйте характер оксидов (основной, кислотный, амфотерный) по величине Э.О. и правилухимических свойств ряда оксидов.
6.3. Запишите соответствующие гидроксиды (основания и кислоты). Определите принадлежность к сильнымили слабым электролитам.
6.4. Составьте уравнения реакций, подтверждающих характер гидроксидов о молекулярном и ионном виде.
6.5. Напишите уравнения реакций электролитической диссоциации гидроксидов.
7. Может ли данный химический элемент образовывать комплексные соединения? Если да, то, какие
(кислоты, основания, соли)? Приведите примеры.
8. Напишите уравнения реакций гидролиза соли
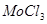 по 1-ой стадии в молекулярном и ионном виде с учетом
всех равновесий. Рассчитайте рН среды при гидролизе этой соли (0
,01
моль/л). Как усилить гидролиз?
по 1-ой стадии в молекулярном и ионном виде с учетом
всех равновесий. Рассчитайте рН среды при гидролизе этой соли (0
,01
моль/л). Как усилить гидролиз?
9. Окислительно-восстановительные реакции.
9.1. Дайте оценку восстановительных свойств Мо и окислительно-восстановительных свойств его ионов в зависимости от его рН среды (используйте справочные характеристики).
Реклама

9.2. Составьте уравнения 3-х окислительно-восстановительных реакций ( с использованием вещества содержащего ионы данного металла) при рН>7, рН=7, рН<7. 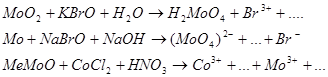
Предварительно рассчитайте Е0
химической реакции, используя метод электронно-ионного баланса.
10. Электрохимические свойства металла.
10.1. прогнозируйте отношение данного металла в компактном виде к атмосфере сухого воздуха (при комнатной температуре и нагревании), к влаге (без аэрации и при аэрации), к неокислительным и окислительным кислотам (на холоду и при нагревании), к растворам и расплавам щелочей.
10.2. Опишите процесс измерения стандартного электродного потенциала данного металла Cu и дайте термодинамический расчет этой величины.
10.3. Составьте и опишите схему гальванического элемента из металлического электрода данного металла и электродной системы С, 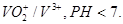
10.4. Опишите процесс электрохимической коррозии при контакте металла и изделия из Mg во влажной среде (Без аэрации и при аэрации). PH=10
10.5. Опишите процесс электролиза с учетом перенапряжения.
Электролит – раствор 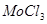 PH= 4, 5
PH= 4, 5
Электроды: катод – Сu,
анод – Zn.
11. Применение.
РЕШЕНИЕ
4.
Электронное строение атома.
4.1. Составьте электронную формулу данного элемента.
Порядковый номер элемента в периодической системе химических элементов Д. И. Менделеева равен 42. Это значит, в молекуле молибдена будет 42 электрона.
Электронная формула молибдена будет такова: 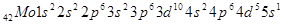
Составим также его электронно – графическую формулу:
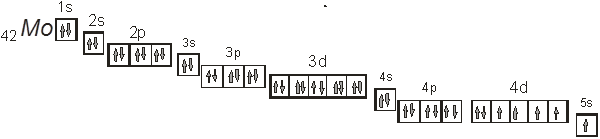
На рисунке выше приведена электронно – графическая формула молибдена.
4.2. Дайте объяснение физического смысла всех индексов у данного химического элемента в системеД.И. Менделеева (порядковый номер, номер периода, номер группы, принадлежность к группе «А» или «Б»). Определите возможность «Эффекта провала электрона».
Порядковый номер химического элемента в периодической системе химических элементов – 42. у молибдена на электронных уровнях находится 42 электрона, а в ядре должно находится также 42 протона.
Молибден расположен в периодической системе химических элементов в пятом периоде, это значит, что у него будет пять электронных слоев с расположенными на них электронами. Главное квантовое число внешнего электронного уровня равно 5.
Молибден расположен в шестой группе, побочной подгруппе. Молибден относят к элементам подгруппы хрома , в которую входят хром, молибден и вольфрам, которые обладают похожими свойствами. У него будет на электронных уровнях один s-электрон и 5 d-электронов на пред внешнем уровне.
Реклама

В состав ядра атома изотопа молибдена-96 входят 42 протона (p) и 54 нейтрона (n): 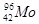 , где массовое число и порядковый номер элемента (число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний – заряд ядра. Количество нейтронов ядра элементов определяют по массовому числу элемента за вычетом количества протонов. , где массовое число и порядковый номер элемента (число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний – заряд ядра. Количество нейтронов ядра элементов определяют по массовому числу элемента за вычетом количества протонов.
Таким образом, в состав атома молибдена входят ядро, состоящее из 42 протонов, 54 нейтронов и электронное облако, представленное 42 электронами.
Вследствие устойчивости d5
-конфигурации энергетически оказывается более выгодным переход одного из ns-электронов в (n-1) d-состояние. Поэтому молибден, как и хром в s-состоянии внешнего уровня имеют по одному, а в предпоследнем слое по 13 электронов. Таким образом, имеет место «проскок» электрона:
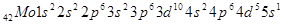
Проскок электрона можно объяснить с точки зрения квантово-механических представлений повышенной энергетической стабильностью конфигурации: 4d5
.
4.3. Выделите валентные подуровни в электронной формуле атома химического элемента, определитепринадлежность химического элемента к типу s-, p-, d-, f-элементов.
Покажем расположение валентных электронов в атоме молибдена. Как видно из электронной формулы моилбден относится к d-элементам, поскольку у него заполняется 4d-подуровень.
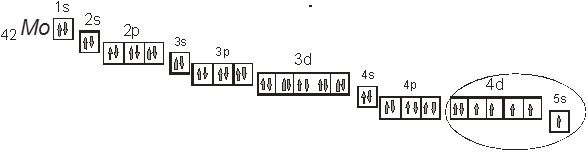
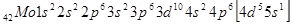
На приведенном рисунке эллипсом выделено расположение валентных электронов в атоме молибдена. Как видно в создании химической связи будут брать участие электроны как 5s- так и 4d-подуровня.
4.4. Напишите наборы квантовых чисел для всех валентных электронов.
У атома молибдена будет разное количество валентных электронов приразных степе5нях окисления, до шести включительно. Запишем наборы квантовых чисел для этих электронов.
Сначала рассмотрим электроны на 5s-подуровне. Главное квантовое число равно 5 и химический элемент находится в 5 периоде периодической системы химических элементов. Поскольку в молибдена валентный электрон расположен на s-подуровне то его орбитальное квантовое число имеет значение равное 0. Поскольку электрон будет только один, то его спин будет иметь значение ms
= +1/2. Поскольку ml
= 0 то у элемента не будет других подуровней кроме s-подуровня.
Набор квантовых чисел будут иметь вид:
n
= 5; l
= 0; ml
= 0; ms
= +1/2.
Рассмотрим электроны на 4d-подуровне. Их количество равно 5. главное квантовое число п
равно 4, 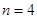 . Орбитальное квантовое число равно . Орбитальное квантовое число равно 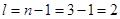 и орбитальное квантовое число может принимать значения равные 0, 1, 2, 3. магнитное квантовое число может принимать значения в пределах от +l
до -l
.
Поскольку и орбитальное квантовое число может принимать значения равные 0, 1, 2, 3. магнитное квантовое число может принимать значения в пределах от +l
до -l
.
Поскольку  то ml
= -2, -1, 0, +1, +2. Согласно правила Хунда суммарный спин должен быть максимальным, поэтому мы можем считать, что спин электронов будет равен +1/2. то ml
= -2, -1, 0, +1, +2. Согласно правила Хунда суммарный спин должен быть максимальным, поэтому мы можем считать, что спин электронов будет равен +1/2.
Запишем наборы квантовых чисел для электронов.
n
= 5; l
= 2; ml
= -2 ; ms
= +1/2.
n
= 5; l
= 2; ml
= -1 ; ms
= +1/2.
n
= 5; l
= 2; ml
= 0 ; ms
= +1/2.
n
= 5; l
= 2; ml
= +1 ; ms
= +1/2.
n
= 5; l
= 2; ml
= +2 ; ms
= +1/2.
4.5. Определите принадлежность химического элемента к металлам или неметаллам, спрогнозируйтевеличины степени окисления.
Поскольку молибден расположен в шестой группе периодической системы, и не в главной подгруппе, а в побочной, то он относится к металлам. В химических реакциях он будет проявлять металлические свойства. Для металлов более приемлема отдача электронов. Поэтому молибден может отдавать максимум шесть электронов с 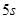 - подуровня и с 4d-подуровня. Поэтому молибден будет проявлять степень окисления +2, +3, +4, +5, +6. соединения с этими степенями окисления обладают разной стойкостью, наиболее стойкими будут соединения с степенью окисления равной +6. - подуровня и с 4d-подуровня. Поэтому молибден будет проявлять степень окисления +2, +3, +4, +5, +6. соединения с этими степенями окисления обладают разной стойкостью, наиболее стойкими будут соединения с степенью окисления равной +6.
4.6. Распределите валентные электроны атома химического элемента по энергетическим ячейкам в соответствии с принципом наименьшей энергии и правилом Гунда.
В соответствии с принципом наименьшей энергии валентный электрон атома молибдена расположен на 5s-подуровне, поскольку он располагает меньшей энергией чем любой другой подуровень. Правило Хунда гласит, что устойчивому состоянию атома отвечает такое расположение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. Поэтому электроны на 4d-подуровне расположатся таким образом как на приведенном рисунке:

4.7. Прогнозируйте тип гибридизация валентных атомных орбиталей при образовании бинарных соединений (фторидов, хлоридов и др.).
Рассмотрим получение 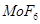 : :

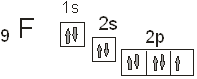
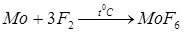
Ион молибдена (VI) имеет на 4d-уровне 0 электронов, а также свободные 4s и 4p-орбитали. Образование связи можно рассматривать как донорно-акцепторный процесс (ион молибдена – акцептор, гидрид-, фторид- и хлорид-ионы – доноры). В бинарных соединениях образуется 6 связей Мо-Э, для каждой из них атом молибдена предоставляет одну свободную орбиталь. Тип гибридизации sd5
(форма октаэдрическая). Следует отметить, что для молибдена характерны разные соединения с галогеними, поэтому и гибридизация в этих соединениях будет разной. Например в трифториде MоF3
для создания химической святи использовано только три электрона: sd2
(форма тетраэдрическая).
5. Соединение данного химического элемента с неметаллами.
Рассмотрим реакции взаимодействия молибдена с неметаллами. Молибден довольно активно реагирует с неметаллами (кремнием, бором, галогенами, серой и т. п.), учитывая то что молибден имеет несколько степеней окисления то получается в таких реакциях несколько продуктов.
5.1. С водородом.
Молибден не реагирует с водородом с получением химических соединений. Имеет место только физическое растворение водорода в молибдене с образованием нестойких связей. Растворимость водорода в молибдене растет с повышением температуры до 0,5 см3
в 100 граммах металла.
5.2. С галогенами.
С молибденом фтор образует летучие фториды. Хлор и бром ре6агируют с ним при температуре красного каления. Йод реагирует с молибденом очень медленно. В присутствии влаги реакция с галогенами ускоряется и она становится возможной даже на холоду.
Молибден образует гексафторид MoF6
, пентафторид MoF5
, тетрафторид MOF4
и трифторид MоF3
; гексахлорид МоС16
, пентахлорид МоС15
, тетрахлорид МоС13
, трихлорид МоС13
и комплексный псевдодихлорид [Мо6
(С1)8
]С14
; тетрабромид МоВг4
, трибромид МоВг3
и комплексный псевдодибромид [Мо6
Вг8
]Вг4
. С иодом достоверно известно лишь два соединения – дииодид МоІ2
и трииодид МоІ3
. Помимо этих соединений, известен ряд оксигалогенидов и несколько менее достоверных соединений.
Фториды.
Гексафторид получается действием сухого фтора в смеси с азотом на металл (в платиновой трубке), трифторида брома на металл при 250°, безводного HF на MoCl5
:
2МоС15
+ 12HF = 2MoF6
+ 10НС1 + Н2
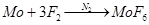 (50) (50)
Гексафторид конденсируется при -70°С в виде белых кристаллов и отгоняется под вакуумом при 40°. Плавится при 17,5°С и кипит при 35°С. Молекула имеет октаэдрическую структуру с атомом металла в центре октаэдра и атомами фтора в вершинах его. Устойчив в сухом воздухе, хлоре, двуокиси серы. Гидролизуется:
MoF6
+ 4Н2
О = Н2
МоО4
+ 6HF (51)
Образует с фторидами щелочных металлов комплексные соли типа Me2
(MоF8
).
Трифторид молибдена получается нагреванием МоВг3
в токе безводного HF. При нормальных условиях твердый. При нагревании во влажном воздухе диссоциирует:
4MoF3
+ 6Н2
О + 3O2
= 4МоО3
+ 12HF (52)
В сухом воздухе устойчив до 800°. При действии водорода восстанавливается до металла. Водой на холоду медленно разлагается.
У молибдена (VI) выделены два оксифторида -MoOF4
и MоO2
F2
. Это твердые, белые, тяжелые кристаллические вещества, получающиеся фторированием молибдена в присутствии кислорода или обменными реакциями МоО3
с фторидами.
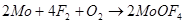
Хлориды
MoCl6
термически очень неустойчив и чувствителен к малейшим следам влаги. Получен недавно длительным кипячением тионилхлорида с МоО3
.МоС15
получается хлорированием молибдена в отсутствие воды и воздуха при 600 – 750°С. Кристаллизуется в виде темно-зеленых тригональных бипирамид. Темпеартура плавления 194°С, температура кипения 238°С. Плотность МоС15
2,9275. Он растворяется в безводном эфире,спиртах, углеводородах, кетонах, альдегидах, сероуглероде, аминах с образованием комплексов. При нагревании в отсутствии кислорода разлагается:
МоС15
= МоС13
+ С12
Водород при 900°С восстанавливает его до металла:
2МоС15
+ 5Н2
→ 10НС1 + 2Мо
Восстанавливать можно над накаленной металлической нитью в токе его пара в смеси с водородом. В этом случае на нити осаждается плотный слой молибдена, но при 250° образуется трихлорид:
МоС15
+ Н2
→ МоСІ3
+ 2НС1
При нагревании МоС15
в сухом воздухе образуется оксихлорид МоО2
С12
. При нагревании во влажном воздухе МоС15
полностью разлагается, образуя окси- и гидроксихлориды. В воде полностью гидролизируется с большим выделением тепла.
Тетрахлорид молибдена получается хлорированием МоО3
смесью СІ2
и ССІ4
. При нагревании без доступа влаги и кислорода МоСІ4
диспропорционирует на MoCl5
и MoCl3
. При нагревании в присутствии влаги и кислорода образуются оксихлориды и гидроксихлориды. С рядом веществ, в том числе органических, тетрахлорид образует продукты присоединения.
Трихлорид МоС13
получается в виде твердого красного вещества частичным восстановлением MoCl5
водородом при 250°, а также пропусканием смеси паров МоС15
с инертным газом над молибденом.
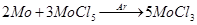
Трихлорид разлагается, не плавясь. Сублимирует в токе инертного газа. Устойчив в сухом воздухе при нормальной температуре, а при нагревании переходит в оксихлориды. При
нагревании в инертном газе разлагается наМоСІ4
и комплексные нелетучие хлориды. Водой и водными растворами щелочей разлагается соответственно при нагревании и на холоду. С аммиаком образует комплексы. Окислителями окисляется до Н2
МоО4
. В соляной кислоте не растворяется. Растворяется в солянокислых растворах МоО3
, образуя комплексы.
Бромиды.
Все бромиды получаются действием Вг2
на Мо в среде СО. Так, черно-зеленые иглы тетрабромида получаются около 600°С при атмосферном давлении, тетрабромид – преимущественно при 350 – 500°С. При более низком давлении или несколько более высокой температуре получается смесь бромидов, в том числе комплексных. Известны также красно-оранжевые кристаллы диоксибромида МоО2
Вг2
и желтые игольчатые кристаллы бромомолибденовой кислоты H3
(MoO3
Br3
).
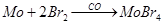
Йодиды.
Достоверно известен лишь диодид молибдена Mol2
. Получается он взаимодействием паров йода с металлом выше 1000°С:
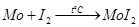
5.3. С серой.
Сера не реагирует с молибденом до температуры 400 - 450°С, при более высокой температуре образуется дисульфид молибдена MoS2
:
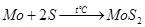
Сероводород реагирует с молибденом при высокой температуре, образуя MoS2
.В парах хлоридов серы образуются сульфохлориды молибдена.
Непрямыми методами были получены сульфиды молибдена MoS3
, Mo2
S5
, Mo2
S3
. Первые два диссоциируют при температурах выше 400°С.
Помимо этих простых сульфидов известны также и полисульфид Mo(S2
)2
,тиомолибдаты Ме2
MoS4
. Высший сульфид MoS3
образуется при пропускании сероводорода через растворы молибдатов щелочных металлов:
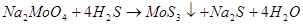
Дисульфид молибдена 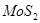 – важнейший минерал молибдена. Он образуется в земной коре в высотемпературных условиях. Имеет сложную слоистую гексагональную кристаллическую решетку. Пары воды окисляют – важнейший минерал молибдена. Он образуется в земной коре в высотемпературных условиях. Имеет сложную слоистую гексагональную кристаллическую решетку. Пары воды окисляют 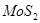 при красном калении. Кислоты-окислители разлагают при красном калении. Кислоты-окислители разлагают 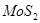 , переводя его в , переводя его в 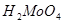 , неокисляющие кислоты не действуют на него. Сульфиды щелочных металлов и щелочи разлагают , неокисляющие кислоты не действуют на него. Сульфиды щелочных металлов и щелочи разлагают 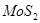 при сплавлении. при сплавлении.
5.4. С азотом.
С азотом молибден не реагирует, азот незначительно растворяется в молибдене. Нитриды молибдена добыты другим путем.
При температуре 400 – 745°С порошок молибдена реагирует с аммиаком с получением нитридов молибдена: МоN, Mo2
N, β-фаза, содержащая 28% азота. Во всех трех фазах были установлены определенные кристаллические структуры. В вакууме при нагревании они легко разлагаются.
Нитриды, как и карбид Мо2
С и бориды, являются соединениями, в которых валентные соотношения не сохранены. Мо3
Nи Mo2
Nотносятся к так называемым фазам внедрения, в которых атом неметалла внедряется между атомами металла, при этом сохраняется кристаллическая структура последнего. МоNимеет более сложную структуру (8, ст. 181) и не может быть отнесен к фазам внедрения.
5.5. С углеродом.
Молибден с углеродом образует два карбида: Мо2
С и МоС. Это очень твердые, тяжелые, тугоплавкие металлоподобные соединения. Они близки по свойствам к фазам внедрения, имеющим металлический характер (проводимость, внешний вид и т. п.), обусловливаемый особенностями их атомно-кристаллической структуры. Мо2
С образуется при 2400°С. Это темно-серый порошок, получаемый обычно науглероживанием в твердой фазе смеси молибденового порошка и сажи при 1400- 1500°С. Может быть также получен науглероживанием накаленной молибденовой проволоки из газовой фазы или взаимодействием МоО3
с СО и углеводородами. МоС плавится при 2650°. Карбиды молибдена, благодаря своей твердости и тугоплавкости, играют важную роль в инструментальной и других отраслях современной техники.
Молибден образует с окисью углерода под высоким давлением гексакарбонил Мо(СО)6
. Он диссоциирует при 150°С. Это ромбоэдрические белые кристаллы, возгоняющиеся при пониженном давлении и комнатной температуре, растворимые в эфире и бензоле. С органическими основаниями образует комплексы. При разложении Мо(СО)6
в зависимости от условий образуется металлическое зеркало или порошок из мелких гранул молибдена.
5.6. С кислородом.
Литой и плотно спеченный слиток молибдена при нормальной и несколько повышенной температуре стоек к действию кислорода и воздуха. При нагревании до темно-красного каления поверхность металла быстро тускнеет и при 600°С молибден загорается выделяя дым – возгон МоО3
. Налет окисла легко разрушается и при длительном нагревании происходит полное сгорание металла до МоО3
.
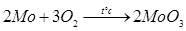
Молибденовый порошок окисляется при более низкой температуре, а мелкодисперсный порошок молибдена может самовозгораться на воздухе или в токе кислорода.
6. Оксиды и гидроксиды данного химического элемента.
6.1. Запишите ряд оксидов данного химического элемента (прогноз по электронной формуле иковалентности).
Для молибдена были идентифицированы оксиды с химической формулой МоО3
, и МоО2
. Ковалентность молибдена в оксидах равна 3 и 2. Кроме того, получены оксиды промежуточного между МоО3
и МоО2
состава: Мо8
О23
, Мо9
О26
,Мо4
О11
, Мо17
О47
. характер связи в оксидах в основном ионный, частично ковалентный.
МоО и Мо2
О3
не выделены в свободном состоянии, хотя ранее в литературе и упоминалось о их выделении (8, ст. 162). Рентгенографически идентифицирована фаза, содержащая кислород в количестве, соответствующему составу Мо3
О. оксид МоО2
более туго плавок и термодинамически устойчив чем оксид МоО3
.
6.2. Прогнозируйте характер оксидов (основной, кислотный, амфотерный) по величине Э.О. и правилухимических свойств ряда оксидов.
Поскольку молибден относится к металлам, то его оксиды должны проявлять основные свойства. Но оксидыМоО3
, и МоО2
проявляют не основные свойства, а кислотные. Они дают ряд соединений общей формулой Н2
МоО4
и Н2
МоО3
. основные свойства проявляет оксид Мо2
О3
.
По химическим свойствам оксид проявляет тем более основные свойства, чем больше разница электроотрицательностей между элементом и кислородом. Электронегативность молибдена по Полингу равна 1,8 а кислорода 3,5. как видно разница электроотрицательностей элементов равна 3,5 – 1,8 = 1,7.
Основные свойства оксидов молибдена можно подтвердить их взаимодействием с растворами кислот и щелочей.
6.3. Запишите соответствующие гидроксиды (основания и кислоты). Определите принадлежность к сильнымили слабым электролитам.
МоО3
, и МоО2
, как наиболее стойким оксидам молибдена, запишем формулы гидратов.
МоО3
характерен гидрат состава Н2
МоО4
и Н2
МоО4
×Н2
О. Н2
МоО4
- белые мелкие кристаллы гексагональной формы. Дигидрат Н2
МоО4
×Н2
О образуется при стоянии подкисленного раствора молибдатов в течении нескольких недель, а также при внесении затравки Н2
МоО4
×Н2
О в сильно подкисленный раствор парамолибдата аммония. Н2
МоО4
- молибденовая кислота, кислота средней силы, например, она более сильная чем угольная кислота и вытесняет ее из ее солей:
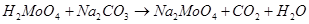
Гидраты окислов с валентностью металла между VI и IVполучены в виде соединений МоО(ОН)3
и Мо(ОН)5
. сила этих электролитов очень слабая, они малорастворимы в воде.
МоО2
характерен гидрат состава Н2
МоО3
, который в свободном состоянии не выделен, выделен только в растворах, также получены его соединения состава Ме2
МоО3
.слабый электролит.
Также при действии аммиака на растворы молибдатов получен Мо(ОН)3
- аморфный порошок черного цвета, не растворим в воде и растворах щелочей, легко растворяется в минеральных кислотах и при отсутствии окислителей дает ионы Мо+3
.
6.4. Составьте уравнения реакций, подтверждающих характер гидроксидов о молекулярном и ионном виде.
Рассмотрим свойства Н2
МоО4
Молибденовая кислота реагирует при повышенной температуре с оксидами, гидроксидами, карбонатами щелочных и щелочноземельных металлов давая соответствующие молибдаты.
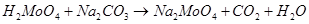
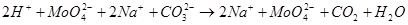
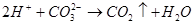
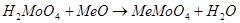
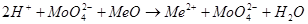
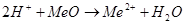
Состояние молибденовой кислоты в растворах зависит от кислотности и разбавлености последних. При большом разбавлении (<10-4
моль/л, РН>6,5) молибденовая кислота находится в растворе в виде простых молекул. В более концентрированных растворах и при РН меньше шести: РН<6 происходит полимеризация молекул. Степень сложности образованных комплексов также зависит от температуры.
Рассмотрим свойства Мо(ОН)3
Сухой Мо(ОН)3
- это аморфный порошок, не растворимый в воде и растворах щелочей. Он проявляет основные свойства. Легко растворяется в растворах минеральных кислот, при этом образуются соли Мо3+
.
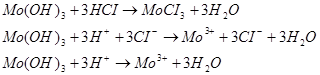
6.5. Напишите уравнения реакций электролитической диссоциации гидроксидов.

7. Может ли данный химический элемент образовывать комплексные соединения? Если да, то, какие
(кислоты, основания, соли)? Приведите примеры.
8. Напишите уравнения реакций гидролиза соли
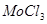 по 1-ой стадии в молекулярном и ионном виде с учетом
всех равновесий. Рассчитайте рН среды при гидролизе этой соли (0
,01
моль/л). Как усилить гидролиз?
по 1-ой стадии в молекулярном и ионном виде с учетом
всех равновесий. Рассчитайте рН среды при гидролизе этой соли (0
,01
моль/л). Как усилить гидролиз?
Гидролиз солей молибдена (IІI) протекает ступенчато, в основном, по первой ступени.
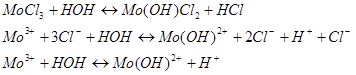
Как видно из записи уравнения гидролиза 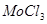 РН раствора будет кислым, поскольку будут синтезироваться ионы водорода.
РН раствора будет кислым, поскольку будут синтезироваться ионы водорода.
Для гидроксида молибдена 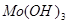 ПР =
ПР = 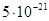 , поскольку он не растворим в воде. , поскольку он не растворим в воде.
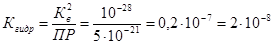
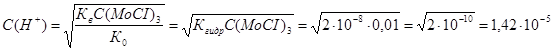
Тогда РН раствора при гидролизе будет равен: 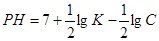 . Но мы нашли концентрацию ионов водорода в растворе, поэтому: . Но мы нашли концентрацию ионов водорода в растворе, поэтому: 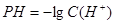 . .
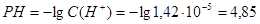
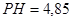
В аналитической практике часто приходится встречаться с гидролизом солей. Гидролиз может способствовать выполнению реакции, а иногда мешает проведению анализа. Имеются следующие способы подавления и усиления гидролиза солей.
1. Прибавление к раствору соли другого электролита, кислоты или основания.
Для усиления гидролиза солей (в т.ч. 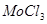 ) добавляют основания для связывания в процессе гидролиза ионов H+
:
) добавляют основания для связывания в процессе гидролиза ионов H+
:
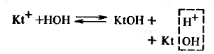
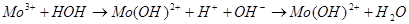
Равновесие реакции смещается в сторону гидролиза соли.
Для подавления гидролиза указанных солей к раствору добавляют кислоты, тогда:
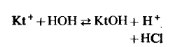
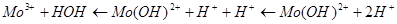
В такой ситуации увеличивается количество ионов H+
и реакция смещается в обратную сторону, т.е. уменьшается гидролиз соли.
Для изменения гидролиза можно прибавлять и другие ионы электролитов: HCO3
-
, HPO4
2-
, HSO4
-
. Для связывания OH-
ионов используют их способность образовывать комплексные ионы: [Co(OH)]+
, [Al(OH)]2+
, [Al(OH)2
]+
и др.
9. Окислительно-восстановительные реакции.
9.1. Дайте оценку восстановительных свойств Мо и окислительно-восстановительных свойств его ионов в зависимости от его рН среды (используйте справочные характеристики).
Мерой окислительно-восстановительной способности веществ служат их окислительно-восстановительные (электродные) потенциалы (φ0
). Чем больше алгебраическая величина стандартного окислительно-восстановительного потенциала данного атома или иона, тем больше его окислительные свойства, а чем меньше алгебраическое значение окислительно-восстановительного потенциала атома или иона, тем больше его восстановительные свойства.
9.2. Составьте уравнения 3-х окислительно-восстановительных реакций ( с использованием вещества содержащего ионы данного металла) при рН>7, рН=7, рН<7. 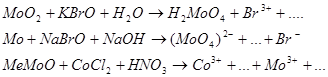
Предварительно рассчитайте Е0
химической реакции, используя метод электронно-ионного баланса.
10. Электрохимические свойства металла.
10.1. Прогнозируйте отношение данного металла в компактном виде к атмосфере сухого воздуха (при комнатной температуре и нагревании), к влаге (без аэрации и при аэрации), к неокислительным и окислительным кислотам (на холоду и при нагревании), к растворам и расплавам щелочей.
Литой и плотно спеченный молибден при комнатной и слегка повышенной температуре стоек против действия воздуха и кислорода. При нагревании до темно-красного каления поверхность металла быстро тускнеет и около 600°С молибден загорается, выделяя белый дым – возгон МоО3
. Налет окисла легко разрушается и при длительном нагревании происходит полное сгорание металла до МоО3
. Молибденовый порошок окисляется при еще более низкой температуре, а наиболее мелкий порошок способен самовозгораться на воздухе. При нагревании во влажной атмосфере, в среде восстановительного или инертного газа, не очищенных тщательно от кислорода и паров воды, наблюдается постепенное более или менее полное окисление металла по реакции:
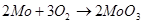
При нагревании молибдена в токе SO2
образуется смесь окислов и дисульфида молибдена, в токе НС1 – летучие хлориды (МоСІ3
) и оксихлориды молибдена.
В растворах, содержащих окислитель (кислород, HNO3
, НС1О3
и др.), молибден окисляется. Растворы при недостатке окислителя окрашиваются в синий цвет. Азотная кислота,одна и в смеси с соляной и серной – окисляети растворяет металл:
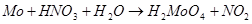
При избытке кислоты из бесцветного раствора выпадает белый или слегка желтоватый осадок молибденовой кислоты Н2
МоО4
. Концентрированная HNO3
задерживает растворение, создавая пассивирующую пленку окислов. Разбавленная НС1 довольно хорошо растворяет компактный металл: за 18 ч потеря массы 20-30%. В концентрированной НС1 растворение более медленное: за 18 ч при 110°С потеря массы 0,34%:
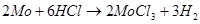
Фтористый водород и плавиковая кислота быстро действуют на молибден, переводя его во фториды. Разбавленная H2
SO4
(d=l,3 г/мл) слабо действует на молибден даже при 110°. Концентрированная H2
SO4
(
d
=
1,82 г/мл) на холоду действует слабо: за 18 ч потеря массы 0,24%. При 200 – 250°С растворение идет быстрее. Фосфорная и органические кислоты воздействуют на металл слабо, но в присутствии окислителей (в том числе воздуха) растворимость заметно увеличивается.
Растворы щелочей и аммиака действуют на молибден медленно, но их действие усиливается окислителями с повышением температуры. При растворении молибдена в щелочах получаем молибдаты щелочных метал лов, реакция будет ускоряться при использовании расплавов щелочей:
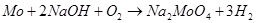
Молибден стоек к действию влаги без аэрации, при аэрации молибден будет окисляться при условии, что он находится в контакте с другим менее активным металлом и есть гальванический элемент. В таком гальваническом элементе будет окисляться более активный металл.
10.2. Опишите процесс измерения стандартного электродного потенциала данного металла Мо и дайте термодинамический расчет этой величины.
Для измерения величины стандартного электродного потенциала металлического электрода, данный электрод соединяют с водородным электродом проводником первого рода. При замыкании электрической цепи вследствие разности электродных потенциалов начнется движение электронов от электрода с меньшим потенциалом (обладающие избытком электронов) к электроду с большим потенциалом (обладающим меньшим количеством электронов). Так, если в качестве измеряемого электрода выступает молибден, то движение электронов будет направлено от платины к молибдену. Увеличение количества электронов на молибденовой пластине будет смещать равновесие в сторону выхода катионов молибдена из раствора, а следовательно на молибденовом электроде будет протекать процесс восстановления.
Мо3
+
+ 3e → Мо0
На водородном электроде молекулы Н2
отдают электроны и окисляются.
Н2
- 2е → 2Н+
Суммарную реакцию можно записать в виде:
2Мо3
+
+3Н2
→ 2Мо0
+ 2Н+
Принято считать электрод, на котором протекает процесс окисления – анодом, а на котором процесс восстановления – катодом. Зная величину ЭДС, измеренную в такой системе, можно легко вычислить потенциал электрода. Так как в рассматриваемом процессе анодом является водородный электрод, а φ0
(2H+
/H2
) = 0
- φА = ЭДС
Если потенциал измеряемого электрода больше водородного, то движение электронов направлено от платины к металлу и величина потенциала электрода будет положительной.
φ0
(Мо3+
/Мо0
) = -0,2 В
Мо3
+
+ 3e → Мо0
 Go
= nFEo Go
= nFEo
Тогда мы получим: 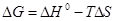 , поскольку для молибдена, как для простого вещества: , поскольку для молибдена, как для простого вещества:
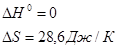
Для водорода:
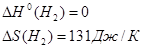
То тогда: 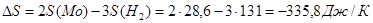
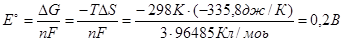
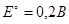
Мы рассчитали стандартный электродный потенциал для молибдена.
10.3. Составьте и опишите схему гальванического элемента из металлического электрода данного металла и электродной системы С, 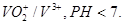
Гальванический элемент состоит из катода и анода. Одним из электродов в нашем случае будет молибденовый электрод, другим электродом будет инертный угольный электрод.
Запишем схему гальванического элемента.

Гальванический элемент состоит из молибденовой пластины опущенной в раствор соли, что содержит ионы V3+
и H+
. поскольку РН <7. Угольный электрод опущен в раствор, что содержит ионы 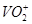 . Между электродами расположена диафрагма, которая пропускает ионы, но не дает смешиваться электродным растворам. Если электрическая цепь разделена, то в приэлектродных пространствах быстро наступает равновесие. . Между электродами расположена диафрагма, которая пропускает ионы, но не дает смешиваться электродным растворам. Если электрическая цепь разделена, то в приэлектродных пространствах быстро наступает равновесие.
Молибденовая пластинка в гальваническом элементе легко отдает свои катионы в раствор, тогда она будет окислятся.
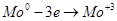
Каждый ион молибдена, переходя в раствор, оставляет на пластинке три электрона. Из-за этого пластинка получит отрицательный заряд. На угольном электроде будут проходить процессы восстановления:
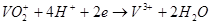
Если цепь замкнуть, то в гальваническом элементе возникнет электрический ток. Электроны из места, где плотность отрицательного заряда высока, будут переходить в место с меньшей плотностью отрицательного заряда.
В целом химическую реакцию, которая происходит в гальваническом элементе можно записать так: 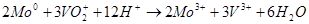 . В молекулярном виде уравнение будет иметь такой вид: . В молекулярном виде уравнение будет иметь такой вид: 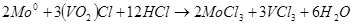 . .
Важной характеристикой любого гальванического элемента будет его ЭРС. Она равна: 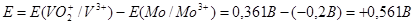 , если округлить полученное значение ЭРС, то мы получим: , если округлить полученное значение ЭРС, то мы получим: 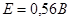 . При вычислении ЭРС мы не учитывали влияния концентрации ионов на величину потенциала, а приведенные значения точны только для ситуации, когда концентрации веществ равны нулю. Поэтому значение ЭРС в реальных гальванических элементах будет несколько другим. Также надо отметить, что чаще используется медно-цинковые гальванические элементы, которые более дешевы чем элементы с использованием молибдена . При вычислении ЭРС мы не учитывали влияния концентрации ионов на величину потенциала, а приведенные значения точны только для ситуации, когда концентрации веществ равны нулю. Поэтому значение ЭРС в реальных гальванических элементах будет несколько другим. Также надо отметить, что чаще используется медно-цинковые гальванические элементы, которые более дешевы чем элементы с использованием молибдена
10.4. Опишите процесс электрохимической коррозии при контакте металла и изделия из Mg во влажной среде (Без аэрации и при аэрации). PH=10
Очевидно, что образуется гальванический элемент. В полученном гальваническом элементе один из металлов, а именно более активный, будет окислятся, а на менее активном будет восстанавливаться ион ОН-
, или какой то другой ион.
Имеем короткозамкнутый элемент, где магний является анодом, а молибден – катодом. Как видно из условия РН раствора щелочной, РН=10.
В разбавленных щелочах цинк реагирует по уравнению:
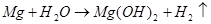 , поскольку в растворе есть большое количество ионов ОН-
то это будет несколько тормозить реакцию окисления магния, равновесие реакции сдвинется влево. , поскольку в растворе есть большое количество ионов ОН-
то это будет несколько тормозить реакцию окисления магния, равновесие реакции сдвинется влево.
Поскольку молибден находится в контакте с магнием и оба эти металла окружены раствором электролита, гальванический элемент оказывается «включенным». Магний в виде иона Mg2+
переходит в раствор щелочи, а оставшиеся от каждого атома два электрона перетекают на более электроположительный металл – молибден :
Mg = Mg2+
+ 2e
–
К молибденовому катоду подходят ионы водорода, принимают электроны и превращаются в атомы водорода, а затем и в молекулы водорода:
Н+
+ е-
= Н; 2Н = H2
Таким образом, потоки движения ионов разделены и при избытке щелочи процесс протекает до тех пор, пока не растворится весь магний. Мы рассмотрели процесс электрохимической коррозии при отсутствии поступления воздуха.
В присутствии воздуха в растворе протекают следующие реакции:
Mg + H2
O + 1/2O2
= Mg(OH)2
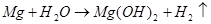
При наличии в растворе газообразного кислорода и невозможности протекания процесса коррозии с водородной деполяризацией основную роль деполяризатора исполняет кислород. Коррозионные процессы, у которых катодная деполяризация осуществляется растворенным в электролите кислородом, называют процессами коррозии металлов с кислородной деполяризацией. Это наиболее распространенный тип коррозии металла в воде.
Общая схема кислородной деполяризации сводится к восстановлению молекулярного кислорода до иона гидроокисла:
O2
+2H2
O + 4e-
= 4OH-
Суммарно на аноде будет проходить растворение магния, на катоде – выделение гидроксид-ионов. Процесс будет протекать до полного растворения магния и перехода его в гидроксид.
10.5. Опишите процесс электролиза с учетом перенапряжения.
Электролит – раствор  PH= 4, 5
PH= 4, 5
Электроды: катод – Сu,
анод – Zn.
В растворе хлорид молибдена будет диссоциировать на ионы согласно уравнения:
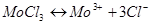
Рассмотрим процессы, которые будут происходить на аноде.
Анод цинковый. На цинковом аноде могут происходить несколько процесов:
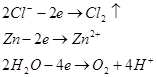
Запишем потенциалы прохождения указанных процессов:

Перенапряжение выделения кислорода на цинковом электроде при плотности тока 1мА/см2
равно 1,75 В. Это значит, что кислород в данной реакции выделятся не будет и на аноде возможны только две электрохимические реакции:
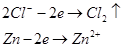
Как видно из значений электродных потенциалов на аноде будет происходить реакция окисления цинка: 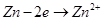 , потенциал которой будет ниже чем потенциал восстановления хлора. Мы будем иметь дело с электрорафинированием цинка. , потенциал которой будет ниже чем потенциал восстановления хлора. Мы будем иметь дело с электрорафинированием цинка.
Рассмотрим электродные процессы на катоде. Материал катода – медь, катод довольно инертен и не будет брать участия в электрохимических процессах. Конечно мы только допускаем это, медь содержит некоторые примеси, которые и будут брать участие в электродных реакциях, но мы считаем, что эти процессы не повлияют существенно на суммарную реакцию. На катоде также возможны несколько реакций, рассмотрим их.
РН среды равно 4,5, среда кислая. На меди при температуре 20ºС перенапряжение выделения водорода при плотности тока 1 А/см2
равно 1,2 В, а при плотности тока 1 мА/см2
всего лишь 0,6 В. За уравнением Нернста мы можем вычислить значение потенциала перенапряжения водорода при РН=4,5. Потенциал водородного электрода находится в линейной зависимости от РН среды.
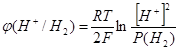
При давлении водорода 1 атмосфера 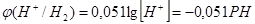 , и при РН=4,5 мы получим перенапряжение равное: , и при РН=4,5 мы получим перенапряжение равное: 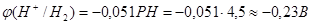
При плотности тока равной 1 А/см2
перенапряжение равно: 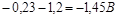 а при плотности тока 1 мА/см2 а при плотности тока 1 мА/см2
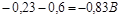 . .
Ионы же цинка восстанавливаются при потенциале равном - 0,763 В, ионы молибдена восстанавливаются при потенциале равном -0,2 В. Перенапряжением восстановления ионов цинка и молибдена на медном электроде можно пренебречь, поскольку оно довольно мало по значению. Из полученных расчетов видно что при малых плотностях тока на медном электроде возможны три конкурирующие реакции:
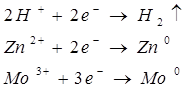
При плотности тока 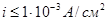 на катоде будет выделятся молибден по уравнению на катоде будет выделятся молибден по уравнению 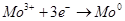 , поскольку потенциал восстановления молибдена будет равен , поскольку потенциал восстановления молибдена будет равен 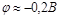 , что больше потенциала восстановления цинка и водорода в данном растворе. , что больше потенциала восстановления цинка и водорода в данном растворе.
При этих условиях потенциал восстановления водорода равен около 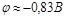 . При плотности тока равной 1 А/см2
перенапряжение равно: . При плотности тока равной 1 А/см2
перенапряжение равно: 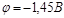 , при этих условиях мы можем вести выделение молибдена из раствора по уравнению: , при этих условиях мы можем вести выделение молибдена из раствора по уравнению: 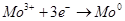 . Тогда водород на электродах выделяться не будет. Выделение молибдена из раствора будет происходить до тех пор пока не выделится он весь, или же его в растворе будет содержаться ничтожно мало. Тогда будет происходить восстановление цинка, потенциал восстановления которого равен - 0,76 В, тогда как потенциал выделения водорода выше – 0,83 В: . Тогда водород на электродах выделяться не будет. Выделение молибдена из раствора будет происходить до тех пор пока не выделится он весь, или же его в растворе будет содержаться ничтожно мало. Тогда будет происходить восстановление цинка, потенциал восстановления которого равен - 0,76 В, тогда как потенциал выделения водорода выше – 0,83 В: 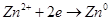 . По нашим данным выделение водорода не будет происходить, реакции восстановления металлов будут более энергетически выгодно. . По нашим данным выделение водорода не будет происходить, реакции восстановления металлов будут более энергетически выгодно.
При проведении электролиза надо учитывать повешение температуры, при повышении температуры на 1ºС перенапряжение уменьшается на 2 – 3 мВ. Оно также зависит от вида поверхности электрода и от наличия некоторых органических добавок в электролите.
11. Применение.
Молибден имеет большое значение в современной технике. Из всего его количества, потребляемого промышленностью, до 80% используется в черной металлургии для производства жаропрочных, жаростойких антикоррозионных, инструментальных, быстрорежущих, магнитных, конструкционных сталей, жаропрочных и жаростойких чугунов. Молибден повышает прочность сталей на холоду и содействует ее сохранению при высокой температуре, повышает жаростойкость сталей и чугуна, улучшает способность принимать закалку, 1 вес. ч. Мо
повышает прочность стали эквивалентно 2 - 2,5 вес. ч. вольфрама.
Молибден в стали входит в состав как свободных выделений карбидов, так и твердого раствора. Присадка его в сталь способствует созданию мелкозернистой структуры. Вследствие этих причин и повышается прочность стали на холоду, при повышенной температуре, кратковременной и длительной нагрузке. Молибден также повышает способность стали к цементации. В магнитных сталях и сплавах он увеличивает магнитную проницаемость. Придает жаропрочность и жаростойкость ряду сплавов на основе цветных металлов.
В жаропрочных сплавах с цветными металлами потребляется около 4 – 5% вырабатываемого молибдена. Также около 5 – 6,5 % Мо выпускают в виде проволоки, прутков, листа для электро- и радиотехнической промышленности и других назначений. Для реактивов, красок и других химикатов используется 4 – 5% Мо. Возрастает и его применение в сельском хозяйстве.
Молибден вводят в стали в виде сплава с железом - ферромолибдена. Молибдена в ферросплавах не менее 50%.
Проволока и прутки из чистого молибдена применяются для холоднокатаной арматуры, вводов, анодов радио- и электроламп, элементов сопротивления высокотемпературных печей с защитной атмосферой, высокотемпературных термопар. Листовой молибден применяется в машиностроении как жаропрочный материал, а в радиоэлектронике – для анодов мощных радиоламп, защитных экранов высокотемпературных электропечей и для других целей. Из молибденового порошка получают «псевдосплавы» (сплавы-смеси) с серебром для электротехнических контактов, карбид молибдена применяется в твердых сплавах, силицид молибдена MoSi2
– в жаростойких изделиях. Последний, как указывалось, применяется в элементах сопротивления электропечей, работающих до 1600°С без защитной атмосферы. Соединения молибдена применяются как катализаторы в органическом синтезе и как реактивы в аналитической химии (парамолибдат аммония и комплексные соединения молибдена), в производстве лаков и красок для шерсти и шелка. В сельском хозяйстве используются соединения молибдена в виде слабых растворов: он облегчает усвояемость растениями питательных веществ из почвы. Но в то же время большие дозы молибдена оказывают токсическое действие на растительные и животные организмы.
Из MoS2
готовят сухую смазку для деталей механизмов, работающих при повышенной температуре. Его смазывающее действие эффективнее, чем графита.
Молибденовые рудные концентраты перерабатывают на ферромолибден, молибдат кальция, МоО3
, парамолибдат аммония, MoS2
. Первые два – полуфабрикаты для производства молибденсодержащих сталей, парамолибдат аммония – полуфабрикат для производства чистых соединений молибдена и самого молибдена.
В последние годы значительно увеличился выпуск молибденовых концентратов в Канаде и Чили, которые в мире вышли в этой области соответственно на второе и третье места. Значительные залежи молибденовых руд есть в России, которая также производит довольно большие количества его как для собственной металлургической промышленности так и на экспорт. Товарная продукция молибдена в США выпускается в виде трехокиси, порошка молибдена, молибдатов аммония и натрия, ферромолибдена, сульфида молибдена MoS2
и др.
Список использованной литературы.
1. Глинка Н. Л. Общая химия. – Л.: Химия, 1988. – 702 с.
2. Полеес М. Э. Аналитическая химия. – М.: Медицина, 1981. – 286 с.
3. Крешков А. П., Ярославцев А. А. Курс аналитической химии. – М.: Химия, 1964. – 430 с.
4. Мороз А. С., Ковальова А. Г. Физическая и коллоидная химия. – Л. : Мир, 1994. – 278 с.
5. Физическая химия. Практическое и теоретическое руководство. Под ред. Б. П. Никольского, Л.: Химия, 1987. – 875 с.
6. Скуг Д., Уэст Д. Основы аналитической химии. В 2 т. Пер с англ. М.: Мир, 1979, - 438 с.
7. Бусев А. И. Аналитическая химия молибдена. М.: Издательство АН СССР, 1962, - 300с.
8. Химия и технология редких и рассеянных элементов. Ч.ІІІ. М.: Высшая школа, 1976, 320 с.
|