МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
Національний університет «Львівська політехніка»
Кафедра «Технології машинобудування»
Контрольна робота
Дисципліна: фізика металів
“ ВПЛИВ ВОДНЮ НА СТРУКТУРУ ТА ВЛАСТИВОСТІ СПЛАВІВ НА ОСНОВІ КРЕМНІЮ”
Зміст
Вступ
1 Мета роботи
2 Опис методики обладнання та проведення експериментів
3 Вибір об’єктів дослідження
4 Дослідження впливу водневої обробки на розрядні характеристики сплаву ZrCrNi
Висновки
Література
Вступ
Протягом останніх років у сучасному матеріалознавстві інтенсивно розвивається новий напрямок хіміко-термічної обробки конструкційних матеріалів, основою якого є використання водню як технологічного середовища, у якому проводять обробку. Найбільш перспективним об’єктом для застосування водневих технологій є новий клас функціональних матеріалів на основі гідридотвірних сплавів рідкісноземельних металів та цирконію– це постійні магніти, гетери та металогідридні електроди для нікель- металогідридних джерел живлення. При цьому основне завдання гідридного матеріалознавства полягає як у розробці нових металогідридних матеріалів, так і у створенні технологічних процесів покращення експлуатаційних характеристик вже широко апробованих металогідридів. Особливо це стосується сплавів і інтерметалідних сполук, які пропонуються для використання як металогідридні електроди.
На даний час найбільш широко для виготовлення металогідридних електродів застосовують сплави на основі сполуки LaNi5
. Однак, всебічна увага дослідників спрямована і на вивчення цирконієвих сплавів зі структурою фаз Лавеса, які володіють вищою розрядною ємністю, однак поступаються вказаним комерційним сплавам низькою швидкістю активації, тобто потребують проведення значної кількості циклів заряду-розряду для досягнення максимальної розрядної ємності. Це зумовлено тим, що розчинення непроникних для водню оксидних плівок, які формуються на електродному матеріалі в процесі його помелу, вимагає певного часу та енергетичних затрат. Крім того, активованість електродів можна підвищити за рахунок гомогенізації і зміни вихідного фазово-структурного стану.
Найбільш перспективним для цієї мети є розроблений у середині 80-х років минулого століття процес диспропорціонування – рекомбінації (ГДДР).
Реклама

Тому вияснення можливостей створення нового технологічного підходу до вирішення проблеми покращення активованості цирконієвих електродів є актуальною задачею гідридного матеріалознавства і складає предмет досліджень даної цієї роботи.
1
Мета роботи
1. Розробити методологічні підходи до вивчення процесу ГДДР в металогідридних матеріалах та визначення їх зарядно-розрядних характеристик.
2. Оптимізувати параметри механохімічного помелу сплавів на основі сполуки ZrCr2
.
3. Встановити особливості процесів ГДДР та Solid-ГДДР у сполуці ZrCr2
зі структурою фаз Лавеса двох типів MgZn2
(С14) та MgCu2
(С15).
4. Дослідити особливості процесу ГДДР у сполуці ZrCr2
при заміщенні хрому на нікель та цирконію на титан.
5. Встановити закономірності та фізичну природу фазових перетворень у сплавах системи Zr-Cr-Ni та їх вплив на зарядно-розрядні характеристики виготовлених з них металогідридних електродів.
6. Видати рекомендації щодо умов комплексної водневої обробки сплавів на основі сполуки ZrCr2
для покращення їх зарядно-розрядних характеристик.
Об’єкт дослідження. Фазові перетворення у цирконієвих сплавах зі структурою фаз Лавеса.
Предмет дослідження. Вплив водню на фазовий склад, структуру і зарядно-розрядні характеристики сплавів на основі сполуки ZrCr2
.
Методи дослідження. Диференціальний термічний аналіз (ДТА) для визначення температур фазових перетворень, метод термодесорбційної спектроскопії для дослідження процесів десорбції водню, рентгеноструктурний аналіз для встановлення фазового складу сплавів, металографічний аналіз та мікрорентгеноспектральний аналізи для вивчення структури і процентного вмісту елементів у фазах, метод гальваностатичного циклування для вивчення зарядно-розрядних характеристик.
2
Опис методики обладнання та проведення експериментів
Для отримання досліджуваних сплавів використовували метали наступної чистоти (масова частка основного компонента, %): Zr (99,5), Ti (99,5), Cr (99,99), Ni (99,9). Отриману шихту сплавляли в електродуговій печі на мідному водоохолоджуваному поді з використанням нерозпилюваного вольфрамового електроду у середовищі очищеного аргону за тиску 110-150 кПа. Маса зразка становила 1,5-3 г.
Термостабільність гідридів та процес ГДДР вивчали на розробленій та виготовленій у ФМІ НАН України комп’ютеризованій установці диференціального термічного аналізу (ДТА), яка дозволяє за виділенням (поглинанням) теплоти фіксувати процес утворення (розпаду) гідридних фаз та забезпечує можливість водневої обробки гідридотвірних матеріалів за тиску водню £10 МПа. Установка обладнана терморегулятором РИФ-101 і забезпечує нагрів з заданою швидкістю до температури 1000 °С. Джерелом водню у експериментах служив термосорбційний компресор ОМЕГА-10, виготовлений на основі гідриду сплаву LaNi5
. Крім того, ця установка дозволяє одночасно вести запис зміни тиску водню у робочій камері.
Реклама

Фазово-структурний аналіз сплавів проводили на дифрактометрі HZG-4A (Cu-Ka
випромінювання). Дифрактограми індексували за допомогою програми PowderCell 2.2, а для уточнення структур використовували розроблений у Львівському національному університеті імені Івана Франка пакет програм Crystal Structure Determination (CSD 4.04). Мікроструктурні дослідження та елементний аналіз складу досліджуваних зразків вивчали на растровому електронному мікроскопі JSM-840 (Японія) з системою мікроаналізаторів-спектрометрів “Analitik Link Systems” та “Ortec” (Англія).
Для дослідження зарядно-розрядних характеристик сплавів використовували металогідридні електроди, виготовлені з суміші порошку досліджуваного сплаву та високодисперсного нікелю (<1 мкм) у масовому співвідношенні 2:1. Суміш “сплав-нікель” отримували помелом у водні сплаву разом з порошком нікелю в однокамерному планетарному млині Pulverisette 6 (Fritsch, Німеччина). Плоскі електроди розмірами 36´12´1 мм формували шляхом пресування отриманої суміші на нікелеву сітку під навантаженням 7000 кг/см2
.
Зарядно-розрядні характеристики вивчали у двоелектродній комірці з позитивним нікелевим (Ni(OH)2
/NiOOH) електродом при 20 °С. Електроліт - 6М водний розчин гідроксиду калію (КОН). Металогідридні електроди активували шляхом повторення циклів заряду-розряду. Питому розрядну ємність Ср
обраховували за формулою:
Ср
=(Ір
´tр
)/m,
де Ір
- сила струму, мА; tр
- час розряду, год; m - маса сплаву, г.
3
Вибір об’єктів дослідження
Перш за все необхідно зазначити, що основним об’єктом дослідження був вибраний сплав ZrCrNi, який вже апробований як матеріал для виготовлення металогідридних електродів. Тому саме на цьому сплаві перевіряли можливості застосування водневої обробки. Однак, щоб зрозуміти процеси, які відбуваються за наводнення цього сплаву, на першій стадії досліджували вихідну сполуку ZrCr2
, як модельний об’єкт.
Згідно з даними рентгенофазового аналізу, зразки вихідних сплавів ZrCr2
та Zr1-x
Tix
Cr2
однофазні , мають гексагональну ґратку зі структурою типу MgZn2
(C14).
Встановлено, що ІМС ZrCr2
(С14) повністю розпадається після нагріву до 950 °С у водні при 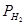 =5 МПа на гідрид цирконію та хром (табл. 1) за схемою =5 МПа на гідрид цирконію та хром (табл. 1) за схемою
ZrCr2
+ H2
®e-ZrHx
+ Cr.
Таблиця 1. Умови та фазовий склад продуктів взаємодії у системі
ZrCr2 (С14)-Н2
| Умови взаємодії |
Фазовий склад
(ст. тип)3
|
Параметри ґратки, нм |
| Режим |
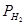 , MПa , MПa |
Tмакс
, °С |
t, год |
а |
с |
| Вихідний сплав |
ZrCr2
(C14) |
0,5104(1) |
0,8267(3) |
| ГД1
|
3 |
950 |
0 |
ZrCr2
Hx
(С14)
e-ZrHx
Cr
|
0,5402(2)
0,3525(4)
0,28838(7)
|
0,8849(5)
0,449(1)
-
|
| ДР2
|
вакуум |
940 |
0 |
ZrCr2
(С14) |
0,5094(1) |
0,8266(3) |
| ГД |
3 |
860 |
3 |
e-ZrHx
Cr
|
0,3495(2)
0,28820(4)
|
0,4488(3)
-
|
| ГД |
5 |
950 |
0 |
e-ZrHx
Cr
|
0,3500(2)
0,2880(1)
|
0,4457(4)
-
|
| ДР |
вакуум |
940 |
0 |
ZrCr2
(С15) |
0,7206(1) |
- |
Примітки: 1
ГД - гідрування-диспропорціонування; 2
ДР - десорбція-рекомбінація; 3
ст. тип - структурний тип.
При цьому на кривій ДТА зафіксовано два екзотермічні ефекти, пов’язані з утворенням гідриду вихідної фази при 20 °C та гідриду цирконію під час диспропорціонування при 875 °С. За 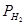 =3 МПа ІМС ZrCr2
(С14) частково розпадається: =3 МПа ІМС ZrCr2
(С14) частково розпадається:
ZrCr2
+ H2
® ZrCr2
Hx
+ e-ZrHx
+ Cr.
Витримка при 860 °С протягом 3 год завершується повним розпадом вихідної фази (табл. 1). ІМС ZrCr2
(С15) повністю розпадається (табл. 2) при 820 °С за 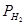 =3 МПа. Підвищення тиску водню до 5 МПа призводить до зниження температури диспропорціонування до 775 °С. =3 МПа. Підвищення тиску водню до 5 МПа призводить до зниження температури диспропорціонування до 775 °С.
Таблиця 2. Умови та фазовий склад продуктів взаємодії у системі
ZrCr2 (С15)-Н2
| Умови взаємодії |
Фазовий склад
(ст. тип)
|
Параметри ґратки, нм |
| Режим |
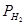 , MПa , MПa |
Tмакс
, °С |
а |
с |
| Вихідний сплав |
ZrCr2
(C15) |
0,7209(1) |
- |
| ГД |
3 |
950 |
e-ZrHx
Cr
|
0,3508(2)
0,28855(2)
|
0,4491(3)
-
|
| ДР |
вакуум |
950 |
ZrCr2
(С15)
Cr
d-ZrHx
- сліди
|
0,7209(1)
0,2885(1)
|
-
-
|
| ГД |
5 |
940 |
e-ZrHx
Cr
|
0,3497(1)
0,28856(8)
|
0,4521(4)
-
|
| ДР |
вакуум |
860 |
ZrCr2
(С15)
d-ZrHx
Cr
|
0,7208(1)
0,4601(2)
0,28867(1)
|
-
-
-
|
Після десорбції-рекомбінації продуктів повного розпаду ZrCr2
(С14) формується низькотемпературна фаза Лавеса з кубічною ґраткою (структурний тип MgCu2
(C15). Нагрів у вакуумі частково диспропорціонованої ZrCr2
(С14) завершується відновленням вихідної фази зі структурою типу С14.
Під час проведення Solid-ГДДР фазовий склад продуктів взаємодії аналогічний.
На прикладі сплавів Zr1-x
Tix
Cr2
(x=0,1; 0,2) досліджено вплив легування титаном на умови та особливості протікання процесу ГДДР. Сплав частково диспропорціонує за 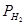 =5 і 3 МПа. За =5 і 3 МПа. За 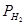 =5 МПа для повного розпаду сплаву з 0,1 ат.Ti/ф.о. потрібна витримка ~4 год (табл. 3), а для сплаву з 0,2 ат.Ti/ф.о. ~17 год (табл. 4). Продуктами розпаду в обох випадках є e-ZrHx
, TiHx
та Cr . Після десорбції-рекомбінації продуктів повного розпаду формується фаза Лавеса з кубічною ґраткою структурного типу MgCu2
(C15). =5 МПа для повного розпаду сплаву з 0,1 ат.Ti/ф.о. потрібна витримка ~4 год (табл. 3), а для сплаву з 0,2 ат.Ti/ф.о. ~17 год (табл. 4). Продуктами розпаду в обох випадках є e-ZrHx
, TiHx
та Cr . Після десорбції-рекомбінації продуктів повного розпаду формується фаза Лавеса з кубічною ґраткою структурного типу MgCu2
(C15).
Таблиця 3. Умови та фазовий склад продуктів взаємодії у системі
Zr0,9Ті0,1Cr2-Н2
| Умови взаємодії |
Фазовий склад
(ст. тип)
|
Параметри ґратки (нм) |
| Режим |
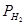 , MПa , MПa |
Tмакс
, °С |
ф, год |
a |
c |
| Вихідний сплав |
Zr0,9
Ті0,1
Cr2
(С14) |
0,5098(2) |
0,8257(3) |
| ГД |
3 |
950 |
0 |
Zr0,9
Ті0,1
Cr2
Hx
(C14)
e-ZrHx
, Cr – сліди
|
0,5387(1) |
0,8793(4) |
| ГД |
5 |
950 |
0 |
Zr0,9
Ті0,1
Cr2
Hx
(C14)
e-ZrHx
Cr
|
0,5365(1)
0,3504(1)
0,28861(3)
|
0,8768(4)
0,4448(3)
-
|
| ДР |
Вакуум |
950 |
0 |
С14 |
0,51036(2) |
0,82595(4) |
| ГД |
5 |
950 |
4 |
e-ZrHx
Cr
Zr0,9
Ті0,1
Cr2
Hx
(C14),
TiHx
– сліди
|
0,3488(2)
0,28899(2)
|
0,4488(4)
-
|
| ДР |
Вакуум |
250 |
0 |
Zr0,9
Ті0,1
Cr2
(C14)
e-ZrHx
Cr
|
0,5111(1)
0,3504(2)
0,28919(4)
|
0.8272(5)
0,4472(4)
-
|
| ДР |
Вакуум |
525 |
0 |
Zr0,9
Ті0,1
Cr2
(C14)
d-ZrHx
Cr
|
0,5113(1)
0,4776(1)
0,28917(4)
|
0,8246(4)
-
-
|
| ДР |
Вакуум |
800 |
0 |
Zr0,9
Ті0,1
Cr2
(C15)
a-Zr
Cr
Zr0,9
Ті0,1
Cr2
(C14),
d-ZrHx
– сліди
|
0,7210(1)
0,3239(1)
0,28951(3)
|
-
0,5156(4)
-
|
| ДР |
Вакуум |
950 |
0 |
Zr0,9
Ті0,1
Cr2
(C15)
d-ZrHx
Cr
|
0,7206(1)
0,4681(2)
0,28939(4)
|
-
-
-
|
| ДР |
Вакуум |
950 |
3 |
Zr0,9
Ті0,1
Cr2
(C15)
d-ZrHx
Cr
|
0,7199(1)
0,4676(1)
0,2891(1)
|
-
-
-
|
Реакція рекомбінації в цьому випадку є незавершеною. Після нагріву у вакуумі частково диспропорціонованого зразка вихідна фаза сплаву відновлюється.
Таблиця 4. Умови та фазовий склад продуктів взаємодії у системі
Zr0,8Ті0,2Cr2-Н2
| Умови взаємодії |
Фазовий склад
(ст. тип)
|
Параметри ґратки (нм) |
| Режим |
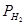 , MПa , MПa |
Tмакс
, °С |
ф, год |
a |
c |
| Вихідний сплав |
Zr0,8
Ti0,2
Cr2
(С14) |
0,5081(1) |
0,8233(3) |
| ГД |
5 |
900 |
0 |
Zr0,8
Ti0,2
Cr2
Hx
(C14)
Cr
e-ZrHx
- сліди
|
0,5357(1)
0,28917(8)
|
0,8734(4)
-
|
| ДР |
Вакуум |
950 |
0 |
Zr0,8
Ti0,2
Cr2
(C14) |
0,50869(6) |
0,8236(1) |
| ГД |
5 |
950 |
12 |
Zr0,8
Ti0,2
Cr2
Hx
(C14)
e-ZrHx
Cr
TiHx
- сліди
|
0,5352(4)
0,3491(2)
0,28932(6)
|
0,8752(7)
0,4489(3)
-
|
| ДР |
Вакуум |
950 |
0 |
Zr0,8
Ti0,2
Cr2
(C15)
Zr0,8
Ti0,2
Cr2
(C14)
Cr
d-ZrHx
- сліди
|
0,7201(2)
0,5097(1)
0,28956(5)
|
-
0,8261(2)
-
|
| ГД |
5 |
950 |
17 |
e-ZrHx
Cr
TiHx
- сліди
|
0,3498(3)
0,28960(5)
|
0,4492(6)
-
|
| ДР |
Вакуум |
950 |
0 |
Zr0,8
Ti0,2
Cr2
(C15)
d-ZrHx
Cr
|
0,7200(2)
0,4665(2)
0,2896(1)
|
-
-
-
|
| ДР |
Вакуум |
950 |
3 |
Zr0,8
Ti0,2
Cr2
(C15)
d-ZrHx
Cr
|
0,7190(2)
0,4650(1)
0,28958(5)
|
-
-
-
|
Таким чином, показано, що часткове заміщення цирконію титаном у сполуці ZrCr2
призводить до зменшення швидкості фазових перетворень.
Основу електродного сплаву ZrCrNi складає фаза Лавеса з гексагональною ґраткою структурного типу MgZn2
(С14) і, як домішки, присутні фази Zr7
Ni10
, Zr9
Ni11
та Cr (рис. 3а).
За даними ДТА під час нагріву сплаву ZrCrNi до 950 °C за початкового тиску 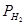 = 5 MРа, крім піку, зумовленого утворенням гідриду сплаву за кімнатної температури, зафіксовано ще чотири теплові ефекти. Два екзотермічні при 535 і 675 °С та два ендотермічні при 790 і 820 °С. Для встановлення фізичної природи фазових перетворень зразки нагрівали до 610, 750 та 810 °С, тобто вище температури відповідних фазових перетворень на термограмі. Рентгенофазовим аналізом показано, що сплав ZrCrNi після нагріву до 610 °С ( = 5 MРа, крім піку, зумовленого утворенням гідриду сплаву за кімнатної температури, зафіксовано ще чотири теплові ефекти. Два екзотермічні при 535 і 675 °С та два ендотермічні при 790 і 820 °С. Для встановлення фізичної природи фазових перетворень зразки нагрівали до 610, 750 та 810 °С, тобто вище температури відповідних фазових перетворень на термограмі. Рентгенофазовим аналізом показано, що сплав ZrCrNi після нагріву до 610 °С (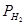 =5 MPа) частково диспропорціонує з утворенням гідриду на основі фази Лавеса (структурний тип С14), гідриду цирконію та хрому . =5 MPа) частково диспропорціонує з утворенням гідриду на основі фази Лавеса (структурний тип С14), гідриду цирконію та хрому .
Після нагріву до 750 °С вихідний сплав ZrCrNi (фаза Лавеса С14) зазнає повного розпаду на e-ZrHx
, Cr, та ZrNi3
. Аналогічний фазовий склад отримали при витримці протягом 4-5 год при 610 °С. Підвищення температури до 810 °С призводить до розпаду фази ZrNi3
та зменшення відносної інтенсивності піків гідриду цирконію. При цьому з’являється кілька рефлексів фази Zr2
Ni7
. В результаті нагріву до 950 °С вихідний сплав розпадається на e-ZrHx
, Cr, Zr2
Ni та Zr2
Ni7
.
Нагрів у вакуумі продуктів часткового диспропорціонування призводить до відновлення фази Лавеса зі структурою типу С14, яка була у вихідному сплаві . Після водневої обробки сплав гомогенізується (зникають рефлекси фази Zr9
Ni11
). Після нагріву у вакуумі продуктів повного розпаду формується фаза Лавеса зі структурою типу С15 та інтерметалідні фази з системи Zr-Ni ( табл. 5).
4
Дослідження впливу водневої обробки на розрядні характеристики сплаву ZrCrNi
Оптимізовано умови і встановлено вплив механо-хімічного помелу та фазово-структурного стану сплаву на розрядні характеристики сформованих на його основі металогідридних електродів.
Помел у планетарному млині є високопродуктивним способом подрібнення матеріалів, однак у випадку застосування його для отримання порошків електродних матеріалів існують вади, пов’язані зі зниженням максимальної розрядної ємності.
Таблиця 5. Умови та фазовий склад продуктів взаємодії у системі ІМС
ZrCrNi-Н2
| Умови взаємодії |
Фазовий склад
(ст. тип)
|
Параметри ґратки, нм |
| Режим |
Tмакс
, °C |
а |
b |
с |
| Вихідний сплав |
ZrCrNi (C14)
Zr7
Ni10
, Zr9
Ni11
,Cr - сліди
|
0,50124(8)
|
- |
0,8214(2) |
| ГД |
610 |
ZrCrNiНх
(C14)
e-ZrHx
Cr - сліди
|
0,5286(2)
0,3489(3)
|
-
-
|
0,8620(8)
0,4530(7)
|
| ДР |
270 |
ZrCrNi (C14)
d-ZrHx
, Cr - сліди
|
0,5013(2) |
- |
0,8209(4) |
| ДР |
530 |
ZrCrNi (C14)
Zr7
Ni10
, Cr - сліди
|
0,50077(8)
|
- |
0,8211(2) |
| ДР |
950 |
ZrCrNi (C14)
Zr7
Ni10
Cr - сліди
|
0,50181(7)
1,2380(9)
|
-
0,9211(7)
|
0,8224(2)
0,9193(6)
|
| ГД |
750 або
610,
t=4-5 год
|
e-ZrHx
ZrNi3
Cr
|
0,3500(1)
0,5309(2)
0,28853(2)
|
-
-
-
|
0,4493(3)
0,4298(3)
-
|
| ДР |
950 |
ZrCrNi (C15)
ZrCrNi (C14)
ZrNi
Cr
|
0,7097(1)
0,5014(3)
0,3261(2)
0,28853(4)
|
-
-
0,9972(6)
-
|
-
0,8167(6)
0,4094(3)
-
|
| ГД |
810 |
e-ZrHx
Cr
Zr2
Ni7
- сліди
|
0,3502(2)
0,28845(6)
|
-
-
|
0,4482(3)
-
|
| ДР |
950 |
ZrCrNi (C15)
ZrCrNi (C14)
ZrNi
Cr
Zr9
Ni11
- сліди
|
0,70955(8)
0,5012(5)
0,3267(3)
0,28847(6)
|
-
-
0,9894(7)
-
|
-
0,819(1)
0,4108(4)
-
|
| ГД |
950 |
e-ZrHx
Cr
Zr2
Ni7
, Zr2
Ni - сліди
|
0,3500(2)
0,28836(6)
|
-
-
|
0,4476(3)
-
|
| ДР |
660 |
Zr7
Ni10
ZrNi
Cr
ZrHx
, Zr2
Ni - сліди
|
1,235(2)
0,3253(4)
0,28836(6)
|
0,9168(7)
0,992(1)
-
|
0,9183(7)
0,4117(5)
-
|
| ДР |
950 |
ZrCrNi (C15)
ZrCrNi (C14)
ZrNi
Cr
|
0,7097(1)
0,5006(4)
0,3265(2)
0,28852(3)
|
-
-
0,9945(8)
-
|
-
0,821(2)
0,4107(4)
-
|
На нашу думку, причина погіршення експлуатаційних характеристик зумовлена напруженнями, які виникають у матеріалі після помелу, та з частковими аморфізацією та диспропорціонуванням сплаву. На це вказує поява гало й розширення ліній на дифрактограмі меленого сплаву та сліди продуктів диспропорціонування, зокрема виділень хрому . Оптимізація умов помелу полягала у зниженні частоти обертання млина (табл. 6), що запобігає аморфізації та диспропорціонуванню сплаву .
Таблиця 6. Умови подрібнення та розрядні характеристики металогідридних електродів з композиту ZrCrNi+Ni
| Умови помелу |
Сплав-звязка,
мас. частки
|
Обробка |
N, кількість |
Iр
, мА/г |
Смакс
,мА·год/г |
| н, об/хв |
ф, хв |
| 400 |
15 |
2:1 |
- |
- |
25 |
172 |
| 300 |
20 |
2:1 |
+1
|
1 |
25 |
240 |
| 100 |
30 |
2:1 |
- |
4 |
50 |
228 |
| 100 |
30 |
2:1 |
-2
|
20 |
50 |
264 |
| 100 |
30 |
2:1 |
+3
|
2 |
50 |
293 |
| 100 |
30 |
2:1 |
+4
|
6 |
50 |
246 |
Примітки: 1
заряд при 80 °С, Із
=50 мА·год/г, ф=8 год; 2
сплав попередньо подрібнений у ступці; 3
ГДДР 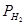 =5 МПа, ГД при 610°С, ДР при 950°С; 4
ГДДР =5 МПа, ГД при 610°С, ДР при 950°С; 4
ГДДР 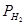 =5 МПа, ГД при 810 °С, ДР при 950°С. =5 МПа, ГД при 810 °С, ДР при 950°С.
Сплави після механохімічного здрібнення потребують малої кількості циклів активації, однак володіють нижчою ємністю. Для усунунення негативних наслідків помелу проводили гомогенізуючу водневу обробку сплаву (процес ГДДР): нагрів до 610 °С у водні з наступним нагрівом до 950 °С у вакуумі.
Внаслідок застосування такого комплексного підходу отримали високу активованість електродів без зниження їх розрядної ємності. Високий ступінь гомогенності сплаву забезпечує, на нашу думку, його високу розрядну ємність. Такий помел у механічному млині у водні запобігає оксидуванню порошку сплаву, що забезпечує високу активованість електроду.
Електроди, виготовлені з гомогенізованого сплаву зі структурою типу С14 вже після другого циклу заряду-розряду досягають ємності 260 мА·год/г, тобто близько 90% від максимальної (293 мА·год/г). Коли основою електродного сплаву є фаза зі структурою типу С15, отримана при нагріві у водні до 810 °С, а потім до 950 °С у вакуумі, то 90% від максимальної ємності досягається після 8 циклів, що становить 256 мА·год/г. Зниження максимальної розрядної ємності зумовлене формуванням бінарних ІМС сполук системи Zr-Ni.
Таким чином, комплексне застосування процесу ГДДР та механохімічної обробки дозволяє зменшити кількість циклів для активації електродів з 20 до 2 (рис. 6, крива 5). На нашу думку, отриманий результат пояснюється впливом двох факторів: відновленням поверхневих оксидних плівок та гомогенізацією сплаву внаслідок проведення ГДДР.
Висновки
1. Встановлено закономірності ГДДР в сполуці ZrCr2
двох структурних модифікацій (типу MgZn2
та MgCu2
). Показано, що диспропорціонування ZrCr2
(структура типу MgZn2
) починається за 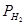 =3 МПа з утворенням гідриду вихідної фази та виділенням хрому і гідриду цирконію. Повністю сплав диспропорціонує за витримки 3 год при 860 °С, або за початковому тиску водню =3 МПа з утворенням гідриду вихідної фази та виділенням хрому і гідриду цирконію. Повністю сплав диспропорціонує за витримки 3 год при 860 °С, або за початковому тиску водню 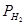 =5 МПа. Нагрів у вакуумі продуктів часткового диспропорціонування сполуки ZrCr2
приводить до відновлення вихідної фази. Аналогічна обробка продуктів повного диспропорціонування завершується утворенням сполуки ZrCr2
зі структурою типу MgCu2
. У випадку сполуки ZrCr2
структурного типу MgCu2
вона розпадається на e-ZrHx
та Cr за температур 820 та 775 °С ( =5 МПа. Нагрів у вакуумі продуктів часткового диспропорціонування сполуки ZrCr2
приводить до відновлення вихідної фази. Аналогічна обробка продуктів повного диспропорціонування завершується утворенням сполуки ZrCr2
зі структурою типу MgCu2
. У випадку сполуки ZrCr2
структурного типу MgCu2
вона розпадається на e-ZrHx
та Cr за температур 820 та 775 °С (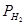 =3 та 5 МПа відповідно) з подальшим відновленням вихідної фази нагрівом продуктів диспропорціонування у вакуумі. =3 та 5 МПа відповідно) з подальшим відновленням вихідної фази нагрівом продуктів диспропорціонування у вакуумі.
2. Вперше показано, що заміщення цирконію на титан зменшує швидкість фазових перетворень у сполуці ZrCr2
при нагріві у водні. Повний розпад сплаву Zr1-x
Tix
Cr2
на e-ZrHx
, ТіНх
та Cr має місце після 4 і 17 год витримки (для x=0,1 і 0,2 відповідно) при 950 °С за 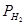 =5 МПа. =5 МПа.
3. Вперше встановлено, що фазові перетворення у системі ZrCrNi-H2
при 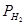 =5 MПa розпочинаються при 535 °С з утворенням гідриду вихідної фази Лавеса зі структурою типу MgZn2
, Cr та e-ZrHx
. Після нагріву до 675 °С утворюються e-ZrHх
, ZrNi3
та Cr; за температури вище 790 °С: e-ZrHх
, Zr2
Ni7
та Cr; вище 820 °С: e-ZrHх
, Zr2
Ni7
, Zr2
Ni та Cr. =5 MПa розпочинаються при 535 °С з утворенням гідриду вихідної фази Лавеса зі структурою типу MgZn2
, Cr та e-ZrHx
. Після нагріву до 675 °С утворюються e-ZrHх
, ZrNi3
та Cr; за температури вище 790 °С: e-ZrHх
, Zr2
Ni7
та Cr; вище 820 °С: e-ZrHх
, Zr2
Ni7
, Zr2
Ni та Cr.
4. В залежності від максимальної температури обробки отримано сплав з різним співвідношенням основних та вторинних фаз: фази Лавеса зі структурою типу MgZn2
та MgCu2
, ZrNi, Cr, Zr9
Ni11
і Zr7
Ni10
. Встановлено, що обробка у водні гомогенізує сплав ZrCrNi.
5. Покращення активованості металогідридних електродів на основі сполуки ZrCr2
зумовлене сумісним впливом двох процесів – відновленням оксидних плівок у водні та гомогенізацією внаслідок застосування ГДДР.
6. Оптимізовано параметри проведення процесу ГДДР та механохімічного помелу сплаву ZrCrNi у водні та видано рекомендаціїї щодо практичного впровадження отриманих результатів.
Література
1. Bulyk I.I., Basaraba Yu. B., Trostianchyn A.M. Features of the HDDR process in ZrT2
(T = Cr, Mn, Fe, Co) compounds // J. Alloys and Compounds. - 2004. -Vol.367. - P. 283-288.
2. Булик І.І., Басараба Ю.Б., Тростянчин А.М. Вплив титану на спричинені воднем перетворення у фазах Лавеса на основі цирконію // Фіз.-хім. механіка матеріалів. - 2004. - № 6. - С. 67-72.
3. Bulyk I.I., Basaraba Yu. B., Dovhyj Ya. O. Influence of Ti on the hydrogen-induced phase-structure transformations in the ZrCr2
intermetallic compound // Intermetallics. - 2006. – Vol.14. - P. 735-741.
4. Bulyk I.I., Basaraba Yu. B., Trostianchyn A.M. Effect of hydrogen on the phase-structure transformations in ZrCrNi alloy // J. Alloys and Compounds. - 2004. – Vol.376. - P. 95-104.
5. Булик І.І., Басараба Ю.Б., Тростянчин А.М., Давидов В.М. Диспропорціонування у водні та рекомбінування фаз Лавеса цирконію з хромом // Фіз.-хім. механіка матеріалів. - 2005. - № 3. - С. 101-108.
6. Булик І.І., Басараба Ю.Б. Вплив водневої обробки на розрядні властивості електродів зі сплаву ZrCrNi // Фіз.-хім. механіка матеріалів. - 2005. - № 5. - С. 49-54.
7. Пат. 51233 Україна, МКІ С22F1/18, 1/02. Спосіб гомогенізації інтерметалічних сполук гідридоутворюючих металів: Пат. 51233 Україна, МКІ С22F1/18, 1/02 Булик І.І., Федоров В.В., Тростянчин А.М, Басараба Ю.Б., Синюшко В.Г. (Україна); Фізико-механічний інститут ім. Г.В. Карпенка. - № 2002020928; Заявл. 05.02.2002; Опубл. 15.09.2005, Бюл. № 9. – 4 с.
8. Булык И.И., Федоров В.В., Тростянчин А.Н., Басараба Ю.Б., Сынюшко В.Г. Гомогенизационный отжиг интерметаллических соединений гидридообразующих металлов в водороде // Сборник докладов 3-й Междунар. конф. “Оборудование и технологии термической обработки металлов и сплавов” (ОТТОМ-3). - Харьков: ННЦ ХФТИ, ИПЦ “Контраст”, 2002. - Часть 1. - С. 186-190.
|